Принцип. Анализ фенола в смеси с другими соединениями с использованием газового хроматографа позволяет определять индивидуальные компоненты в воде; точность определения 0,001 мг/л. Анализ состоит из трех стадий — экстрагирования фенола и сопутствующих органических соединений из воды, концентрирования экстракта, хроматографического определения фенола.
Аппаратура. Делительная воронка вместимостью 2 л для экстракции (пробку и кран смазывать нельзя). Мерные цилиндры объемом 100 и 1000 мл. Мерные колбы с притертыми пробками вместимостью 10 мл, пипетки на 1 мл; конические колбы для сбора и сушки экстрактов. Грушевидные колбы для концентрирования экстрактов. Водяная баня.
Хроматограф газовый с двумя колонками, пламенно-ионизационным детектором и термостатом, имеющим систему программирования температуры, самописцем с ценой деления на шкале 1 мВ, микрошприцы на 10 и 50 мкл.
Хроматографические колонки. Две одинаковые колонки из нержавеющей стали внутренним диаметром 3 мм, длиной 2 м, заполненные Хроматоном N-AW с 5% Carbowax 20 М и Хроматоном N-AW с 5% SE-30.
Условия хроматографического разделения. Газ-носитель — азот особой чистоты. Скорость газа-носителя 40 мл/мин. Расход воздуха 200 мл/мин, расход водорода 50 мл/мии. Температура испарителя 300° С. Скорость движения диаграммной ленты 600 мм/ч.
Температура термостата колонок программируется от 60 до 250е С со скоростью 4 град/мин.
Реактивы. Гексан перегнанный. Едкий натр, 10%-ный раствор. Эфир диэтиловый. Натрий хлористый. Соляная кислота, 10%-ный раствор.
Сульфат натрия безводный, прокаленный.
Фенолы, набор стандартных растворов.
Парафины, набор стандартов.
Универсальная индикаторная бумага.
Основной раствор фенолов. В 10 мл диэтилового эфира растворяют 0,1 г фенола, 0,1 г о-крезола, 0,1 г п-крезола, 0,1 г гидрохинона.
Рабочий раствор 1. В мерную колбу на 10 мл помещают 0,2 мл основного раствора, добавляют до метки диэтиловый эфир (Cj).
Рабочий раствор 2 В мерную колбу на 10 мл помещают 0,5 мл рабочего раствора 1, добавляют до метки диэтиловый эфир. Концентрация каждого компонента в растворе С2=0,01 мг/мл.
Калибровочная кривая. Одним из общепринятых методов количественного определения веществ в экстрактах является абсолютная калибровка. Поскольку чувствительность детектора к различным веществам неодинакова, при количественном анализе необходимо строить калибровочные кривые зависимости площади пика от количества введенного в хроматограф вещества. Если при анализе микропримесей применяется метод абсолютной калибровки, то в хроматограф вводят пробы разной величины. Микрошприцем последовательно вводят в испаритель хроматографа рабочий раствор 2 объемом 1, 2, 5, 10 мкл на его полуширину (ширину на половине высоты); можно воспользоваться планиметром или интегратором. Затем строят калибровочную функцию зависимости площади пика (Sn, мм2) от количества введенного вещества для каждого ί-го компонента, которое определяют по формуле
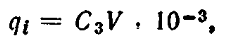
где С3 — концентрация калиброванного раствора, мг/мл; V —объем раствора в микрошприце, мкл.
В случае необходимости калибровочную функцию можно продолжать в сторону больших или меньших qt пользуясь теми же рабочими растворами. Определение проводят в линейном диапазоне работы детектора.
Ход определения. К 1 л пробы (Vo) добавляют раствор едкого натра до pH 8—9, раствор переносят в делительную воронку и добавляют 20 мл гексана. Воронку сильно встряхивают в течение 5 мин, дают отстояться для разделения слоев и отделяют гексановый экстракт. Экстракцию повторяют свежей порцией гексана. Вытяжки объединяют и используют для анализов на нефтепродукты и другие органические соединения. К водной части добавляют хлористый натрий (100 г NaCl на 1 л пробы) и подкисляют соляной кислотой до pH 3. Полученный раствор в делительной воронке экстрагируют трижды диэтиловым эфиром порциями последовательно по 100, 50 и 50 мл. Эфирные экстракты сливают в одну колбу, сушат безводным сульфатом натрия, переливают в грушевидную колбу и упаривают на водяной бане до объема (VH) 0,5—1 мл. Из этого объема микрошприцем отбирают пробу (V) от 5 до 20 мкл для анализа в газовом хроматографе. Экстракты фенолов можно хранить в герметично закрытой посуде в течение 12 дней.
Расчет. Пики идентифицируют по относительным параметрам удержания (время, объемы) в стандартных условиях разделения. Пики, характерные для фенола, должны быть на хроматограммах, снятых для каждой неподвижной фазы.
Определяют площади пиков, соответствующих фенолу. На-
ходят среднюю величину площади

калибровочной кривой определяют qi Концентрацию вещества в исходной пробе (мг/л) определяют по формуле
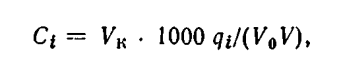
где V0— объем пробы, взятой для анализа, л; Vk — объем экстракта после упаривания, мл; V — объем пробы в микрошпрнце, мкл; qi — количество детектированного вещества, определенное по калибровочной кривой, мг [7, стр. 89].
Заключение
Для определения фенола применяют различные физико-химические методы анализа. В данной курсовой работе описаны следующие методы: фотоколориметрия, газожидкостная хроматография, высокоэффективная жидкостная хроматография.
В основе фотоколориметрического метода лежит реакция образования азосоединения при действии хлористого нитродиазобензола на отогнанный с водяным паром фенол, в кислой среде. Данное азосоединение окрашивает раствор в слабо-оранжевый цвет. Этот раствор колориметрируют на фотоэлектроколориметре. По интенсивности окраски раствора с помощью градуировочного графика находят содержание фенола.
При определении фенола методом газожидкостной хроматографии используют газовый хроматограф. Это позволяет определять индивидуальные компоненты в воде; точность определения 0,001 мг/л. Анализ состоит из трех стадий — экстрагирования фенола и сопутствующих органических соединений из воды, концентрирования экстракта, хроматографического определения фенола.
При хроматографическом определении и разделении фенола и сопутствующих веществ можно использовать различные наполнители хроматографической колонки: Хроматон N-AW с 5% Carbowax 20 М и Хроматон N-AW с 5% SE-30.
Одним из общепринятых методов количественного определения веществ в экстрактах при хроматографическом определении является абсолютная калибровка. Поскольку чувствительность детектора к различным веществам неодинакова, при количественном анализе необходимо строить калибровочные кривые зависимости площади пика от количества, введенного в хроматограф вещества. Если при анализе микропримесей применяется метод абсолютной калибровки, то в хроматограф вводят пробы разной величины.
Библиографический список
1. Ляликов, Ю.С. Физико-химические методы анализа/ Ю.С. Ляликов. – Москва: Высшая школа, 1951. – 308 с.
2. Харлампович Г. Д., Чуркин Ю. В. Фенолы./ Г.Д. Харлампович, Ю.В. Чуркин. М., «Химия», 1974. 376 с.
3. ГОСТ 23519-93. Фенол синтетический технический. – Москва: Изд-во стандартов, 1981. – 12 с.
4. Черных В.П. Органическая химия./ В.П. Черных, Б.С. Зименковский, И.С. Гриценко. Под общ. ред. В.П. Черных. - 2-е изд., испр. и доп. - Х.: Изд-во НфаУ; Оригинал, 2007. - 776 с
5. Закошанский В. М. Фенол и ацетон: Анализ технологий, кинетики и механизма основных реакций./ В.М. Закошанский - СПб.: ХИМИ8ДАТ, 2009. - 608 с.: ил.
6. Белянин Б. В., Эрих В. Н. Технический анализ нефтепродуктов и газа: Учебное пособие для техникумов. — 4-е изд., пере- раб. — Л.: Химия, 1979. — 224 с., ил.
7. Методика технологического контроля работы очистных сооружений городской канализации. Изд. 3-е, перераб. и доп. М., Стройиздат, 1977. 299 с.






