Из анализа величин скорости образования зародышей и скорости роста кристаллов следует, что эти характеристики имеют два важных свойства. Во-первых, они всегда конечны по величине. Во-вторых, при уменьшении температуры вследствие роста кинетических затруднений, значения скоростей роста зародышеобразования и их дальнейшего роста уменьшаются до нуля. Следовательно, их произведение, характеризующее долю закристаллизованного объема, тоже имеет конечную величину и в области низких температур превращается в ноль. Это значит, что для любого вещества можно подобрать такую скорость охлаждения, при которой в случае охлаждения до абсолютного нуля в расплаве возникнет кристаллическая фаза, объемная доля которой будет заведомо меньше какой-либо наперед заданной величины. Как указывалось выше, если охлаждать жидкость, которая обладает стеклообразующей способностью, от температуры, равной температуре плавления, до температуры Т, которая лежит ниже температуры стеклования Тg с такой скоростью q, что в единице объема возникает всего один центр кристаллизации (Nk =1), то полученное таким образом вещество фактически не будет содержать кристаллических включений и по существу будет стеклообразным. В данном случае скорость q, введенная физически строго, не может быть непосредственно сопоставлена с экспериментальными результатами.
Практически для анализа и экспериментальных исследований используют величину критической скорости охлаждения как минимальной скорости охлаждения расплава от температуры плавления, при которой в жидкости объемная доля кристаллической фазы не превышает некоторого наперед заданного значения. Впервые этот подход применил Улманн для расчета критической скорости охлаждения.
Для расчета критической скорости охлаждения по Улманну можно воспользоваться уравнением Колмогорова – Аврами для зависимости доли закристаллизованного объема от времени в упрощенном виде (18). Пусть доля закристаллизованного объема равна 10-6, что в стеклообразном материале экспериментально не определяется и считается, что материал кристаллических включений не содержит.
По уравнению (18) можно рассчитать для каждой температуры время, в течение которого в переохлажденной жидкости образуется указанное выше количество кристаллической фазы. При подстановке численных значений в уравнение (18), получается следующее выражение:
t = 34 [π I (T) u3(T)]1/4.
Полученные величины можно отложить на зависимости температура – время (рис.8). Кривая на рис.8, напоминающая по форме нос, называется Т – t - α кривой. Точки, лежащие внутри кривой, соответствуют условиям выдержки, при которых в образце вырастает кристаллическая фаза, объемная доля которой свыше заданной величины 10-6. Линейному режиму охлаждения от температуры плавления отвечает прямая (см. рис.8).
Очевидно, что для касательной к Т - t - α кривой, выходящей из точки Тпл, выполняется условие α < 10-6. Скорость охлаждения, соответствующая этой прямой, и является критической скоростью охлаждения для данной доли кристаллической фазы.
Достоинство представленного метода состоит в его простоте и наглядности. Однако, далеко не во всех случаях полученные результаты удовлетворительно согласуются с экспериментом, даже если наперед заданная величина объемной доли закристаллизованной фазы значительно увеличена (например, до 5%).
В качестве примера можно рассмотреть данные по критическим скоростям охлаждения халькогенидов мышьяка (табл.1).
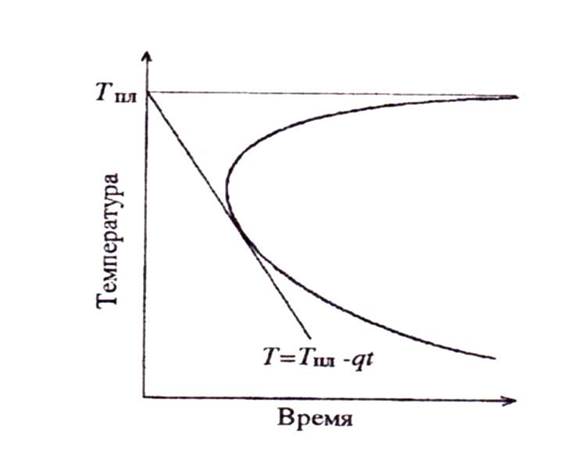
Рис.8. Общий вид Т - t - α диаграммы.
Таблица 1. Критические скорости охлаждения халькогенидов мышьяка.
| Соединение | Тпл, К | Критическая скорость охлаждения, К/с | |||
| по (18) | α=10-6 по (21) | α=0.05 по (21) | Эксперимент | ||
| As2O3 | 1.4.10-4 | 2.7.10-5 | 1.8.10-6 | < 2.10-5 | |
| As2S3 | 3.1.10-4 | 3.9.10-5 | 2.6.10-6 | < 2.10-5 | |
| As2Se3 | 0.44 | 5.1.10-2 | 3.4.10-3 | (9±2).10-3 | |
| As2Te3 | 4.2 | 28±3 |
Основная причина такого несоответствия заключается в автоматическом переносе результатов расчета скорости кристаллизации при изотермическом отжиге на неизотермический режим реального охлаждения образца. Более достоверный метод оценки критической скорости охлаждения должен основываться на расчетах по обобщенному уравнению Колмогорова – Аврами, которое для неизотермических условий (т.е. когда I и u являются функциями времени) может быть записано в следующем виде:
α(t) = 1 - exp  . (20)
. (20)
Для случая линейного охлаждения со скоростью q в уравнении (20) время может быть заменено на температуру и тогда
α(Т) = 1 - exp  . (21)
. (21)
Используя уравнение (21), можно найти скорость охлаждения q, при которой доля кристаллической фазы в стекле будет равна некоторой наперед заданной величине (например, 5%). В табл.1 представлены величины рассчитанных таким образом критических скоростей охлаждения халькогенидов мышьяка.
Экспериментально критическую скорость охлаждения находят при охлаждении расплава с определенной скоростью; при этом по ходу охлаждения непосредственно исследуется процесс кристаллизации расплава, либо наличие кристаллической фазы определяется в образце после охлаждения. Для примера на рис. 9 приведены концентрационные зависимости критических скоростей охлаждения в трех халькогенидных системах. Видно, что максимуму критических скоростей охлаждения соответствуют составы соединений, плавящихся конгруэнтно (с открытым максимумом). Также характерной особенностью является уменьшение критической скорости охлаждения при приближении состава к эвтектическому. На основании изложенного выше, величина критической скорости охлаждения сложным образом зависит от внутренних параметров вещества (теплота и температура плавления, вязкость и энергия активации вязкого течения, поверхностного натяжения на границе жидкость-кристалл). При этом, например, для селенидов мышьяка, наибольшее влияние на величину критической скорости охлаждения оказывает температура плавления. Именно поэтому в системах с эвтектическим характером взаимодействия компонентов составы с минимальной критической скоростью охлаждения близки к составам эвтектик.
Критическая скорость охлаждения может рассматриваться в качестве количественной меры стеклообразующей способности. Действительно, чем меньше критическая скорость охлаждения, тем более мягкими являются условия получения вещества в стеклообразном состоянии, тем легче может быть получено стекло.
С точки зрения кинетической теории стеклообразования для любого вещества можно подобрать критическую скорость охлаждения, при которой оно может быть переведено в стеклообразное состояние без кристаллизации. Поэтому, строго говоря, вопрос о том, какие вещества могут при охлаждении образовывать стекла, смысла не имеет. В основном, существующие на этот счет ограничения связаны с максимальными размерами образца, который может быть получен в стеклообразном состоянии. Проиллюстрировать это можно следующим образом.
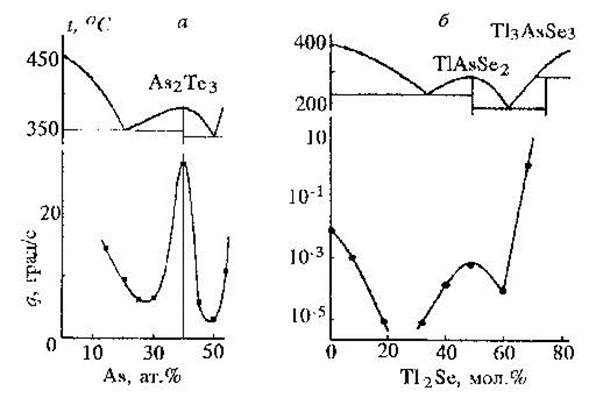

Рис.9. фрагмент диаграммы состояния и концентрационная зависимость критической скорости охлаждения в системах As-Te (a), As2Se3-Tl2Se (б) As2Te3-Tl2Te (в).
Рассмотрим каплю жидкости радиуса r, которая находится при температуре плавления. Охлаждение центра капли с максимально возможной скоростью будет протекать в том случае, если каплю поместить в среду, абсолютная температура которой Т=0. Временная зависимость температуры в центре капли может быть найдена из уравнения теплопроводности, представленного в следующем виде:
 или
или  ,
,
где λ – теплопроводность жидкости, Cp - теплоемкость жидкости, Q - количество теплоты. С учетом начальных условий (t=0, Т=Тпл), считая, что, после разделения переменных и интегрирования, можно получит приближенную зависимость температуры в центре капли от времени охлаждения
T = Тплexp  .
.
Для получения стекла необходимо переохладить жидкость до температуры стеклования Тg, которая согласно эмпирической закономерности обычно составляет около 0.667 Тпл. Время охлаждения до этой температуры равно
t = r Cpln  .
.
Для идентификации образца необходимо, чтобы его толщина имела макроскопическую величину порядка 1 мкм. С учетом этой величины, а также с учетом типичных значений теплоемкости (1 Дж . град-1. см-3), теплопроводности неметаллических жидкостей (4 . 10-2 Дж . см-2 . с-1 . град-1) получается значение t ≈ 0.001 с. Для Тпл= 1000 К и Тg = 600 К это соответствует средней скорости охлаждения в 4 . 105 К/с. Данное значение скорости (с точностью до двух порядков) можно считать предельным значением скорости охлаждения, которая может быть достигнута для получения вещества в стеклообразном состоянии. Следовательно, с макроскопической точки зрения граница между стеклообразующими и нестеклообразующими жидкостями находится вблизи критической скорости охлаждения порядка 107 К/с.
Таким образом, при помощи понятия «критическая скорость охлаждения» современная теория кристаллизации жидкостей позволяет определить способность любого вещества к стеклообразованию. Однако для высокоточных расчетов необходимо знать такие свойства вещества, как теплота и температура плавления, а главное, параметры температурной зависимости вязкости переохлажденной жидкости. Именно последнее свойство практически сводит на нет предсказательные возможности кинетической теории стеклообразования. С другой стороны, из этого следует, что проблема стеклообразования является частной проблемой взаимосвязи свойств вещества и его строения.
Трудности применения кинетической теории к описанию процессов стеклообразования в конкретных системах обусловливает существование многочисленных эмпирических критериев, связывающих возможность образования стекол в конкретных системах с некоторыми свойствами этих систем (такими, как электронная структура потенциально стеклообразующих атомов, их координационное число, характер и энергия химического взаимодействия между ними, температура ликвидуса, количество и тип структурных элементов, вязкость и т.п.). Все эти трудности обусловливают частное применение подобных критериев, т.к. зачастую преувеличивается значение каких-либо отдельных свойств жидкости или кристалла для процесса стеклообразования без сколько-нибудь серьезного теоретического подтверждения со стороны кинетической теории стеклообразования. Тем не менее, полуэмпирический подход для предсказания стеклообразования для систем, информация о свойствах которых недостаточна для строгого использования кинетической теории, зачастую бывает полезным.
Структура кристаллических и стеклообразных тел.
На сегодняшний день нет сомнений в том, что кристаллическое состояние вещества исследовано намного лучше, несравненно больше и несравненно точнее, чем стеклообразное. Поэтому при описании особенностей строения стекол целесообразно проводить аналогии с особенностями строения кристаллов. Во всех без исключения случаях вещество в кристаллическом состоянии построено гораздо проще, чем вещество в стеклообразном состоянии. И во всех случаях структурных исследований стекол прямо или косвенно используются знания о строении кристаллов.
Основная особенность строения кристаллов заключается в том, что некоторое число атомов (ионов или молекул) образует элементарную ячейку. В идеальном случае, зная особенности строения этой ячейки и закон перемещения ее в пространстве (трансляции) можно описать строение всего кристалла в целом, каким бы большим этот кристалл ни был. Такое пространственное повторение перемещения элементарной ячейки носит название дальний порядок. Следовательно, для описания идеального кристалла надо только определить, какие атомы и как распределены в элементарной ячейке. Однако для этого требуется очень сложный эксперимент и достаточно сложные расчеты. В настоящее время возможно выяснить точное положение атомов в элементарных ячейках, содержащих несколько десятков, а то и сотен атомов. Для решения этой задачи пользуются рентгеноструктурным анализом. На вращающийся кристалл падает узкий рентгеновский луч заданной длины волны, который рассеивается только в фиксированных направлениях со строго определенной интенсивностью. И то, и другое вытекает из известных условий Лауэ, связывающих между собой длину волны, параметры кристалла и направления рассеяния. Полученные таким образом экспериментальные данные по направлению рассеяния лучей, их интенсивности и соотношения между этими интенсивностями, после компьютерной обработки позволяют построить искомую структуру элементарной ячейки с точностью по положению атомов до десятитысячных долей ангстрема.
Если исследуется не один кристалл вещества, а поликристаллический образец, состоящий из большого числа очень мелких кристалликов, беспорядочно ориентированных в пространстве, то первичный падающий луч будет рассеиваться, образуя конусы, вдетые друг в друга. Определение их интенсивностей проводится по линии их центров, и результат изображается на рисунках в виде вертикальных линий, высота которых пропорциональна интенсивности, а положение определяет угол рассеяния (рис.10).

Рис.10. Рентгенограммы (дебаеграммы) метасиликата натрия в различных агрегатных состояниях: а – поликристалл, б – смесь мелких кристалликов, в – стекло.
Определение структуры элементарной ячейки по дебаеграмме возможно только для простейших кристаллов (рис.10 а).
В случае исследования структуры реального кристалла, возникает дополнительный ряд затруднений, связанных с наличием в его структуре различного рода дефектов (искажений решетки, пустот, включений, и т.п.), которые приводят к дополнительному рассеянию лучей вне направлений, вытекающих из условий Лауэ. При этом возникает еще более сложная задача – определить эти дефекты иногда по очень слабым и размытым рефлексам. Например, в поликристалле, состоящем из очень мелких кристалликов (менее 0.1 мкм), дебаевские линии на рентгенограмме будут расширяться (рис.10 б) и по их ширине можно вычислить размеры этих кристалликов.
Применение рентгеноструктурного анализа для выяснения строения аморфных веществ и, в частности, стекол оказывается более сложным, по сравнению с исследованием строения кристаллов. Ведь в какой-то степени стекло можно представить как некое подобие кристалла (кристаллитом), в котором заметно искажена каждая элементарная ячейка и где отсутствует дальний порядок. Неудивительно, что рентгенограммы стекол сильно отличаются даже от рентгенограмм поликристаллов (рис.10 в): вместо четких линий появляются широкие размытые полосы, частично перекрывающие друг друга. При этом расчеты количества элементарных ячеек в подобной сильно искаженной кристаллоподобной структуре по ширине размытых полос приводят к отрицательному выводу: кристаллиты должны содержать 1 -2 элементарные сильно искаженные ячейки и тем самым теряется смысл самого понятия «кристаллит».
Однако к размытой рентгенограмме (рис.10 в) можно подходить совсем иначе. Применяя к кривой интенсивности (которая характеризует распределение интенсивности вдоль любого радиального направления) строгую математическую обработку (анализ Фурье) можно преобразовать кривую интенсивности в кривую радиального распределения в стекле атомной плотности вокруг любого, принятого за начальный, атома в стекле. Такая кривая для кварцевого стекла показана на рис.11.

Рис.11. Кривая радиального распределения для кварцевого стекла.
А – измеренная кривая. Рассчитанные из кривой А вклады от отдельных пар атомов: B (Si-O); C (O-O); D (Si-Si); E (Si-O-второй кислород); F (O-O-второй кислород); G (Si-Si-второй кремний); r – расстояние от центра атома, принятого за начальный.
Функция радиального распределения атомов, которая служит для описания структуры аморфных и стеклообразных веществ, определяется следующим образом: произведение G(r)dr есть число атомов, находящихся в шаровом слое от r до r+dr. Объем шарового слоя равен произведению площади поверхности 4πr2 на толщину слоя dr. Поэтому можно записать следующее выражение
G(r)dr = 4πρ(r)r2dr,
где ρ– плотность вещества в данной точке, выраженная как число частиц на единицу объема (ρ зависит от расстояния). Функция радиального распределения атомов должна обладать следующими свойствами: шаровой симметрией, непрерывностью, независимостью от выбора центрального атома.
Функция радиального распределения атомов характеризует упорядоченность во взаимном расположении атомов. Например, для идеального газа характерно полное отсутствие какой-либо упорядоченности и его состояние характеризуется средней плотностью ρ. Поэтому для идеального газа функция G(r) представляет собой параболу. Если функция G(r) характеризуется какими-либо особенностями в виде максимумов и минимумов, то это свидетельствует о наличии некоторых преимущественных взаимных ориентаций атомов друг относительно друга, т.е. о существовании некоторой структуры.
Функция G(r) определяется из данных по рассеянию рентгеновских лучей под большими углами. Для рассеяния электромагнитного излучения при прохождении его через вещество имеет значение степень однородности этого вещества. Рассеяние не происходит в том случае, когда характерный размер неоднородностей (центров рассеяния) d много меньше длины волны падающего излучения d << λ. Если в качестве рассеивающих центров рассматриваются отдельные атомы, то неупорядоченное строение аморфного или стеклообразного вещества практически не отразится на прохождении через него светового излучения. В то же время, неупорядоченность во взаимном расположении атомов будет существенна для рентгеновских лучей, для которых d ≈ λ.
Возвращаясь к рис.11, следует отметить, что положение максимумов на этой кривой определяет (с точностью до 0.01Å) наиболее вероятные расстояния между атомами, а по величине площади под максимумами можно определить количество соседей вокруг атома, выбранного за начальный, т.е. его координационное число. Так, анализ первого, наиболее хорошо разрешенного максимума, свидетельствует о том, что в кварцевом стекле каждый атом кремния окружен четырьмя атомами кислорода в форме тетраэдра и этот тетраэдр, естественно, в самых различных пространственных положениях, воспроизводится по всему объему стекла. Таким образом, по первому максимуму кривой радиального распределения с высокой точностью можно определить первую координационную сферу, ближайшее окружение атомов, т.е. ближний порядок.
Второй максимум на кривой радиального распределения относится к расстоянию между атомами кислорода внутри тетраэдра. Третий максимум, частично перекрывающийся со вторым, более размыт: он определяет расстояние между двумя атомами кремния в соседних тетраэдрах. Анализ первого и третьего максимумов позволяет установить факт несимметричного расположения двух атомов кремния около атома кислорода. Угол между связями кислорода с этими двумя атомами кремния оказывается не постоянным и меняется в пределах от 130 до 160о при наиболее вероятном значении, близком к 144о. Диаметр области ближнего порядка в стеклообразном оксиде кремния лежит в пределах 15 – 20 Å, хотя границы этой области размыты, и, следовательно, неопределенны. Тем не менее, на основании кривой радиального распределения для этого стекла были рассчитаны не только расстояния внутри кремний-кислородного тетраэдра, но и еще пять наиболее вероятных межатомных расстояний в соседних тетраэдрах.
В современных исследованиях, в связи с повышением разрешающей способности используемых приборов, выявляется несколько большее число максимумов, чем это показано на рис.2. Но и в этом случае выявляется не более 9 – 12 пиков на радиальном расстоянии 9 – 10 Å. По мере удаления от центрального атома, эти пики размываются все больше и больше и их разрешение (разделение) и идентификация (т.е. отнесение к расстояниям между конкретными атомами) становится затруднительным. В этом случае приходится прибегать к моделям, для которых определяется «модельная» кривая радиального распределения, которая и сравнивается с экспериментальной кривой; после чего вводятся те или иные поправки, улучшающие совпадение теории и эксперимента. Следует отметить, что подобный подход хоть и имеет под собой почву, но не может претендовать на полную однозначность, т.к. всегда принципиально возможно применение совершенно отличных друг от друга моделей, приводящих к кривым радиального распределения, соответствующим экспериментальной.
Полученная экспериментально кривая радиального распределения является объективной характеристикой (своего рода паспортом) ближнего порядка структуры стекла. Любые структурные модели строения стекла, полученные с использованием каких-либо структурно-чувствительных методов, не могут считаться достоверными, если рассчитанные по ним кривые радиального распределения не соответствуют экспериментальным.
Подобная трактовка рентгенограмм стекол полностью соответствует модельным представлениям Захариасена, согласно которым атомы (или ионы) стекла образуют непрерывную неупорядоченную пространственную сетку. Проекция на плоскость подобной сетки стеклообразного оксида кремния представлена на рис.12 (б). Поскольку это двумерное изображение, каждый атом кремния окружен лишь тремя атомами кислорода, четвертый атом кислорода на схеме отсутствует. Понятно, что в реальном тетраэдре три (а на самом деле четыре) атома кислорода и атом кремния не лежат в одной плоскости и представленная проекция дает искаженную картину. Тем не менее, она правильно отражает основные идеи трехмерной пространственной сетки стекла, и ввиду своей наглядности получила в мировой стекольной литературе самое широкое распространение.
Рис.12. Схематическое изображение на плоскости строения кристаллического оксида кремния (а), стеклообразного оксида кремния (б) и натриевосиликатного стекла (в).
Как показали многочисленные рентгеновские и нейтронографические исследования, модель неупорядоченной пространственной сетки полностью подтверждается в отношении структур однокомпонентных стекол (стеклообразных оксидов кремния, бора, германия и некоторых других). Структура этих стекол характеризуется только ближним порядком и, как в случае любых других тел, тепловыми флуктуациями плотности, т.е. вызванными тепловыми колебаниями атомов локальными отклонениями плотности от средней по всему образцу.
Следует отметить, что тепловые флуктуации плотности рассеивают рентгеновские лучи под малыми углами с почти постоянной во всем интервале углов интенсивностью. Этот уровень интенсивности соответствует уровню, который можно оценить путем термодинамических расчетов. Ближний порядок (т.е. кривая радиального распределения), уровень тепловых колебаний плотности – это все сведения, которые можно получить о структуре однокомпонентных стекол. Эти характеристики изменяются с изменением температуры, давления, облучения быстрыми нейтронами и т.п., но при помощи рентгеноструктурного анализа изменение этих структурных параметров можно отслеживать с высокой точностью.
Структура стекол более сложного состава, например, содержащих оксиды щелочных металлов, значительно усложняется. Изменяется ближний порядок, что накладывает отпечаток на кривые радиального распределения: возникают дополнительные пики, соответствующие расстояниям между новыми типами атомов. При этом многоэлектронные атомы дают более резкие пики. Все это вносит дополнительные трудности в описании ближнего порядка такого рода стеклообразных систем.
Однако уже достаточно давно были предложены различные способы выяснения природы некоторых пиков на кривых радиального распределения, полученных для сложных стекол. К ним относятся изоструктурное (т.е. без заметного нарушения структуры) замещение легких атомов на более тяжелые (либо изменением состава стекла при синтезе, либо при помощи ионного обмена), использование различной рассеивающей способности атомов для рентгеновских и нейтронных лучей, использование аномального рассеяния рентгеновских лучей определенной длины волны отдельными атомами образца.
Для уточнения положения атомов в многокомпонентных стеклах чаще других используется способ изоструктурных замещений. В качестве индикаторов в стекла вместо легких атомов щелочных металлов вводится более тяжелое многоэлектронное серебро. При этом, размытые перегибы на кривой превращаются в резкие максимумы и по их положению оказывается возможным гораздо точнее определять расстояния не только в первой, но и в нескольких последующих координационных сферах.
Следует отметить, что в стеклах, содержащих два или более компонентов, наряду с тепловыми флуктуациями плотности неизбежно возникают тепловые флуктуации состава или тепловые флуктуации концентрации, в результате чего стекло становится химически неоднородным. Для таких сложных стекол гипотеза неупорядоченной сетки Захариасена становится несостоятельной, т.к. в этом случае для описания их общей структуры недостаточно знать только ближний порядок; необходимо определить их строение на расстояниях, значительно превышающих межатомные, т.е. за пределами кривой радиального распределения. Для этого исследуется субмикроскопическая структура стекла, т.е. не структурные образования в пределах 10Å, а образования от десятков до нескольких сотен и даже тысяч ангстрем. С этой целью применяются новые методы структурного анализа – а именно метод рассеяния рентгеновских лучей под малыми углами (РМУ) и метод рассеяния под средними углами (РСУ).
В результате применения всех перечисленных выше методов структурного анализа, в настоящее время сформулированы и приняты общие закономерности в расположении атомов, образующих стекло, т.е. фактически определено понятие «структура стекла». В зависимости от размеров структурного элемента по сравнению с размерами атома, можно определить структуру ближнего порядка, структуру среднего порядка и макроструктуру.
Как указывалось выше, под структурой ближнего порядка обычно понимают координационное число вокруг какого-либо центрального атома, длины связей, углы между связями в элементарном многограннике, т.е. ближний порядок в стекле описывает степень химической упорядоченности в пределах первой координационной сферы любого атома в составе стекла.
Средний порядок описывает структурные мотивы сочленения и взаимного расположения элементарных многогранников (цепи, ленты, трехмерные элементы, слои, кольца и т.д.), т.е. он отвечает за наличие некоторых закономерностей в упаковке элементарных полиэдров.
И, наконец, повторяемость элементов, образующих средний порядок, в какой-то мере может определять макроструктуру стекла. Следует отметить, что подобная повторяемость может быть и неполной, например, в неоднородных двухфазных стеклах.

Кривая радиального распределения для кварцевого стекла.
А – измеренная кривая. Рассчитанные из кривой А вклады от отдельных пар атомов: B (Si-O); C (O-O); D (Si-Si); E (Si-O-второй кислород); F (O-O-второй кислород); G (Si-Si-второй кремний); r – расстояние от центра атома, принятого за начальный.






