


A B C

D E
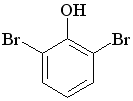
Для защиты аминогруппы проводят реакцию ацилирования амино фенола. Укажите продукт реакции.



А. В. С.


D. E.
11. При взаимодействии фенола с избытком концентрированной азотной кислоты образуется:

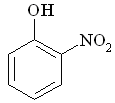
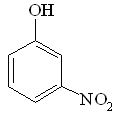
A B C


D E
Эталоны ответов:
1.D, 2.E, 3.D, 4.C, 5.В, 6.Е, 7.Е, 8.C, 9.B, 10.А, 11.D.
Тема № 14
АлифатическиЕ альдегидЫ и алифатическиЕ кетонЫ
АктуальнОсть темЫ
Альдегидами и кетонами называют производные углеводородов, которые содержат в своем составе карбонильную группу -С = О. Это большой класс органических соединений, они нашли свое применение в различных отраслях.
Формальдегид в больших количествах используют в производстве фенолоформальдегидных, мочевиноформальдегидным и других смол, необходимых в электропромышленности и машиностроении; он является исходным веществом в производстве синтетического каучука, красок, лекарственных веществ и др. 37-40% водный раствор формальдегида применяется под названием "формалин" как дезинфицирующее и дубильный средство, консервант для анатомических препаратов. Представитель алифатических кетонов - ацетон, хорошо известен как универсальный растворитель и как исходное вещество для синтеза многих органических соединений. Ацетон также используют в производстве искусственного шелка, кинопленки, лаков, лекарственных веществ, например, йодоформа.
Умение интерпретировать химическое строение и свойства алифатических альдегидов и кетонов необходимые студенту фармацевтического факультета для изучения таких дисциплин, как фармацевтическая химия, токсикологическая химия, фармакология, фармакогнозия. Они позволяют разрабатывать и совершенствовать новые методы синтеза лекарственных веществ.
ЦЕЛИ ОБУЧЕНЯ
Общая цель: Уметь определять химические свойства алифатических альдегидов и кетонов для использования в фармацевтической химии, фармацевтическом и токсикологическом анализе.
Конкретные цели
Уметь:
1. Интерпретировать электронное строение алифатических альдегидов и кетонов.
2. Составлять названия алифатических альдегидов и кетонов.
3. Выбирать способы добывания альдегидов и кетонов.
4. Интерпретировать химические свойства алифатических альдегидов и кетонов, составлять уравнения реакций.
СОДЕРЖАНИЕ ОБУЧЕНИЯ
Основные теоретические вопросы:
1. Классификация, номенклатура и изомерия алифатических альдегидов и кетонов;
2. Способы добывания алифатических альдегидов и кетонов;
3. Электронное строение алифатических альдегидов и кетонов. Реакционные центры в молекулах альдегидов и кетонов;
4. Физические и химические свойства алифатических альдегидов и кетонов:
-реакции нуклеофильного присоединения (АN);
-реакции присоединения - отщепления;
-реакции конденсации;
-реакции с участием a- углеродного атома;
-полимеризация альдегидов;
-окисления и восстановления;
5. Реакции идентификации алифатических альдегидов и кетонов. Значение в фармацевтической химии.
2. Основные термины и их определения
Альдегиды и кетоны называют производные углеводородов, содержащие в своем составе карбонильную группу> С = О. В альдегидах карбонильная группа связана с углеводородным радикалом и атомом водорода. Общая формула альдегидов R -СOH. В кетонах карбонильная группа связана с двумя углеводородными радикалами.
Тривиальные названия альдегидов происходят от названий кислот, в которые они превращаются при окислении. По замисниковий номенклатури ИЮПАК названия альдегидов образуют с помощью суффикса -аль. Нумерацию главного карбонового цепи начинают с атома углерода альдегидной группы.
Кетонную группу по заместительной номенклатуре означают суффиксом -он и цифрой обозначают атом углерода, входящего в кетогруппу.
Способы получения.
1. Реакция окисления спиртов. Первичные спирты окисляются до альдегидов, а вторичные - до кетонов.
2. Реакция гидратации алканов (реакция Кучерова). В условиях реакции Кучерова из ацетилена образуется уксусный альдегид, все гомологи ацетилена дают кетоны.
3. Реакция гидролиза дигалогеналканив. При гидролизе геминальних дигалогеналканив с атомами галогена у первичного атома углерода образуются альдегиды, а в вторичного - кетоны:
4. Реакция термического разложения солей карбоновых кислот. Со смешанной соли муравьиной и других карбоновых кислот при термичному разложении (пиролизе) получают альдегиды, а в других случаях образуются кетоны:
Насыщенные альдегиды и кетоны являются бесцветными жидкости со своеобразным запахом (формальдегид - газ с острым запахом). Карбонильные соединения имеют более низкие температуры кипения, чем соответствующие спирты, потому что не способны образовывать водородные связи. Кетоны являются хорошими растворителями. Высшие альдегиды имеют цветочный запах и широко применяются в парфюмерии.
Химические свойства альдегидов и кетонов определяются наличием в их молекуле карбонильной группы, которая является сильно полярной группой.
Атом углерода карбонильной группы находится в состоянии Sр2-гибридизации и связан с тремя атомами, расположенными в одной плоскости под углом 120 °. Атом кислорода, как более электроотрицательный элемент, притягуе к себе σ- и π-электроны. В результате этого двойная связь карбонильнои группы сильно поляризован. На атоме кислорода появляется частичный отрицательный заряд, а на атоме углерода - частичный положительный. Альдегиды, как правило, более реакционные, чем кетоны. Поскольку алкильные радикалы за счет + I-эффекта уменьшают положительный заряд на атоме углерода карбонильной группы, наличие в молекуле кетона двух алкильных групп приводит к большему снижению положительного заряда, чем в молекулы альдегида.
Реакции нуклеофильного присоединения:
1. Присоединение синильной кислоты. Синильная (цианидном) кислота присоединяется к карбонильных соединений, образуя циангидрины или гидроксинитрилы:
2. Присоединение натрия гидросульфита. Альдегиды и кетоны реагируют с гидросульфитом (бисульфитом) натрия, образуя бисульфитное соединения.
3. Присоединение воды. Растворение альдегидов в воде сопровождается образованием гидратов. Продукты реакции гидратации обычно неустойчивы и выделить их практически невозможно:
4. Присоединение спиртов. В спиртовом растворе альдегиды образуют полуацетали, а в присутствии следов минеральных кислот - ацетали:
Кетоны из-за высокой реакционной способности со спиртами не взаимодействуют.






