Могут принимать формы двух конформаций: кресла и ванны. Эти две формы постоянно переходят друг в друга в процессе свободного вращения вокруг оси С-С связи.

| 
| 
| 
| 
|
Форма кресла энергетически более выгодна (более симметрична), ее потенциальная энергия ниже на 5,6 ккал/моль потенциальной энергии ванны, поэтому последняя при обычных условиях почти не реализуется. Кресловидная конформация имеет плоскость симметрии, ось симметрии и центр симметрии (рисунок 1).
Направление С-Н связей в этих формах может быть двояким: 6 связей С-Н направлены от центра симметрии к его периферии под углом 109028/ к оси симметрии и называются экваториальными связями (е), 6 связей С-Н направлены параллельно оси симметрии и называются эквиальными (а).
Рисунок 1.
Атомы 2,4,6 лежат в нижней плоскости, атомы 1,3,5 – в верхней параллельной плоскости. Средняя между ними плоскость является плоскостью симметрии. Относительно этой плоскости заместители, расположенные у двух различных атомов углерода, могут занимать цис- или транс-положение. Геометрическая изомерия возможна при 1,2; 1,3; 1,4-положении заместителей.

1,2- и 1,3-дизамещенные циклогексана могут иметь и оптические изомеры, в то время как 1,4-изомеры являются оптически недеятельными, т.к. имеют плоскость симметрии, проходящую через 1 и 4 углеродные атомы.

Рисунок.
Изучение пространственного расположения заместителей проводится с помощью физико-химических методов анализа: рентгенографии, электронографии, спектрального анализа, определения дипольных моментов и др. Кроме того, сейчас накоплен большой материал, который позволяет делать выводы о пространственном строении циклических соединений в зависимости от химических свойств.
Изучая свойства соединений, можно делать выводы о конформации исследуемых молекул. Методика определения возможных и наиболее выгодных конформаций получила название конформационного анализа.
Способы получения
1. Действие активного металла на дигалоидные алкилы.
Используется, в основном, для получения трех- и четырехчленных циклов.
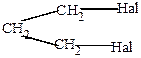
| +Zn (пыль)  ZnHal2 + ZnHal2 +
| 
|
Этот метод позволяет получать цикл, содержащий на 1 атом углерода больше, чем исходные соединения.
2.Сухая перегонка солей двухосновных карбоновых кислот.

| прокал
 - CaCO3
- CaCO3
| 
| 4H
 - H2O
- H2O
| 
|
| адипинат кальция | циклопентанон |
Руничка, используя соли тория, получил этим методом макроциклы до 40 атомов углерода в кольце.
3.Внутримолекулярная конденсация сложных эфиров двухосновных кислот (реакция Дикмана), например,

|

| 
| + НОН
 - С2H5OH
- С2H5OH
| |
| диэтиладипинат | ||||
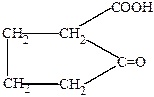
| t
 -CO2
-CO2
| 
| +4H
 -H2O
-H2O
| 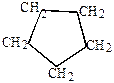
|
| кетокислота | циклопентанон | циклопентан |
4.Гидрирование ароматических углеводородов:

|
Pt
1000C
+ 3Н2 
 3000C
3000C
| 
|
5.Получение гомологов с боковыми ответвлениями с помощью реакции Вюрца.

|
+2Na + Br-CH3 
| 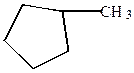
| +2NaBr |
Физические свойства
Циклизация углеродной цепи приводит к повышению Ткип, плотности и показателя преломления.
| Ткип, 0С | d420, г/см3 | nd20 | |
| Циклопентан | 49,00 | 0,740 | 1,4065 |
| Цис-2-пентен | 36,94 | 0,656 | 1,3700 |
| Пентан | 36,00 | 0,626 | 1,3577 |
Циклопропан и циклобутан – газы, следующие члены ряда – жидкости и твердые вещества. Растворимость в воде – ничтожна. В органических растворителях она несколько иная, чем у соединений открытого строения, например, в анилине циклопарафины растворяются лучше, чем парафины. Это используется в анализе углеводородных смесей (метод анилиновых точек).
Химические свойства
Зависят от величины цикла. Согласно теории Байера, устойчивость цикла тем меньше, чем больше отклонение валентного угла в цикле от тетраэдрического. В циклах с шестью и более атомами углерода угловое напряжение фактически отсутствует, почти нет его у циклопентана. Они ведут себя как предельные углеводороды. Соединения с трех- и четырехчленными циклами менее прочны. Напряженная С-С связь в таких циклах легко рвется, и они преимущественно дают реакции за счет разрушения кольца, приближаясь по свойствам к олефинам.






