Тургорное давление (лат. turgor — набухание)
— внутреннее давление, которое развивается в растительной клетке, когда в нее в результате осмоса входит вода и цитоплазма прижимается к клеточной стенке; это давление препятствует дальнейшему проникновению воды в клетку.
Еще одно свойство воды это плотность. Плотность величина не постоянная зависти от температуры. Когда тело нагреваем плотность падает, а когда охлаждаем падает. У воды аномальное свойство, у нее максимальная плотность при +4 С. Дальше, когда она начинает охлаждаться ее плотность начинает падать и лед легче воды.
Функции воды:
1. Универсальный растворитель. Среда для протекания всех биохимических реакций и физиологических процессов. Обменные процессы возможны только в растворах и больше никак.
2. Вода непосредственно участвует в химических реакциях как реагент. Как правило, эти реакции приводят к расщеплению или разрушению веществ.
В+H2O = B1 + В2
Ли́зис (от греч. λύσις) — растворение, разрушение клеток и их систем.
Такие реакции называются гидролизными (разрушение веществ при участии воды).
Структурно-строительная.
Вода составляет основу цитоплазмы каждой клетки. И основу жидких тканей, например, кровь (плазма на 90% состоит из воды).
4. Транспортная. Обеспечивает распределение в виде переноса веществ по организму и из клетки в клетку. Только в растворах все.
5. За счет процессов осмоса и тургора обеспечивает поддержание объема и формы клетки.
Участвует в терморегуляции.
У воды высокая теплоемкость (удержание температуры). Высокая теплопроводность (перераспределение тепла). Высокая теплота испарения (сброс тепла).
7. Участвует в процессах метаболизма (обмена веществ).
Минеральные соли:
Гидрофобные.
Гидрофобные минеральные соли нерастворимы в воде. В воде находятся в твердом состоянии. Твердые соли. Внутри живой клетки твердых солей быть не должно. Это патология. Они не могут выводиться. Кость - соли накапливаются в межклетниках.
Они обеспечиваю (входят в состав) опорных тканей.
Гидрофильные.
Они растворяются в воде. Распадаются (диссоциацируют на ионы).
Диссоциация на ионы в растворах происходит вследствие взаимодействия растворённого вещества с растворителем; по данным спектроскопических методов, это взаимодействие носит в значительной мере химический характер. Наряду с сольватирующей способностью молекул растворителя определённую роль в электролитической диссоциации играет также макроскопическое свойство растворителя — его диэлектрическая проницаемость
Ио́н (др.-греч. ἰόν — идущее) — одноатомная или многоатомная электрически заряженная частица, образующаяся в результате потери или присоединения атомом или молекулой одного или нескольких электронов.
Ионы заряженные частицы которые либо потеряли электрон, либо приобрели.
Ионы делятся на 2 группы:
1) Катионы
Катио́н — положительно заряженный ион. (потерял электрон)
Нас интересует особая группа катионов, которые нам нужна: K+ Na+ Ca2+ Mg2+
2) Анионы
Анио́н — отрицательно заряженный ион. (приобрел электрон) Cl -.
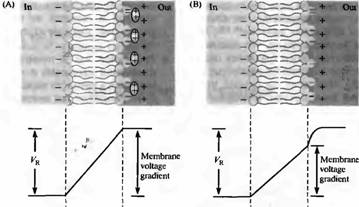
Ввиду того что мембрана клетки полупроницаема концентрация ионов внутри и снаружи клетки разная. Внутри огромное количество ионов калия, но по сравнению снаружи разница концентрации в 40 раз больше. Все остальные ионы преобладают снаружи. Внутри клетки постоянно синтезируются органические вещества и среди них очень много органических кислот. Эти кислоты имеют отрицательный заряд (аминокислоты, жирные кислоты и т.д.).
| Цитоплазма K+ В 40 раз больше Органические кислоты имеющие «-» заряд |
| Межклеточная среда Na+ Ca2+ Mg2+ Cl- |
Для нас принципиально не то, что этих веществ разная концентрация, а то что они имеют разные заряды. Таким образом, на внутренней части мембраны заряд в основном скапливается отрицательный, а на внешней положительный. Эта разница зарядов создает разность потенциалов между внутренней и внешней поверхностью мембраны. Эта разность потенциалов получила название мембранный потенциал.
Мембранный потенциал – разность потенциалов между внутренней и внешней поверхности мембраны, которая создается за счет разности зарядов. Разность зарядов создается за счет разности концентраций ионов внутри живой клетки.
В основе существования живой системы принцип не равновесия. Баланс ионов.
Изменения состояния нервной клетки возникает в результате изменения мембранного потенциала. Откуда берется это изменение - ионы начинают, перемещается через мембрану. Для этого нужен специальный механизм, который начнет их пропускать.
Органические вещества
Органические вещества — класс химических соединений, в состав которых входит углерод (за исключением карбидов, угольной кислоты, карбонатов, оксидов углерода и цианидов)
Биополимеры - это длинные цепи, которые образованы мелкими органическими молекулами мономерами.
Биополиме́ры — класс полимеров, встречающихся в природе в естественном виде, входящие в состав живых организмов: белки, нуклеиновые кислоты, полисахариды, лигнин. Биополимеры состоят из одинаковых (или разных) звеньев — мономеров. Мономеры белков — аминокислоты, нуклеиновых кислот — нуклеотиды, в полисахаридах — моносахариды.
Выделяют два типа биополимеров — регулярные (некоторые полисахариды) и нерегулярные (белки, нуклеиновые кислоты, некоторые полисахариды).
G YjiGZFiGZniGaJiGariGbNiGbviGcBiHcjiHdMg0XFiHeJiHejgGIQAAO1BLAQItABQABgAIAAAA IQA46GDHCQEAABMCAAATAAAAAAAAAAAAAAAAAAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0A FAAGAAgAAAAhADj9If/WAAAAlAEAAAsAAAAAAAAAAAAAAAAAOgEAAF9yZWxzLy5yZWxzUEsBAi0A FAAGAAgAAAAhADAIYBs3BQAAwQwAAA4AAAAAAAAAAAAAAAAAOQIAAGRycy9lMm9Eb2MueG1sUEsB Ai0AFAAGAAgAAAAhALXvoH65AAAAIQEAABkAAAAAAAAAAAAAAAAAnAcAAGRycy9fcmVscy9lMm9E b2MueG1sLnJlbHNQSwECLQAUAAYACAAAACEAwXBSpt8AAAAIAQAADwAAAAAAAAAAAAAAAACMCAAA ZHJzL2Rvd25yZXYueG1sUEsBAi0ACgAAAAAAAAAhAMBxkrhCYwAAQmMAABQAAAAAAAAAAAAAAAAA mAkAAGRycy9tZWRpYS9pbWFnZTEuZ2lmUEsFBgAAAAAGAAYAfAEAAAxtAAAAAA== "> 
| Мономер |
Важнейшим биополимерами составляющими основу жизни являются белки и нуклеиновые кислоты.
Группы органических веществ.
Углеводы
Это органические вещества, которые состоят из 3-ех атомов: углерода, кислорода и водорода. Для большинства из них, не зависимо от того как они будут выглядеть общая формула записывается как Cn(H2O)m. В среднем в клетках они составляют от 1 до 5% массы сухого вещества.
Есть клетки где углеводы составляют до 90% массы сухого вещества, это там где они запасаются, например, в картофеле крахмал. Углеводы разделяются на группы в зависимости от своего строения:
a) моносахариды (глюкоза, сахароза, уксусная кислота):
глюкоза (виноградный сахар) – основной источник энергии клетки.
b) дисахариды ( частный случай олигосахаридов ):
димерные молекулы - их молекулы состоят из 2-ух моносахаридов.
Пример: сахароза (тросниковый или свекольный сахар), состоит из двух молекул фруктозы + глюкозы;
Лактоза – молочный сахар (основной источник энергии для детенышей)
Эти первые две группы гидрофильные их растворы имеют сладкий вкус отсюда название сахара.
c) полисахариды -длинные ветвящиеся и неветвящиеся цепи.
Чем больше моносахаридов они содержат, тем менее они растворимы в воде. Примером служит крахмал, его аналог гликоген, целлюлоза или клетчатка. Это все полимеры глюкозы.
Функции углеводов:
Энергетическая.
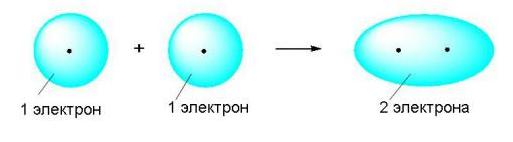 Что бы соединить два атома углерода в одну молекулу их нужно сблизить. Два электрона начинают отталкиваться, что бы их заставить изменить свою орбиту нам нужно потратить энергию. В итоге образуется ковалентная связь.
Что бы соединить два атома углерода в одну молекулу их нужно сблизить. Два электрона начинают отталкиваться, что бы их заставить изменить свою орбиту нам нужно потратить энергию. В итоге образуется ковалентная связь.
Химическая энергия ковалентной связи.
Когда мы ее разрываем, электроны возвращаются на свои места. Они нам эту энергию и отдают.
О
При расщеплении одного 1 грамма глюкозы высвобождается 17,6 кДж энергии.
2. Запасающая. Глюкоза как источник энергии запасается в виде крахмала у растений и в виде гликогена у животных и грибов. Место, где хранится гликоген это печень. Максимум что она может запасти это 300 грамм гликогена и еще скелетная мышца, там есть запас, который при необходимости от него можно отщеплять глюкозу и выбрасывать ее в кровь.
3. Структурно-строительная. Например, полисахарид целлюлоза образует клеточную стенку у растений. Хитин, хитиновый панцирь у членистоногих или клеточная стенка у грибов (поэтому мы не можем их нормально переваривать).
4. Защитная. Хитиновый панцирь защищает тело членистоногих. Или целлюлоза защищает клетку растения. Но есть полисахариды (в нашем организме) которые образуют слизистые секреты, т.к. они плохо растворяются в воде, то слизистая оболочка – это живые клетки, которые непосредственно соприкасаются с внешней средой (носовая полость, ротовая полость) и любая клетка сразу высыхает и погибает (должна быть покрыта влажным субстратом) если смачивать водой, то вода быстро испаряется. Слизистый секрет раствор полисахарида, который плохо испаряет воду.
5. Сигнальная (рецепторная). Полисахариды входят в состав рецепторов клеточных мембран (смотреть белки).
Липиды
В основе строения липидов спирты, которые соединяются с жирными кислотами. Жирные кислоты содержат очень много атомов углерода (более 15). Это тяжелые полимеры и они плохо растворяются в воде. Поэтому все липиды гидрофобные. Но они растворимы в неполярных растворителях, например, эфир, хлороформ, бензол. Это все у нас вызывает отравление организма и мутацию, т.к. разрушают наши клеточные мембраны.
В клетке липиды составляют 5 -15% массы сухого вещества. У нас есть стратегический запас в клетках подкожной жировой клетчатке жиров до 90%.
Группы липиды:
Стероиды.
a) Половые гормоны.
b) Кортикостероиды - гормоны стресса.
2. Воска. Покрываю листья у некоторых растений, кожу, перья, шерсть у некоторых животных (гидрофобные вещества).
3. Каротиноиды. Например, предшественники витамина А.
4. Нейтральные жиры. Триглицериды.
Соединение трехатомного спирта глицерина и жирных кислот, например, стеариновая кислота, пальмитиновая. Растительные жиры при комнатной температуре жидкие и называются масла, исключение кокосовое масло. Животные жиры при комнатной температуре твердые, исключение рыбий жир.
5. Фосфолипиды. Это органические вещества липиды, которые содержат остаток неорганической фосфорной кислоты. Эти молекулы уникальны.
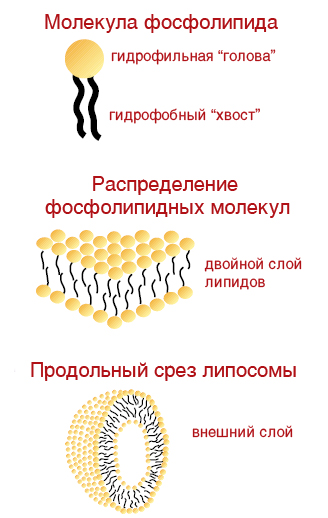
Голова содержит остаток фосфорной кислоты. Она полярная т.к. фосфорная кислота сбрасывает водород.
Неполярные хвосты жирных кислот.
Гидрофобные хвосты друг к другу притягиваются. Образуются билипидный слой.
- клеточная мембрана и основа всех оболочек нервных волокон.
Функции липидов:
1. Энергетическая. Жиры дополнительный источник энергии тогда, когда не хватает углеводов. При расщеплении 1 грамма жира высвобождается 38,9 кДж энергии.
2. Эндогенный (внутренний). Эндогенный источник воды в организме. Т.к. жир состоит из углерода, кислорода и водорода. Когда мы расщепляем жир, то выделяется много энергии и воды. При расщеплении 1кг жира образуется 1,1 литра воды.
3. Запасающая. Жиры накапливаются в тканях как источник энергии и как источник воды.
4. Защитная. Подкожная жировая клетчатка обеспечивает нам две защиты. Защита внутренних органов от механических повреждений и теплоизоляция.
Воск защита от смачиваемости (промокания).
5. Регуляторная. Гормоны. Жироподобные витамины: A, D, E, K. Они контролируют работу отдельных клеток, целых систем органов, а иногда и организма в целом (половое поведение).
6. Структурно-строительная. Фосфолипиды образуют основу всех биологических мембран и оболочек нервных волокон.
Липиды у все одинаковые, отличаются только количеством.
Белки.
Белки составляют от 50 до 80% сухой массы клетки. Это биополимеры, мономерами которых являются аминокислоты.
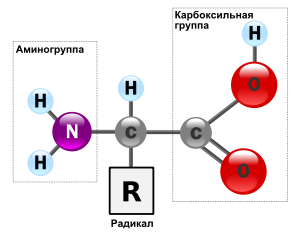
Все белки построены из азота. Радикалом может быть все что угодно, начиная от атомов кислорода и заканчивая гидроциклами сложными. На сегодняшний день известно 60 видов аминокислот. Все они отличаются только радикалом. Из этих 60 аминокислот 22 входят в состав всех живых организмов. Какой организм ни взять все его белки содержат 22 вида аминокислот не больше и не меньше. Белки отличаются только составом аминокислот.
Аминокислоты собираются в линейный биополимер, соединяясь ковалентной связью, образуют цепочку белка. Они соединяются друг с другом пептидной связью:

В среднем в молекуле белка от 300 до 500 аминокислотных остатков. Часто называют полипептидная цепь вместо молекулы белка. Если в цепочке от 2 до 17 аминокислот, то их называют пептиды, если больше то уже белок.
В структуре белковой молекулы выделяют 4 уровня организации:

Первичная структура: строго определенный порядок расположения аминокислот в полипептидной цепи. Для каждого белка он уникален. Именно он определяет все свойства и функции белка. Эта структура закодирована в генах.
Вторичная структура: самопроизвольное сворачивание цепочки аминокислот в правую спираль.
В виде такой спирали существуют некоторые белки, например, коллаген.
На этом уровне находятся фибриллярные (нитчатые) белки. Например, мышечные белки: актин, ниозин, фибриноген.
Третичная структура (глобулярная): Многократное сворачивание спирали в 3-ех мерное образование глобулу (комок). Форма глобулы для каждого белка строго определенная.
 Именно форма глобулы обеспечивает белком его определённых функций.
Именно форма глобулы обеспечивает белком его определённых функций.
Четвертичная структура: объединение нескольких белковых молекул (субъединиц) в одну систему. В качестве субъединиц могут быть спирали, глобулы. По своему составу субъединицы могут быть идентичными, а могут быть разными. Пример такого белка, гемоглобин.
Пространственной конфигурацией белка, начиная с вторичной структуры, называют конформацией. Белки подвижны (изменяются) под воздействием физических и химических воздействий. Изменяется, например, температура, кислотность, давление и конформациея белка начинает меняться. Такая способность к изменению лежит в основе свойства, которое называется пластичность белка. Пластичность белка лежит в основе пластичности клетки, лежит в основе пластичности нервной системы, а это лежит в основе нашей психики, нашего поведения, а все идет от пластичности белка.
Пластичность белка это способность белковой молекулы обратимо изменять конформациею под влиянием физических и химических факторов. Воздействие прекратилось и белок возвращается в исходное состояние. Бывают воздействия на клетку неадекватные, тогда под действием разных факторов белок начинает разрушаться, такой процесс называется денатурацией белка.
Денатурацией белка - разрушение структуры белка под влиянием вредящих физических и химических факторов.
В зависимости от того что произошло с белком денатурация бывает 2-ух видов:
обратимая и необратимая.
Обратимая денатурация – процесс, когда сохраняется первичная структура. В этом случае все остальные структуры белка самопроизвольно восстанавливаются (ренатурация).
Необратимая денатурация – ситуация в которой разрушается первичная структура. В этом случае восстановление остальных структур невозможно.
Работа белков:
Катализатор – это вещество в присутствии, которого реакция протекает намного быстрее, чем без него, но само оно в реакции не участвует.
Ферменты (энзимы) – биологические катализаторы, ускоряющие биохимические реакции в 1000 раз. Большинство ферментов являются белками, потому что есть ферменты нуклеиновые кислоты.
Субстрат – вещество, которое подвергается действию фермента.
Как функционирует фермент?


Конформация активного центра, распределение зарядов в нем может быть. Оно соответствует тому субстрату, на который будет действовать тот фермент, как замок к ключу. Субстрат и фермент взаимно дополняют друг друга. Если у фермента стоит отрицательный заряд, то у субстрата должен быть положительный.
Комплементарность – означает, что 2, 3, или более молекул пространственное дополняют друг друга (принцип пазла).
Катализ реакции осуществляет не вся молекула фермента, а только ее активный центр, который комплементарен конкретному субстрату.
Как работает фермент:
Фермент фиксируется в мембране, чтобы не болтаться в цитоплазме и он такая подвижная молекула, как чашечка его активный центр, то открывается, то закрывается. А мимо цитоплазмой гонятся все молекулы органических и неорганических веществ и каждая молекула тычется в этот активный центр. Как только пришедшая молекула комплементарна этому активному центру, то все это ее субстрат. Соответственно тут же субстрат фиксируется в активном центре фермента, а дальше фермент пластичен, он изменяет свою конформацию, а субстрат разрывается на два, произошла реакция расщепления. Как только субстрат был поделен, он был одной молекулой, а стал двумя, его конформация изменилась, он уже не может соединяться с активным центром, выбрасывается из активного центра. А раз на фермент ни чего не действует, то он возвращается в исходное состояние и ждет следующей молекулы. Одна молекула фермента может превращать 10 000 молекул субстрата в минуту.
Свойства ферментов:
1. Субстратная специфичность. Фермент узнает только определённую группу субстратов и катализирует их превращение.
2. Специфичность действия. Каждый фермент катализирует определенный тип реакции: синтез, расщепление, перенос, какой то группы.
3. Коферменты и витамины. Коферменты часть фермента, помощник фермента. Фермент без этого кусочка работать может, но реакция идет медленнее. Кофермент наш организм синтезировать не может.
Если мы ее не можем синтезировать, то для нас она является витамином. И мы ее едим.
Витамины пополняют функции коферментов. Без них в организме начинаются патологические изменения.
4. Все ферменты активны только в определенных физико-химических условиях, которые обеспечивают их поддержание нормальной конфирмаций. Для нас это температура от 36 до 37 С, pH средний = 7,2 – 7,4. В желудки нужна кислая среда.
5. Ферменты – это биологически или физиологические активные вещества. Это значит, что они в малых дозах обладают мощными эффектами. Например, одна молекула в минуту превращает до 10 000 субстратов.
Белки - рецепторы.
Рецептор – универсальный.
Это белки, которые встроены в мембрану клетки. Пронизывают ее насквозь. В той части, где они выступают наружу, есть небольшой участок, к нему прикрепляются усики полисахаридов. И эта часть называется активный центр.
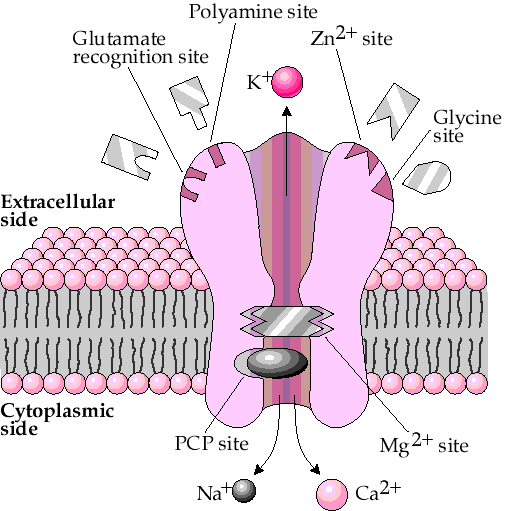 Функции белков:
Функции белков:
1. Структурно-строительная. Белки входят в состав всех клеточных структур, начиная от мембраны и заканчивая органоидами.
2. Каталитическая. Белки ферменты контролируют биохимические процессы в клетках.
3. Транспортная. Белки обеспечивают транспорт веществ через мембрану, а так же по организму в целом. Гемоглобин переносит кислород, например.
4. Двигательная. Белки мышечной ткани актин, миозин. Это сократительные белки. Именно за счет их скольжения друг относительно друга, мышцы сокращаются и именно через это сокращение обеспечивается движения многоклеточного организма, как движения тела, так и речь.

5. Защитная. Антитела крови. Защитные белки иммунной системы. Фибриноген. Активируются при повреждении стенок сосуда и приводят к формированию тромба.
Одного белка нахватает – гемофилия.
6. Сигнальная (рецепторная). Белки образуют рецепторы клеточных мембран и обеспечивают восприятие сигналов и ответ клетки на это.
7. Регуляторная. Функцию выполняют белковые гормоны, например белок инсулин.
8. Энергетическая. Белок не откладывается в запас. При расщеплении 1 грамма белка высвобождается 17,6 кДж энергии. Эту функцию использования белков в качестве энергии, белки начинают использовать только тогда, когда истощены запасы углеводов и жиров.
Если белки служат источником энергии это называется самоперевариванием. Иногда, на каком-то этапе расщепления белков процесс становится необратимым и в клетках запускается генно-клеточная смерть- это называется запрограммированная клеточная смерть (апоптоз). И организм погибает, даже если его начинают кормить. Процесс становится необратимым – это называется самоперевариванием.
9. Исключительная функция Запасающая. Запас белков в яйцеклетке (желток) для обеспечения начальных этапов развития зародыша, пока он сам еще не может синтезировать.
Нуклеиновые кислоты.
Нуклеус – ядро. Были обнаружены в ядре. Гигантский полимер, мономерами которого являются нуклеотиды.
Виды нуклеиновых кислот:
1. ДНК. Дезоксирибонуклеиновая кислота.


ДНК – носитель наследственной информации.
Наследственная информация – информация о свойствах и признаках каждой клетки и организма в целом, которая передается из поколения в поколение.
Функции ДНК:
1. Хранение наследственной информации. Единица хранения наследственной информации это ген. Ген – участок молекулы ДНК. Гены бывают двух видов:
a) Структурные. Это гены, которые кодируют первичную структуру полимерных молекул (белка или РНК). Из всех 46 молекул структурные гены составляют не более 20% всех ДНК. Все остальное это не информативные участки. Их составляют регуляторные гены.
b) Регуляторные. Регуляторные гены это не кодирующие участки, которые регулируют активность (экспрессию) структурных генов.
2. Реализация наследственной информации через синтез белка. Синтезированный белок начинает выполнять свою функцию. И тогда появляется свойства или признак клетки или организма.
3. Передача наследственной информации дочерним клеткам при делении. В основе такого механизма уникальная способность молекулы ДНК к самоудвоению (Доклад).
РНК.
Существуют три вида РНК. Все они представляют функциональную систему, которая обеспечивает реализацию наследственной информации через процесс синтеза белка. Они обеспечивают синтез белка. Определенный участок ДНК является структурным геном. В этом гене хранится информация первичное строение белка. Первое, что нужно сделать - это снять копию с этого гена (участка ДНК) и перенести туда, где эта структура будет собираться. Первый вид РНК, называется информационное РНК.
a) Информационное РНК (иРНК). Это копия структурного гена. Дальше она будет перемещаться в цитоплазму. Т.к. белок построен из аминокислот, то эти аминокислоты нужно куда-то подносить, к месту синтеза белка. Отсюда второй вид РНК это транспортное РНК.
b) Транспортное РНК (тРНК). Она обеспечивает транспорт аминокислот к месту синтеза белка. Осталось соединить два этих видов РНК, чтобы точно правильно собрать эти аминокислоты и не ошибиться. Для этого существует место которое называется рибосома. Это маленькое тельце состоящие из белков.
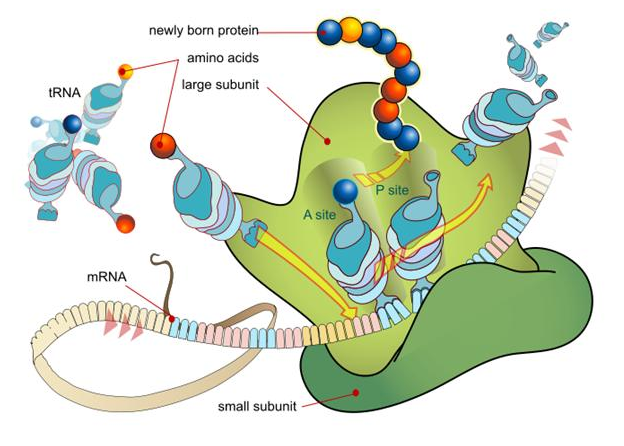
Рибосома представляет собой две субъединицы, между которыми зажимается иРНК. В месте, где зажата иРНК подходят тРНК. Эти тРНК несут аминокислоты. В этом месте эти аминокислоты будут соединять аминокислоты, и синтезировать белок. Пространственную организацию рибосомы (сборки белка) определяет рРНК, чтобы процесс сборки белка происходил правильно и ни одна тРНК в своих действиях не ошиблась.
Итак, первый вид:
Информационная иРНК, иначе матричная (мРНК) – это копия структурного гена ДНК которая переносит информацию о строении белка от ДНК, т.е. из ядра к месту синтеза белка (рибосоме). Она служит матрицей, по которой собирают белок.
Второй вид РНК, транспортный РНК, они транспортируют аминокислоты к месту синтеза белка (рибосоме) и непосредственно участвуют в этой сборке.
c) Третий вид это рибосомная рРНК. Она формирует рибосому и таким образом обеспечивает правильное пространственное взаиморасположение информационной и транспортной РНК в рибосоме.
АТФ
Аденозинтрифосфат – Аденозинтрифосфорная кислота.
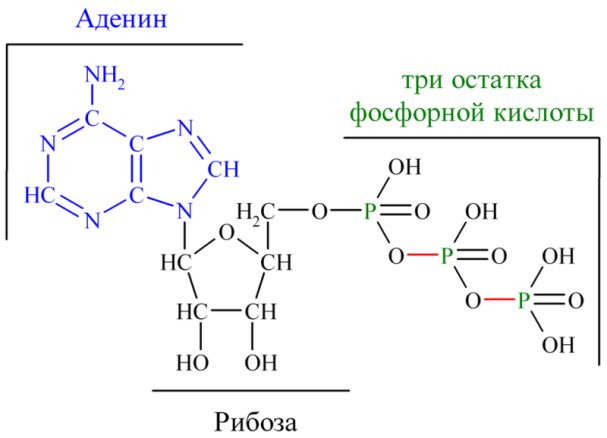
Макроэргические связи — это ковалентные связи, которые гидролизуются с выделением значительного количества энергии: 30 кДж/моль и более (свободная энергия гидролиза).
Ковалентная связь
|
Аденозин –---------------------------Фн~Фн~Фн
| | |
АМФ -- АденозинМоноФосфат -| | |
АДФ -- АденозинДиФосфат ---------| |
АТФ -- АденозинТриФосфат ------------|
Уникальное соединение. Способ аккумуляции энергии всех обитателей нашей планеты.
АТФ – универсальный аккумулятор и транспортёр энергии в клетке. Клетка получает из него энергию путем гидролиза. Фермент, который катализирует эту реакцию называется АТФаза.
АТФ + H2O -> АДФ + Фн + Е
АДФ + H2O -> АМФ + Фн + Е
Растения получают энергию виде солнечного света и преобразуют ее в АТФ.
Мы получаем белки, жирки, углеводы расщепляем их и запасаем в АТФ и только потом используем в клетке. Отсюда потери энергии. При расщеплении мы 45% энергии рассеиваем виде тепла и только 55% запасаем в АТФ. Температура нашего тела это побочный продукт синтеза АТФ.
Строение клетки

Клетка
Структуры:
1. Клеточная (цитоплазматическая) мембрана. Плазмалемма. Это то что отделяет клетку от окружения.
2. Ядро. ДНК должна быть защищена и вокруг нее выстраивается целая структура.
В этом ядре есть
- хроматин (нити ДНК); Когда ДНК стерилизуется, упаковывается, получается хромосом.
- ядрышки;
- ядерный сок (кариоплазма);
- ядерная оболочка, которая все это отделяет от цитоплазмы.
3. Цитоплазма и ее органоиды (ядро не является органоидом цитоплазмы).
A) Гиалоплазма;
b) Органоиды – это отдельные участки цитоплазмы, которые имеют определенное строение и выполняют определенные функции; Органоиды делятся на 2-ве группы:
1. Мембранные органоиды. Их стенки образованны элементарными мембранами похожими на клеточную мембрану. К мембранным органоидам относятся:
· Эндоплазматическая сеть (ЭПС);
· Комплекс Гольджи;
· Лизосомы
· Митохондрии;
2. Не мембранные органоиды. В основном они состоят из белков. К ним относятся:
· Рибосомы;
· Цитоскелет;
· Клеточный центр;
· Клеточные ключи;
· Центриоль
Клеточная мембрана (Плазмалемма):
Клеточная мембрана состои 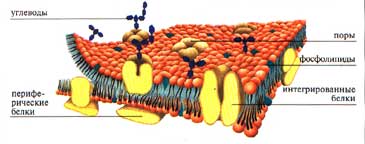 т из:
т из:
1. Билипидного слоя из фосфолипидов.
Толщина билипидного 7,5 нм
2. Белков из 3 групп:
a) Периферические белки.
П. б. удерживаются за счет электростатических сил притяжения от полярных фосфолипидов.
Функция: Структурная.
b)  Полуинтегральные белки. Удерживаются за счет взаимодействия с гидрофобными хвостами, т.к. тоже имеют гидрофобные части.
Полуинтегральные белки. Удерживаются за счет взаимодействия с гидрофобными хвостами, т.к. тоже имеют гидрофобные части.
Функции:
1. Эти белки могут быть ферментами.
Фиксируются в мембране в определенном порядке для конверсии субстрата.
2. Транспортная. Челночный транспорт. У данного белка будет активный центр, который комплементарен, например, иону Na или K, Ca или молекулы Глюкозы, тогда белок захватывает на одной стороне мембраны это вещество протаскивает его сквозь билипидный слой и выбрасывает на другой стороне. Возвращается назад пустой, либо с другим веществом. Ходит туда-сюда как челнок по мембране.
c) Интегральный белок. Выполняют три разных видов функций:
1. Транспортная функция. Канальный транспорт. Белок имеет такую конформацию, что внутри него имеется канал. Через этот канал свободно перемещаются (диффундируют) по закону осмоса, те или иные вещества. Канал может быть постоянно открыт тогда его называют постоянно открытый канал или пора. Либо может быть закрыт тогда для его открытия нужны определенные условия.
2. Эти белки могут быть частью ферментной системы (выполняют ферментативную функцию).
Рецепторная.
Мембранный транспорт.
Свойство мембраны – способность избирательно пропускать в клетку и из нее определенные вещества. Транспорт мембраны бывает 2 видов:
1. Пассивный транспорт. Не требует затрат энергии и протекает по законам осмоса. Вещества сами протекают их требуется только пропустить. Существует 2 вида пассивного транспорта: через поры (открытые каналы) или каналы, которые постоянно открыты диффундирует вода и некоторые ионы минеральных солей (полярные вещества).
Непосредственно сквозь билипидный слой перемещаются гидрофобные, жироподобные вещества, например, жирные кислоты или жироподобные витамины.
2. Активный вид транспорта. Требует затрат энергии и не зависит от концентрации веществ (для закона осмоса).
a) При помощи транспортных белков мембраны. Таким путем могут перемещаться небольшие (низкомолекулярные вещества), например, ионы, мономеры разных органических веществ, аминокислоты, моносахариды, другие органические кислоты.
В зависимости от того какие белки этот транспорт осуществляют он может быть:
1. Челночным. Обеспечивают полуинтегральные белки.
2. Канальным. Обеспечивают интегральные белки.
b) При помощи мембранных структур. Транспортируются крупные частицы, либо порции веществ.
1. Эндоцитоз. Захват клеткой частиц из внешней среды. Частицы фиксируются на поверхности мембраны (существует комплиментарность). Мембрана образует выпячивание вокруг этой частицы, начинает ее охватывать.

Различают: фагоцитоз – поглощение твердых частиц и
пиноцитоз – поглощение капель жидкости с растворенными веществами.
2. Экзоцитоз. Выведение из клетки порций продуктов метаболизма. Пример, выброс медиаторов нейроном, железы выбрасывают гармоны.

Функции клеточной мембраны:






