Всасывание лекарства в организм в значительной степени зависит от аккуратности больного при выполнении назначений. Если больной дисциплинирован, то причиной низких концентраций лекарства в крови может быть нарушение всасывания в тонкой кишке.
Клиренс может меняться, когда у больного имеются серьезные нарушения функции почек, печени или сердца.
Хорошим индикатором нарушения функции ночек является клиренс креатинина. Для лекарств, выводимых почками, требуются поправки на клиренс, учитывающие функциональное состояние почек.
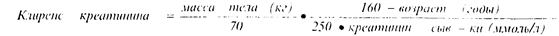
Для женщин значение клиренса уменьшается на 10% вычисленного по формуле, т.к. у них меньше мышечная масса, определяющая продукцию креатинина. У тучных больных для расчета следует использовать идеальную массу тела (см. ниже), у тяжело больных - вносить поправку на атрофию мышц.
Заболевания печени могут снижать клиренс и удлинять период полувыведения лекарств, элиминируемых печенью.
Снижение скорости системного кровотока при недостаточности кровообращения приводит к уменьшению клиренса как за счет печеночного застоя, так и за счет снижения клубочковой фильтрации.
На величину концентрации лекарств влияет не только клиренс, но и степень связывания с белками. Снижение уровня альбуминов плазмы при нефротическом синдроме, циррозах, кахексии ведет к уменьшению общей концентрации лекарств (фенитоин, салицилаты, дизопирамид) в плазме. Концентрация лекарств, связывающихся с альфа1-кислым гликопротеином (хинидин, лидокаин и пропраполол), уровень которого резко возрастает при острых воспалительных заболеваниях, может значительно увеличиваться.
Объем распределения меняется параллельно величине связывания лекарства тканями.
У равномерно распределяющихся лекарств (теофиллин), Vd близок к общему содержанию жидкости в организме, поэтому поправка на объем пропорциональна массе тела. Так, если пациент весит 90 кг, а Vd теофнллина (35 л) дан для массы 70 кг, корригированный объем распределения составит (35 л* 90кг/70 кг) 45 л.
Для лекарств, плохо проникающих в жировую ткань (дигоксин, аминогликозиды) у тучных больных при расчете поправки используется не истинная, а идеальная для данного роста масса тела, равная: для мужчин 48+1,1 кг, а для женщин 45+0,9 кг на каждый см роста выше 152 см.
У больных с отеками, асцитом, гидротораксом значения объема распределения для аминогликозидных антибиотиков (гентамнцин, тобрамицин) рассчитывают, прибавляя к обычной массе тела объем избыточной жидкости.
Метаболизм лекарств
Организм обладает мощной системой удаления (элиминации) чужеродных веществ (ксенобиотиков), попавших в его внутреннюю среду. К их числу относятся и лекарства.
В неизменном виде с мочой экскретируется лишь малая часть препаратов, для этого необходима высокая гидрофильность (растворимость в воде) или матый размер молекул. Большинство же лекарств липофильны (жирорастворимы) и, как правило, сильно связаны с белком, поэтому плохо фильтруются почками. Для того, чтобы вывести эти вещества, необходимо сделать их более водорастворимыми в результате химических превращений -метаболизма. В процессе биотрансформации лекарств участвуют многие из тех ферментов, которые используются в синтезе эндогенных соединений (стероидные гормоны, холестерин, желчные кислоты) или экскреции эндогенных метаболитов (билирубин).
Протекающие в ходе метаболических превращений реакции могут быть разделены на две фазы биотрансформации.
В фазе I исходное вещество превращается в более полярный метаболит путем введения или раскрытия функциональной группы –ОН, -NH или -SH (реакции окисления, восстановления, гидролиза). Если при этом метаболит приобретает достаточную гидрофильность, то легко экскретируется почками. Если нет - подвергается последующей трансформации (II фаза) с помощью реакций соединения (конъюгации) с эндогенными глюкуроновой, серной, уксусной кислотами или аминокислотами. Эти реакции приводят к образованию высокорастворимых соединений, которые легко элиминируются. Большинство лекарств проходят обе фазы биотрансформации последовательно, однако возможна и обратная последовательность превращений.
Продукты метаболизма часто фармакологически неактивны или менее активны, нежели исходное лекарство, однако могут иметь и более высокую активность, а подчас - даже вызывать токсические эффекты. Некоторые инертные вещества (пролекарства) в процессе метаболизма превращаются в высокоактивные дериваты, обеспечивающие собственно фармакологическое действие.
Главным органом метаболизма является печень, однако ряд лекарств более интенсивно метаболизируются в кишечнике (хлорпромазин, клоназепам). Определенную роль в элиминации играют легкие, кожа, почки.
Хотя биотрансформация лекарств может осуществляться путем спонтанных некатализируемых реакций, в большинстве случаев в роли катализатора выступают специфические клеточные белки - ферменты. Многие из них располагаются на липофильных мембранах эндонлазматического ретикулума печени и других тканей. При гомогенизации и фракционировании клетки эти мембраны приобретают вид везикул, названных микросомами.
В микросомальной фракции локализованы ферменты-монооксидазы, катализирующие реакции окисления (I фаза). На каждую молекулу субстрата (лекарства) расходуется молекула кислорода, один атом из которой соединяется с субстратом, другой - с водородом. Для реакции необходимо присутствие ферментов: цитохрома Р-450, цитохром Р-450 редуктазы, а также восстанавливающего агента (НАДФ*Н) и молекулярного кислорода. Субстратная специфичность цитохрома Р-450 низка, поэтому он может взаимодействовать с широким кругом липофильных соединений - лекарств.
Некоторые вещества при повторном введении могут повышать активность цнтохрома Р-450 путем увеличения скорости синтеза или замедления разрушения. Этот феномен, получивший название индукции, чаше приводит к ослаблению лечебного действия, но, если метаболиты активнее исходного лекарства, индукция может вызывать токсические эффекты. Способностью к индукции обладают барбитураты, рифампицин, противосудорожные средства и др.
Некоторые лекарства обладают способностью ингибировать активность ферментов группы цитохрома Р-450 действием, противоположным индукции. Ингибированне цитохрома Р-450 приводит к замедлению метаболизма совместно вводимых лекарств и некоторых эндогенных веществ (тестостеропа), что чаще приводит к усилению их действия. Хотя результат может быть и обратным, если препарат представляет собой пролекарство. К числу ингибиторов микросомальной системы печени можно отнести некоторые антисекреторные средства (циметидин, омепразол), ряд антибиотиков и химиопренаратов, этанол.
Феномены индукции и ингибирования цитохрома Р-450 объясняют некоторые важные механизмы взаимодействия лекарств.
Конечным этапом метаболизма многих лекарств является их конъюгация с эндогенными соединениями (II фаза). Она осуществляется с помощью ферментов-трансфераз, локализованных в микросомах или в цитозоле гепатоцитов. В качестве эндогенных субстанций могут выступать УДФ-глюкуроновая кислота, ацетил-КоА, глутатиои, S-аденозилметионин и др. Подавляющее большинство конъюгатов неактивны, однако некоторые из них могут быть токсичными, например: ацилглюкурониды неспецифических противовоспалительных средств или N-ацетилат изониазида.
Важную роль в регуляции процессов конъюгации играет питание, обеспечивающее поступление эндогенных участников реакции. При недостаточности процессов конъюгации в крови могут накапливаться токсичные продукты I фазы метаболизма. Типичным примером такой ситуации может быть метаболизм некоторых канцерогенов, когда в результате самоиндукции ускоряется их окисление, а конъюгация относительно запаздывает. Этому способствует дефицит эндогенного участника конъюгации - глутатиона. Накапливающиеся в крови продукты окисления (эпоксиды) оказывают токсическое действие.
Метаболизм некоторых лекарств существенно изменяется при заболеваниях печени. Эти лекарства даже в обычных дозах могут вызвать интоксикацию у пациента с тяжелым поражением печени. При нарушении печеночного кровотока (портальная гипертензия, недостаточность кровообращения) значительно замедляется метаболизм лекарств, клиренс которых определяется интенсивностью кровотока через печень. Выраженность этих изменений трудно предвидеть и оценить количественно.
ОСНОВНЫЕ ПРИНЦИПЫ МЕДИКАМЕНТОЗНОГО ЛЕЧЕНИЯ






