Большинство веществ могут существовать в одном из трех агрегатных состояний: газообразном (парообразном), жидком и твердом. В определенных условиях эти фазы способны переходить друг в друга, то есть всякую жидкость путем испарения можно перевести в газ, а охлаждением – в твердое состояние. На рис. 6.9 показаны взаимные фазовые превращения вещества.
Рисунок 6.9Взаимное превращение трех агрегатных состояний друг в друга
Равновесия между различными фазами одной системы называют фазовыми, а описывают эти фазовые равновесия посредством фазовых диаграмм или диаграмм состояния. Фазовая диаграмма позволяет установить условия равновесия между числом фаз, числом компонентов и числом степеней свободы (вариантностью) системы.
Фаза (Ф) – гомогенная (однородная по химическому составу и термодинамическим свойствам) часть системы, отделенная от других частей поверхностью раздела. Так, два нерастворимых друг в друге твердых вещества, как и две несмешивающиеся жидкости, образуют две фазы.
Компоненты (К) – химически индивидуальные вещества, наименьшее число которых достаточно для образования фаз системы.
Число компонентов определяется количеством индивидуальных веществ в системе за вычетом числа возможных между ними обратимых взаимодействий. Например, система из трех индивидуальных веществ H2O, H2, O2 будет двухкомпонентной, поскольку для образования всех фаз достаточно любых двух веществ: = H2 + 1/2O2.
По числу компонентов системы делятся на одно-, двух-, трех- и многокомпонентные.
Степени свободы (С) – число параметров (температура, давление, состав системы), которые можно произвольно менять без изменения числа фаз в системе.
Правило фаз Гиббса: в изолированной равновесной системе число степеней свободы равно числу компонентов системы плюс два минус число фаз: С = К + 2 – Ф
В качестве примера однокомпонентной системы, для которой правило фаз С = 3 – Ф, на рис. 6.10 приведена фазовая диаграмма диоксида углерода.
Рисунок 6.10Фазовая диаграмма CO2
При P < 5,3 атм. CO2 в жидком состоянии не может находится. При атмосферном давлении твердый диоксид углерода сублимирует при 195 K.
Если один из параметров системы (температура или давление) имеет постоянное значение, то правило фаз принимает вид: C = K + 1 – Ф.
Это уравнение используется при изучении конденсированных систем, состоящих только из твердых и жидких фаз, поскольку состояния равновесия в таких системах малочувствительны к изменению давления.
Наибольшее практическое значение имеют только изобарные диаграммы двухкомпонентных систем, содержащие только конденсированные фазы. Рассмотрим некоторые из них.
Пове́рхностно-акти́вные вещества́ (ПАВ) — химические соединения, которые, концентрируясь на поверхности раздела фаз, вызывают снижение поверхностного натяжения.
Основной количественной характеристикой ПАВ является поверхностная активность — способность вещества снижать поверхностное натяжение на границе раздела фаз — это производная поверхностного натяжения по концентрации ПАВ при стремлении С к нулю. Однако, ПАВ имеет предел растворимости (так называемую критическую концентрацию мицеллообразования или ККМ), с достижением которого при добавлении ПАВ в раствор концентрация на границе раздела фаз остается постоянной, но в то же время происходит самоорганизация молекул ПАВ в объёмном растворе (мицеллообразование или агрегация). В результате такой агрегации образуются так называемые мицеллы. Отличительным признаком мицеллообразования служит помутнение раствора ПАВ. Водные растворы ПАВ, при мицеллообразовании также приобретают голубоватый оттенок (студенистый оттенок) за счёт преломления света мицеллами.
Методы определения ККМ:
Метод поверхностного натяжения
Метод измерения контактного угла с тв. или жидкой поверхностью (Contact angle)
Метод вращающейся капли (Spindrop/Spinning drop)
Строение ПАВ
Как правило, ПАВ — органические соединения, имеющие амфифильное строение, то есть их молекулы имеют в своём составе полярную часть, гидрофильный компонент(функциональные группы -ОН, -СООН, -SOOOH, -O- и т. п., или, чаще, их соли -ОNa, -СООNa, -SOOONa и т. п.) и неполярную (углеводородную) часть, гидрофобный компонент. Примером ПАВ могут служить обычное мыло (смесь натриевых солей жирных карбоновых кислот — олеата, стеарата натрия и т. п.) и СМС (синтетические моющие средства), а также спирты, карбоновые кислоты, амины и т. п.
Области применения
Моющие средства. Основное применение ПАВ — в качестве активного компонента моющих и чистящих средств (в том числе, применяемых для дезактивации), мыла, для ухода за помещениями, посудой, одеждой, вещами, автомобилями и пр. В 2007 году в России было произведено более 1 млн тонн синтетических моющих средств, главным образом — стиральных порошков.
Косметика. Основное использование ПАВ в косметике — шампуни, где содержание ПАВ может достигать десятков процентов от общего объёма. Также ПАВ используются в небольших количествах в зубной пасте, лосьонах, тониках и других продуктах.
Текстильная промышленность. ПАВ используются в основном для снятия статического электричества на волокнах синтетической ткани.
Кожевенная промышленность. Защита кожаных изделий от лёгких повреждений и слипания.
Лакокрасочная промышленность. ПАВ используются для снижения поверхностного натяжения, что обеспечивает лёгкое проникновение красочного материала в маленькие углубления на обрабатываемой поверхности и их заполнение с вытеснением при этом оттуда другого вещества (например, воды).
Бумажная промышленность. ПАВ используются для разделения чернил и варёной целлюлозы при переработке использованной бумаги. Молекулы ПАВ адсорбируются на пигменте чернил. Пигмент становится гидрофобным. Далее воздух пропускается через раствор пигмента и целлюлозы. Пузырьки воздуха адсорбируются на гидрофобной части ПАВ и частички пигмента чернил всплывают на поверхность. См. флотация.
Металлургия. Эмульсии ПАВ используются для смазки прокатных станов. Снижают трение. Выдерживают высокие температуры, при которых сгорает масло.
Защита растений. ПАВ широко используются в агрономии и сельском хозяйстве для образования эмульсий. Используются для повышения эффективности транспортировки питательных компонентов к растениям через мембранные стенки.
Пищевая промышленность. ПАВ в виде эмульгаторов (например лецитина[источник не указан 260 дней]) добавляют для улучшения вкусовых качеств мороженого, шоколада, взбитых сливок, соусов для салатов и других блюд.
Нефтедобыча. ПАВ применяются для гидрофобизации призабойной зоны пласта (ПЗП) с целью увеличения нефтеотдачи.
Строительство. ПАВ[источник не указан 260 дней], называемые пластификаторами, добавляют к цементно-песчаным смесям и бетонам для уменьшения их водопотребности при сохранении подвижности. Это увеличивает конечную прочность (марку) затвердевшего материала, его плотность, морозостойкость, водонепроницаемость.
Медицина. Катионные и анионные ПАВ применяют в хирургии в качестве антисептиков. Например, четвертичные аммониевые соединения приблизительно в 300 раз эффективнее фенола по губительному действию в отношении микроорганизмов. Антимикробное действие ПАВ связывают с их влиянием на проницаемость клеточных мембран, а также ингибирующим действием на ферментативные системы микроорганизмов. Неионогенные ПАВ практически не обладают противомикробным действием.
Адсорбция (лат. ad — на, при; sorbeo — поглощаю) — это, в широком смысле, процесс изменения концентрации у поверхности раздела двух фаз, а в более узком и употребительном — это повышение концентрации одного вещества (газ, жидкость) у поверхности другого вещества (жидкость, твердое тело).
53. Дисперсные системы, гетерогенные системы из двух или большего числа фаз с сильно развитой поверхностъю раздела между ними. Обычно одна из фаз образует непрерывную дисперсионную среду, в объеме которой распределена дисперсная фаза (или несколько дисперсных фаз) в виде мелких кристаллов. твердых аморфных частиц, капель или пузырьков. Дисперсные системы могут иметь и более сложное строение, например, представлять собой двухфазное образование, каждая из фаз которого, будучи непрерывной, проникает в объем другой фазы. К таким системам относятся твердые тела. пронизанные разветвленной системой каналов-пор, заполненных газом или жидкостью. некоторые микрогетерогенные полимерные композиции и др. Нередки случаи, когда дисперсионная среда "вырождается" до тончайших слоев (пленок), разделяющих частицы дисперсной фазы.
Основные типы дисперсных систем. По дисперсности, то есть размеру частиц дисперсной фазы или отношению общей площади межфазной поверхности к объему (или массе) дисперсной фазы (удельной поверхности), Дисперсные системы условно делят на грубодисперсные и тонко(высоко)дисперсные. Последние, по традиции, называемые коллоидно-дисперсными или просто коллоидными системами. В грубодисперсных системах частицы имеют размеры от 1 мкм и выше (удельная поверхность не более 1 м2/г), в коллоидных - от 1 нм до 1 мкм (удельная поверхность достигает сотен м2/г). Дисперсность оценивают по усредненному показателю (среднему размеру частиц, удельной поверхности) или дисперсному составу (см. Дисперсионный анализ). Тонкопористые тела характеризуют пористостью -понятием, аналогичным дисперсности.В свободнодисперсных системах сцепление между частицами дисперсной фазы отсутствует, каждая частица кинетически независима и при достаточно малых размерах участвует в интенсивном броуновском движении. Для структурированных (связнодисперсных) систем характерно наличие неупорядоченной пространственной сетки (каркаса), образованной частицами дисперсной фазы (см. Структурообразование в дисперсных системах). Особую группу составляют высококонцентрированные дисперсные системы, в которых частицы находятся в "стесненных" условиях как, например, в периодических коллоидных структурах. Механические свойства свободнодисперсных систем определяются главным образом свойствами дисперсионной среды, а связнодисперсных систем - также свойствами и числом контактов между частицами дисперсной фазы.
По агрегатному состоянию дисперсионной среды и дисперсной фазы выделяют следующие основные виды дисперсных систем: 1) аэродисперсные (газодисперсные) системы с газовой дисперсионной средой: аэрозоли (дымы, пыли. туманы), порошки. волокнистые материалы типа войлока. 2) Системы с жидкой дисперсионной средой; дисперсная фаза может быть твердой (грубодисперсные суспензии и пасты, высокодисперсные золи и гели), жидкой (грубодисперсные эмульсии, высокодисперсные микроэмульсии и латексы) или газовой (грубодисперсные газовые эмульсии и пены). 3) Системы с твердой дисперсионной средой: стеклообразные или кристаллические тела с включениями мелких твердых частиц, капель жидкости или пузырьков газа, например, рубиновые стекла, минералы типа опала, разнообразные микропористые материалы. Отдельные группы дисперсных систем составляют многие металлические сплавы, горные породы, сложные композиционные и другие многофазные системы.
Лиофильные и лиофобные дисперсные системы с жидкой дисперсионной средой различаются в зависимости от того, насколько близки или различны по своим свойствам дисперсная фаза и дисперсионная среда. В лиофильных дисперсных системах межмолекулярные взаимодействия по обе стороны разделяющей фазы поверхности различаются незначительно, поэтому удельная свободная поверхностная энергия (для жидкости - поверхностное натяжение) чрезвычайно мала (обычно сотые доли мДж/м2), межфазная граница (поверхностный слой) может быть размыта и по толщине нередко соизмерима с размером частиц дисперсной фазы. Лиофильные дисперсные системы термодинамически равновесны, они всегда высокодисперсны, образуются самопроизвольно и при сохранении условий их возникновения могут существовать сколь угодно долго. Типичные лиофильные дисперсные системы - микроэмульсии. некоторые полимер-полимерные смеси, мицеллярные системы ПАВ, Дисперсные системы с жидкокристаллическими дисперсными фазами. К лиофильным дисперсным системам часто относят также набухающие и самопроизвольно диспергирующиеся в водной среде минералы группы монтмориллонита, например, бентонитовые глины.
Следует отметить, что в прошлом "лиофильными коллоидами" называли растворы полимеров. то есть принципиально гомогенные системы. Однако в современной терминологии понятие "коллоид" относится только к микрогетерогенным системам; по отношению к гомогенным (однофазным) системам его не употребляют.
В лиофобных дисперсных системах межмолекулярное взаимодействие в дисперсионной среде и в дисперсной фазе существенно различно; удельная свободная поверхностная энергия (поверхностное натяжение) велика - от нескольких единиц до нескольких сотен (и тысяч) мДж/м2; граница фаз выражена достаточно четко. Лиофобные дисперсные системы термодинамически неравновесны; большой избыток свободной поверхностной энергии обусловливает протекание в них процессов перехода в более энергетически выгодное состояние. В изотермических условиях возможна коагуляция -сближение и объединение частиц, сохраняющих первоначальные форму и размеры, в плотные агрегаты, а также укрупнение первичных частиц вследствие коалесценции -слияния капель или пузырьков газа, собирательной рекристаллизации (в случае кристаллич. дисперсной фазы) или изотермич. перегонки (молекулярного переноса) вещества дисперсной фазы от мелких частиц к крупным (в случае дисперсных систем с жидкой дисперсионной средой - последний процесс называемый переконденсацией). Нестабилизованные и, следовательно, неустойчивые лиофобные дисперсные системы непрерывно изменяют свой дисперсный состав в сторону укрупнения частиц вплоть до полного расслоения на макрофазы. Однако стабилизованные лиофобные дисперсные системы могут сохранять дисперсность в течение длительного времени.
Образование дисперсных систем. Возможно двумя путями: диспергационным и конденсационным. Диспергирование макрофаз с образованием лиофильных дисперсных систем происходит самопроизвольно - для этого достаточно энергии теплового движения. Такой процесс осуществляется при значениях поверхностного натяжения s ниже некоторого критического значения sкр = bkТ/d2, где d - размер частиц дисперсной фазы, Т - абсолютная температура, k - постоянная Больцмана. b - безразмерный коэффициент, принимающий значения примерно 10-30.
Образование лиофобных дисперсных систем путем диспергирования стабильной макрофазы требует значительных энергетических затрат, определяемых суммарной площадью поверхности частиц дисперсной фазы. В реальных условиях на образование поверхности при измельчении твердых тел или при распылении и эмульгировании жидкостей приходится лишь небольшая часть (доли процента) подводимой к системе энергии; остальное расходуется на побочные процессы и рассеивается в окружающем пространстве (см. Диспергирование).
Конденсационный путь образования дисперсных систем связан с зарождением новой фазы (или новых фаз) в пересыщенной метастабильной исходной фазе - будущей дисперсионной среде. Для возникновения высокодисперсной системы необходимо, чтобы число зародышей новой фазы было достаточно большим, а скорость их роста не слишком велика. Кроме того, требуется наличие факторов, ограничивающих возможности чрезмерного разрастания и сцепления частиц дисперсной фазы. Переход первоначально стабильной гомогенной системы в метастабильное состояние может произойти в результате изменения термодинамических параметров состояния (давления, температуры, состава). Так образуются, например, природные и искусственные аэрозоли (туман - из переохлажденных водяных паров, дымы - из парогазовых смесей, выделяемых при неполном сгорании топлива), некоторые полимерные системы - из растворов при ухудшении "термодинамического качества" растворителя, органические золи металлов путем конденсации паров металла совместно с парами органической жидкости или при пропускании первых через слой органической жидкости, коллоидно-дисперсные поликристаллические тела (металлические сплавы. некоторые виды горных пород и искусственных неорганических материалов).
Возможно также образование дисперсных систем в результате химической реакции в гомогенной среде, если продукт реакции при данных условиях находится в агрегатном состоянии, отличном от "материнской" фазы, или практически не растворяется в ней. Примерами подобных систем могут служить аэрозоли с твердыми частицами NH4Cl (образуются при взаимодействии газообразных NH3 и НСl), аэрозоли с капельно-жидкими частицами H2SO4 (при взаимодействии SO3 и водяного пара). В природе и технологических процессах часто образуются гидр.золи разного состава при гидролизе солей и др. соед., неустойчивых к действию воды. Окислительно-восстановительные реакции используют для получения золей Аu и Ag, разложение Na2S2O3 разбавленной серной или соляной кислотой - для получения гидрозоля элементарной серы. Хим. или термохим. разложения карбонатов, органических порофоров (порообразователей, вспенивающих агентов) и других соединений с выделением газообразных веществ в первоначально жидких средах лежит в основе промышленного производства многих пеноматериалов.
Устойчивость дисперсных систем характеризуется постоянством дисперсности (распределения частиц по размерам) и концентрации дисперсной фазы (числом частиц в единице объема). Наиболее сложна в теоретическом аспекте и важна в практическом отношении проблема устойчивости аэрозолей и жидких лиофобных дисперсных систем.
Различают седиментационную устойчивость и устойчивость к коагуляции (агрегативную устойчивость). Седиментационно устойчивы коллоидные системы с газовой и жидкой дисперсионной средой, в которых броуновское движение частиц препятствует оседанию; грубодисперсные системы с одинаковой плотностью составляющих их фаз; системы, скоростью седиментации в которых можно пренебречь из-за высокой вязкости среды.
В агрегативно устойчивых дисперсных системах непосредственно контакты между частицами не возникают, частицы сохраняют свою индивидуальность. При нарушении агрегативной устойчивости дисперсных систем частицы, сближаясь в процессе броуновского движения, соединяются необратимо или скорость агрегации становится значительно больше скорости дезагрегации. Между твердыми частицами возникают непосредственные точечные ("атомные") контакты, которые затем могут превратиться в фазовые (когезионные) контакты, а соприкосновение капель и пузырьков сопровождается их коалесценцией и быстрым сокращением суммарной площади межфазной поверхности. Для таких систем потеря агрегативной устойчивости означает также потерю седимeнтационной устойчивости.
В агрегативно устойчивых системах дисперсный состав может изменяться вследствие изотермич. перегонки - молекулярного переноса вещества дисперсной фазы от мелких частиц к более крупным. Этот процесс обусловлен зависимостью давления насыщенного пара (или концентрации насыщенного раствора) от кривизны поверхности раздела фаз.
Агрегативная устойчивость и длительное существование лиофобных дисперсных систем с сохранением их свойств обеспечивается стабилизацией. Для высокодисперсных систем с жидкой дисперсионной средой используют введение веществ - стабилизаторов (электролитов, ПАВ, полимеров. В теории устойчивости Дерягина-Ландау-Фервея-Овербека (теории ДЛФО) основная роль отводится ионно-электростатическому фактору стабилизации. Стабилизация обеспечивается электростатическим отталкиванием диффузных частей двойного электрического слоя, который образуется при адсорбции ионов электролита на поверхности частиц. При некотором расстоянии между частицами отталкивание диффузных слоев обусловливает наличие минимума на потенциальной кривой (дальний, или вторичный, минимум; смотри рисунок). Хотя этот минимум относительно неглубок, он может препятствовать дальнейшему сближению частиц, притягиваемых силами межмолекулярного взаимодействия. Ближний, или первичный, минимум соответствует прочному сцеплению частиц, при котором энергии теплового движения недостаточно для их разъединения. Сближаясь на расстояние, отвечающее этому минимуму, частицы объединяются в агрегаты, образование которых ведет к потере системой агрегативной устойчивости. При этом устойчивость системы к коагуляции определяется высотой энергетического барьера.
Зависимость энергии взаимодействия Е между частицами от расстояния R: 1 и 2 - ближний и дальний минимумы соответственно.
При введении в Дисперсные системы в качестве стабилизатора ПАВ фактором стабилизации может быть "термодинамическая упругость" пленок среды, разделяющей частицы. Стабилизация обеспечивается тем, что при сближении частиц, например, капель или газовых пузырей, происходит растяжение и утоньшение разделяющей их прослойки, содержащей ПАВ, и, как следствие, нарушение адсорбционного равновесия. Восстановление этого равновесия и приводит к повышению устойчивости прослойки среды, разделяющей частицы.
Гидродинамич. сопротивление вытеснению жидкой дисперсионной среды из прослойки между сближающимися частицами - один из кинетических факторов стабилизации дисперсных систем. Он особенно эффективен в системах с высоковязкой дисперсионной средой, а при застекловывании последней делает систему неограниченно устойчивой к агрегации частиц и коалесценции. Структурно-механический фактор стабилизации, по П. А. Ребиндеру, возникает при образовании на межфазной границе полимолекулярных защитных слоев из мицеллообразующих ПАВ, высокомолекулярных соединений, а иногда и тонких сплошных или дискретных фазовых пленок. Межфазный защитный слой должен обладать способностью сопротивляться деформациям и разрушению, достаточной подвижностью для "залечивания" возникших в нем дефектов и, что особенно важно, быть лиофилизованным с внешней стороны, обращенной в сторону дисперсионной среды. Если защитный слой недостаточно лиофилен, он, предохраняя частицы от коалесценции. не сможет предотвратить коагуляции. Структурно-механический барьер является, по существу, комплексным фактором стабилизации, который включает термодинамические, кинетические и структурные составляющие. Он универсален и способен обеспечить высокую агрегативную устойчивость любых дисперсных систем с жидкой дисперсионной средой, в том числе высококонцентрированных, наиболее важных в практическом отношении.
Основные свойства дисперсных систем определяются поверхностными явлениями: адсорбцией, образованием двойного электрического слоя и обусловленных им электрокинетических явлений, контактными взаимодействиями частиц дисперсной фазы. Размер частиц определяет оптические (светорассеяние и другие) и молекулярно-кинетические свойства (диффузия, термофорез, осмос и дрeubt).
Дисперсные системы повсеместно распространены в природе. Это - горные породы, грунты, почвы, атмосферные и гидросферные осадки, растительные и животные ткани. Дисперсные системы широко используют в технологических процессах; в виде дисперсных систем выпускается большинство промышленных продуктов и предметов бытового потребления. Высокодисперсные технические материалы (наполненные пластики, дисперсноупрочненные композиционные материалы) отличаются чрезвычайно большой прочностью. На высокоразвитых поверхностях интенсивно протекают гетерогенные и гетерогенно-каталитические химические процессы.
Учение о дисперсных систем и поверхностных явлениях в них составляет сущность коллоидной химии. Самостоятельный раздел коллоидной химии - физико-химическая механика - изучаeт закономерности структурообразования и механические свойства структурированных дисперсных систем и материалов в их связи с физико-химическими явлениями на межфазных границах.
54. Золь иначе лиозоль; коллоидный раствор (англ. sol от лат. solutio — раствор) — высокодисперсная коллоидная система (коллоидный раствор) с жидкой (лиозоль) или газообразной (аэрозоль) дисперсионной средой, в объеме которой распределена другая (дисперсная) фаза в виде капелек жидкости, пузырьков газа или мелких твердых частиц, размер которых лежит в пределе от 1 до 100 нм (10−9—10−7м)[1].
Строение мицеллы
Мицеллой лиофобной системы называется гетерогенная микросистема, которая состоит из микрокристалла дисперсной фазы, окруженного сольватированными ионами стабилизатора.
Потенциалопределяющими называются ионы, адсорбирующиеся на поверхности частички твердой фазы (агрегата) и придающие ей заряд. Агрегат вместе с потенциалопределяющими ионами составляет ядро мицеллы.
Противоионы – ионы, группирующиеся вблизи ядра мицеллы.
Расположение противоионов в дисперсионной среде определяется двумя противоположными факторами: тепловым движением (диффузией) и электростатическим притяжением.
Противоионы, входящие в состав плотного адсорбционного слоя, называются «связанными» и вместе с ядром составляют коллоидную частицу, или гранулу. Коллоидная частица (гранула) имеет заряд, знак которого обусловлен знаком заряда потенциалопределяющих ионов.
Противоионы, образущие диффузный слой, – «подвижные», или «свободные».
Коллоидная частица с окружающим ее диффузным слоем сольватированных про-тивоионов составляют мицеллу. В отличие от коллоидной частицы мицелла электронейтральна и не имеет строго определенных размеров.

В мицелле с ионным стабилизатором на границе раздела фаз имеется ДЭС, возникает разность потенциалов между дисперсной фазой и дисперсионной средой – термодинамический потенциал ф (межфазный), который определяется свойствами данной дисперсной системы, а также зарядом и концентрацией потенциалопределяющих ионов, адсорбированных на твердой фазе.
Перемещение заряженных коллоидных частиц в неподвижной жидкости к одному из электродов под действием внешнего электрического поля называется электрофорезом.
Поверхность, по которой происходит перемещение, называется поверхностью скольжения. Величина скачка потенциала на границе фаз, находящихся в движении относительно друг друга при электрофорезе и в броуновском движении, т. е. на поверхности скольжения, называется электрокинетическим или ζ-потенциалом (дзета-потенциал).
Золь +соль =..." - так мы описали воздействие электролита на дисперсную систему (ДС). Многоточие - это вопрос об устойчивости золя к этому воздействию.
Устойчивость дисперсных систем (ДС) — это способность сохранять постоянство своих свойств во времени или при достаточно сильном изменении условий. Всеобъемлющим свойством является равномерность распределения частиц дисперсной фазы по всему объему системы. Различают два вида устойчивости ДС: агрегативную и седиментационную. Понятие об агрегативной (как устойчивости к коагуляции, т.е. к слипанию частиц) и седиментационной устойчивости (как устойчивости к оседанию частиц) дисперсных систем впервые было введено Н.П. Песковым.
В литературе понятие устойчивости часто используется в узком смысле — как способность ДС противостоять коагуляции при введении в нее электролита. Это объясняется тем, что длительное время введение электролитов оставалось единственным способом дозированного воздействия на состояние системы, результаты которого можно было увидеть, зарегистрировать и принять в качестве характеристики устойчивости. (Вот откуда название «золь + соль =…»).
Естественно, что низкая агрегативная устойчивость приводит к укрупнению частиц, а крупные частицы могут оседать, поэтому существует глубокая связь между агрегативной и седиментационной устойчивостью.
Теория устойчивости ДС получила общее признание под названием «теория ДЛФО» — по именам авторов Дерягин Б.В., Ландау Л.Д., Фервей (Vervey) и Овербек (Overbek). В ней рассматривается совместное действие сил притяжения и отталкивания между частицами. Чтобы поддерживать стабильность коллоидной системы, силы отталкивания должны быть доминирующими. Все проблемы устойчивости ДС упираются в строение ДЭС (двойного электрического слоя). Важнейшей характеристикой устойчивости ДЭС является ζ -потенциал. На его величину оказывают влияние: температура, pH, концентрация золя, диэлектрическая проницаемость, вязкость дисперсионной среды и т.д. Наиболее сильное влияние на стпроение ДЭС оказывает добавление электролитов, приводящее к коагуляции золей. Для начала коагуляции золя необходима некоторая минимальная концентрация электролита, называемая порогом коагуляции.
Коагулирующим действием обладает тот из ионов электролита, заряд которого противоположен заряду коллоидных частиц. При увеличении концентрации электролита в растворе происходит перераспределение противоионов между адсорбционным и диффузными слоями ДЭС. ζ –потенциал (и заряд частицы) уменьшается, уменьшается отталкивание между частицами, происходит коагуляция.
В рядах неорганических ионов с одинаковыми зарядами коагулирующее действие возрастает с уменьшением их размера. Ионы одинаковой валентности располагаются в так называемые лиотропные ряды (ряды Гофмейстера): Li+— Na+— K+— Rb+— Cs+.
Коагулирующее действие иона обратно пропорционально его заряду в шестой степени (привило Щульце-Гарди). Внедрение многозарядного иона в плотный слой ДЭС приводит к резкому падению ζ –потенциала (и заряда частицы) вплоть до ноля, наступает изоэлектрическое состояние. А при сверхэквивалентном содержании такого иона в плотном слое произойдет перезарядка поверхности. При добавлении к отрицательному золю электролитов с многозарядными катионами–коагулянтами наблюдается явление «неправильных рядов коагуляции». Также возможна взаимная коагуляция золей.
На практике необходимо учитывать, что для протекания коагуляции необходимо время, т.е. кинетику коагуляции золей.
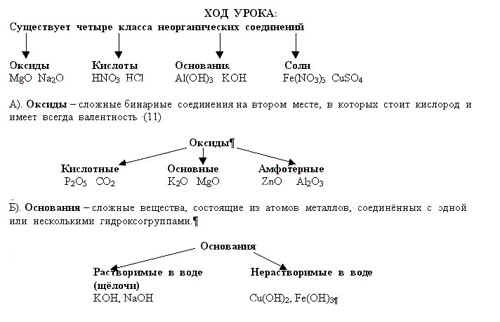
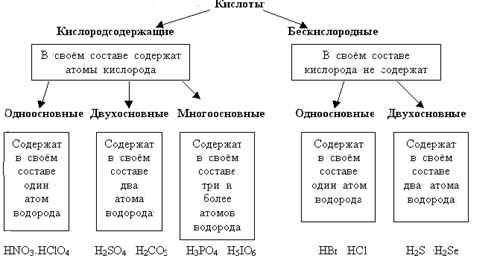
Окси́д (о́кисел, о́кись) — бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся почти все соединения химических элементов с кислородом. К исключениям относятся, например, дифторид кислорода OF2.
Оксиды — весьма распространённый тип соединений, содержащихся в земной коре и во Вселенной вообще. Примерами таких соединений являются ржавчина, вода, песок, углекислый газ, ряд красителей. Оксидами называется класс минералов, представляющих собой соединения металла с кислородом (см. Окислы).
Соединения, которые содержат атомы кислорода, соединённые между собой, называются пероксидами (перекисями; содержат цепочку −O−O−), супероксидами (содержат группу О−2) и
озонидами (содержат группу О−3). Они не относятся к категории оксидов.
Классификация
В зависимости от химических свойств различают:
Солеобразующие оксиды:
основные оксиды (например, оксид натрия Na2O, оксид меди(II) CuO): оксиды металлов, степень окисления которых I—II;
кислотные оксиды (например, оксид серы(VI) SO3, оксид азота(IV) NO2): оксиды металлов со степенью окисления V—VII и оксиды неметаллов;
амфотерные оксиды (например, оксид цинка ZnO, оксид алюминия Al2О3): оксиды металлов со степенью окисления III—IV и исключения (ZnO, BeO, SnO, PbO);
Несолеобразующие оксиды: оксид углерода(II) СО, оксид азота(I) N2O, оксид азота(II) NO.
Номенклатура
В соответствии с номенклатурой ИЮПАК, оксиды называют словом «оксид», после которого следует наименование химического элемента в родительном падеже, например: Na2O — оксид натрия, Al2O3 — оксид алюминия. Если элемент имеет переменную степень окисления, то в названии оксида указывается его степень окисления римской цифрой в скобках сразу после названия (без пробела). Например, Cu2О — оксид меди(I), CuO — оксид меди(II), FeO — оксид железа(II), Fe2О3 — оксид железа(III), Cl2O7 — оксид хлора(VII).
Часто используют и другие наименования оксидов по числу атомов кислорода: если оксид содержит только один атом кислорода, то его называют монооксидом или моноокисью, если два — диоксидом или двуокисью, если три — то триоксидом или триокисью и т. д. Например: монооксид углерода CO, диоксид углерода СО2, триоксид серы SO3.
Также распространены исторически сложившиеся (тривиальные) названия оксидов, например угарный газ CO, серный ангидрид SO3 и т. д.
В начале XIX века и ранее тугоплавкие, практически не растворимые в воде оксиды химики называли «землями».
Оксиды с низшими степенями окисления (субоксиды) иногда по старой русской номенклатуре называют[1] закись (англ. аналог — protoxide) и недокись (например, оксид углерода(II), CO — закись углерода; диоксид триуглерода, C3O2 — недокись углерода[2]; оксид азота(I), N2O — закись азота; оксид меди(I), Cu2O — закись меди). Высшие степени окисления (оксид железа(III), Fe2O3) называют в соответствии с этой номенклатурой окись, а сложные оксиды — закись-окись (Fe3O4 = FeO·Fe2O3 — закись-окись железа, оксид урана(VI)-диурана(V), U3O8 — закись-окись урана). Эта номенклатура, однако, не отличается последовательностью, поэтому такие названия следует рассматривать скорее как традиционные.






