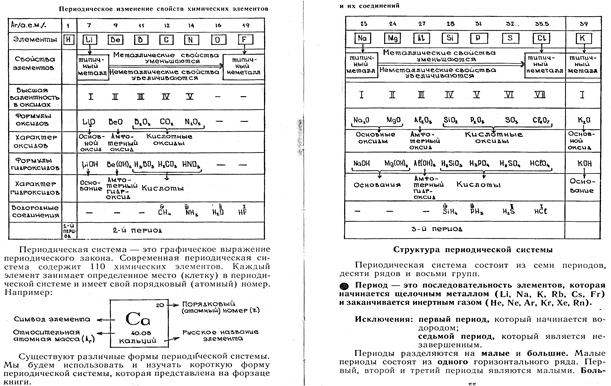


Энергетическая диаграмма уровней и подуровней, последовательность заполнения орбиталей в соответствии с принципом миним. Энергии: Клечковский, Паули, Гунд.

Энергию электрона на 90-95% определяет главное квантовое число – порядковый
№ энергетического уровня-(расстояние от ядра) – "n", которое принимает значения от 1 до 7, далее – до бесконечности, соответствующее превращению нейтрального атома в катион (+1) при отрыве 1е;
l – орбитальное квантовое число, определяет форму орбитали:
l = 0 – s орбиталь, l = 1 – p орбиталь, l = 2 орбиталь, l = 3 d – орбиталь
Энергия электрона зависит от суммы главного и орбитального чисел ∑(n + l)
Последовательность застройки (б) полностью отражает изменение значения







Выделение (поглощение) тепла – экзо- или эндотермические процессы






