Введение
Флюорит СаF2 (от латинского "fluo") - текучий. Живший в XVI веке в горнорудных районах Саксонии и Чехии врач Георг Бауэру взявший латинский псевдоним Агрикола, назвал этот камень флюоритом. Этот минерал в качестве добавки при плавлении руды, придавал шлакам текучесть и они легко отделялись от металла. За эти же свойства его стали называть - плавиковым шпатом или флюсшпатом.

рис.1 - флюорит
Для оптических целей давно используются природные кристаллы: каменная соль(NaCl)(кубическая решетка), сильвин(KCl), флюорит (СаF2),кварц(SiO2), кальцит(CaCo3), слюда.
Из этих кристаллов изготавливают призмы, окна, детали проекционных микроскопов, спектральных приборов, компенсаторы. Однако природные оптические кристаллы надлежащей однородности, прозрачности и размеров встречаются редко. Поэтому только с развитием методов искусственного выращивания кристаллы в больших масштабах стали применяться кристаллические материалы.
Не все кристаллы встречаются в природе. Кристаллы KDP и ADP, полупроводниковые кристаллы(Si, Ge …), в природе не встречаются и выращиваются искуственно.
Число синтетических кристаллов уже давно превышает число природных, т.е. в оптотехнике используются искусственные кристаллы за некоторым исключением, так как искусственные дешевле.
Основными поставщиками флюоритов являются Монголия, Мексика, ЮАР, Китай, Испания. Встречаются флюориты в Германии, Италии, Франции, Норвегии, Гренландии, Великобритании, Канаде, США, Таджикистане. Крупные месторождения известны в Узбекистане, Киргизии, Казахстане. В России месторождения флюорита есть в Читинской области, Приморье и на Северном Кавказе.
Структура
Сингония - кубическая; гексаоктаэдрический в. с. 3L44L636L29PC.
Кристаллическая структура - является типической для многих соединений типа АХ2. Она характеризуется двумя координационными числами: для Са-8 и для F-4 (рис. 2). Ионы Са2+ расположены так, как в гранецентрированном кубе (по углам и в центрах граней). Ионы F1- занимают центры всех малых кубов (рис. 3).
Облик кристаллов - В пустотах встречается в виде хорошо образованных кубических (рис. 4), реже октаэдрических и додекаэдрических кристаллов. Кроме форм {100), {111} и {110), иногда присутствуют {210}, {421} и др. Кристаллы в редких случаях достигают 20-25 см в поперечнике. Грани куба обычно гладкие, а октаэдрические грани-матовые. Иногда грани куба исштрихованы параллельно четырем ребрам или образуют паркетообразный рисунок. Двойники часты по (111).
Агрегаты - Чаще наблюдается в виде вкраплений и сплошных зернистых, реже землистых, масс (ратовкит).
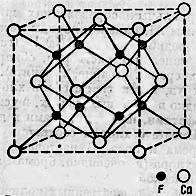
Рис 2. Кристаллическая решетка флюорита
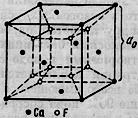
Рис 3. Кристаллическая решетка флюорита
Химический состав
Са 51,2%, F 48,8%. Иногда содержит в виде изоморфной примеси Сl (главным образом желтые разности). В некоторых случаях обнаруживаются битуминозные вещества, издающие запах. Из других примесей укажем Fe2O3, редкие земли, изредка уран (до нескольких процентов), фтор и гелий.
Отличительные свойства (оптические, термохимические, химические и др.)
Цвет. Флюорит редко бывает бесцветным и водяно-прозрачным. Большей частью окрашен в различные цвета: желтый, зеленый, голубой, фиолетовый, иногда фиолетово-черный. Любопытно, что окраска исчезает при нагревании, и вновь возвращается при облучении рентгеновскими лучами. В бесцветных кристаллах можно вызвать фиолетовую окраску также действием паров металлического кальция и электрическими разрядами. Это наводит на мысль, что в ряде случаев цвет обусловлен появлением в кристаллической структуре электрически нейтральных атомов Са и F.
Блеск стеклянный. N = 1,434.
Твердость 4. Хрупок. При продолжительном одностороннем давлении обнаруживает пластическую деформацию.
Спайность совершенная по октаэдру, а не по ромбическому додекаэдру, как это можно было бы ожидать, исходя из представлений о том, что наименьшее сцепление должно иметь место для плоских сеток с наибольшими расстояниями друг от друга. Объясняется это тем, что среди плоских сеток (111) каждая сетка ионов кальция переслоена двумя параллельными сетками одинаково заряженных ионов фтора, чем и обусловливается наименьшее сцепление именно между ними.
Удельный вес 3,18 (у нечистых разностей колеблется в пределах 3,0-3,2).
Прочие свойства. Часто проявляется флюоресценция (термин произошел именно от названия этого минерала). В катодных лучах флюорит светится обычно фиолетовым цветом со своеобразным синевато-зеленым оттенком. Свечение появляется также при нагревании (термолюминесценция).
Применение
Основными потребителями плавикового шпата являются металлургическая и химическая промышленность, а также атомная энергетика и производство сварочных материалов.
В небольшом количестве он применяется в производстве цемента, непрозрачных белил и эмалей.
В черной металлургии плавиковый шпат используется в качестве флюса для разжижения шлаков при выплавке стали, чугуна, получении сплавов специального назначения. В качестве фторсодержащего сырья для черной металлургии возможно использование и бедных карбонатно-флюоритовых руд или оплавикованных известняков (с содержанием флюорита от 3 до 15 %) без предварительного обогащения.
В химической промышленности плавиковый шпат служит основным сырьем для получения плавиковой кислоты, безводного фтористого водорода, фтористых солей и прочих фторсодержащих продуктов. Фтористые соли широко используются в цветной металлургии: криолит (Na3AlF6) служит растворителем глинозема при электролитическом способе производства алюминия; фтористый алюминий (AlF3) и фтористый натрий (NaF) добавляются для корректирования состава криолитового электролита. Фтористые соли используются также для получения стекловолокна и многих других продуктов.
В производстве сварочных материалов плавиковый шпат используется при изготовлении электродов, порошковой проволоки, плавленых и керамических сварочных флюсов. В небольших количествах он используется и в литейном производстве. Неорганические фториды и фторсиликаты применяются в качестве дезинсекционных средств и при производстве кислотоупорных бетонов. Фтористый водород используется в процессах органического синтеза, а также при получении высокооктанового бензина; фторпроизводные углеводородов применяются в атомной энергетике, используются как смазочные материалы и пластмассы, обладающие высокой химической и термической стойкостью. Фторхлорпроизводные углеводородов (фреоны) применяются в холодильной промышленности. Бифториды калия, натрия, алюминия и углерода используются для получения элементного фтора.
В производстве цемента плавиковый шпат применяется как добавка, облегчающая процесс обжига клинкера. В производстве стекол и эмалей его используют для придания непрозрачности, а также для ускорения варки стекла.






