÷ели, задачи:
Ќа фактическом уровне получени€ знаний:
1. ќсновные положени€ квантовой механики, квантово-механическа€ модель атома, квантовые числа;
2. ѕон€тие электронной орбитали, основные правила и принципы заполнени€ электронами атомных орбиталей;
3. Ёлектронные формулы атомов, электронно-графические схемы;
4. –аспределение химических элементов по электронным семействам;
5. ѕериодический закон ƒ.». ћенделеева, структура периодической системы элементов.
Ќа операционном уровне получени€ знаний:
ќбучить студента:
1. «аписывать полную электронную формулу атома любого химического элемента;
2. ќписывать набором четырех квантовых чисел любой электрон в атоме на основании приведенной электронной формулы;
3. –аспредел€ть электроны по квантовым €чейкам в электронно-графической схеме.
Ќа аналитическом уровне получени€ знаний:
ќбучить студента:
1. ѕо приведенной электронной формуле атома определ€ть энергетическое состо€ние атома (нормальное, возбужденное или запрещенное);
2. ќпредел€ть электронейтральное или ионное состо€ние описывает данна€ электронна€ формула;
3. ѕо электронной формуле валентной структуры атома указывать местоположение данного химического элемента в периодической системе (период, группа, подгруппа) возможные его степени окислени€;
4. ќпредел€ть, к какому электронному семейству элементов относитс€ данный элемент и правильно назвать его электронные аналоги.
‘актический материал:
I. раткое изложение основных положений квантовой механики: а) квантованность энергии; б) корпускул€рно-волновой дуализм электрона, уравнение де Ѕройл€ (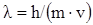 ; в) пон€тие орбитали и волновой функции, физический смысл квадрата волновой функции
; в) пон€тие орбитали и волновой функции, физический смысл квадрата волновой функции 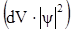 ; г) энергетическое описание электрона в атоме набором четырех квантовых чисел (привести возможные значени€ и физический смысл каждого квантового числа).
; г) энергетическое описание электрона в атоме набором четырех квантовых чисел (привести возможные значени€ и физический смысл каждого квантового числа).
II. ќсновные правила и принципы распределени€ электронов по электронным орбитал€м в многоэлектронных атомах: а) принцип минимума энергии, правила лечковского; б) принцип ѕаули; в) правило ’унда. Ёлектронна€ формула атома (полна€ и формула валентной структуры). ѕон€тие квантовой электронной орбитали (квантовой €чейки), графическое изображение электронной оболочки атома при помощи энергетической диаграммы Ц электронно-графической схемы.
III. —труктура периодической системы элементов. Ёлектронные семейства химических элементов. –аспределение химических элементов по периодам, группам и подгруппам согласно структуры их электронных оболочек (s-, p-, d-, f- элементы). ѕон€тие электронных аналогов. ратка€ характеристика общих основных химических свойств элементов (окислительно-восстановительных и кислотно-основных) по электронным семействам. ѕон€тие потенциала ионизации и сродства к электрону и изменение этих характеристик элементов в периодической системе. —овременна€ формулировка периодического закона ƒ.». ћенделеева.
¬ыводы по теме:
1. јтом сложна€ система, химические свойства которой определ€ютс€ структурой ее электронной оболочки.
|
|
|
2. –аспределение электронов в атоме подчин€етс€ принципам и правилам квантовой механики.
3. ѕериодически повтор€ющиес€ с возрастанием зар€да €дра атомов однотипные электронные конфигурации атомов лежат в основе периодического закона и определ€ют структуру периодической системы элементов.
¬опросы дл€ самопроверки:
1. ”казать элемент, которому соответствует электронна€ формула атома 1s22s22p63s23p63d104s24p2:
а) —а; б) Zn; в) Ge.
2. ”казать полное число электронов в атоме, валентна€ структура которого имеет формулу 3d104s2:
а)30; б) 18; в) 20.
3. ƒл€ атома с массовым числом 36 а.е.м. и пор€дковым номером 17 в периодической системы укажите число протонов (р) и нейтронов (n) в €дре и число электронов (е) в электронной оболочке нейтрального атома:
а) р=17,n=19, е=17; б) р=19, n=17, е=17; в) р=17, n=17, е=17.
4. »зотопы какого элемента (Ni, Zn,Si) имеют в €дре соответствующее количество протонов (р) и нейтронов (n):
а) р=14, n=14; б) р=14, n=15; в) р=14, n=16?
5. —колько неспаренных электронов имеет атом марганца Mnв основном состо€нии:
а) 7; б) 5; в) 2.
6. јтом какого элемента в основном состо€нии содержит три свободных 4d орбитали:
а) Sc; б) V; в)Zr?
7. ”читыва€ правило ’унда, определить, атому какого элемента соответствует электронна€ конфигураци€ валентной структуры 1s22s22p63s13p3 в высшем энергетическом состо€нии:
а) P; б) As; в)Si.
8. √идроксид какого элемента: Na, Mg или Al €вл€етс€ более сильным основанием:
а)Na; б) Mg; в) Al.
9. √идроксид какого элемента: алюмини€ 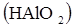 , кремни€
, кремни€ 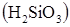 или фосфора
или фосфора 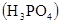 €вл€етс€ более сильной кислотой:
€вл€етс€ более сильной кислотой:
а) Al; б) Si; в)P.
10. «начени€ первых потенциалов ионизации элементов I группы периодической системы соответственно равны (в вольтах): Li (5,4); Cu (7,7); Ag (9,2). ”казать, у какого элемента металлические свойства выражены сильнее:
а) Li; б) Cu; в) Ag.
“ема 2. ’имическа€ св€зь
÷ели и задачи:
Ќа фактическом уровне получени€ знаний:
1. ѕон€тие молекулы и иона;
2. ќсновные положени€ теории химического строени€ ј.ћ. Ѕутлерова;
3. ѕон€тие химической св€зи;
4. ”слови€ и механизмы образовани€ химической св€зи;
5. ћетоды описани€ химической св€зи, ¬— и ћќ;
6. ’арактеристики, виды и свойства химических св€зей;
7. “еории гибридизации и валентность;
Ќа операционном уровне получени€ знаний:
ќбучить студента:
1. ќпредел€ть виды химической св€зи в молекулах, ионах, кристаллах;
2. ќценивать пол€рность св€зи;
3. –ассчитывать степени окислени€ атомов в молекулах и ионах;
4. —оставл€ть валентные схемы молекул и комплексных ионов;
5. ќпредел€ть основные типы гибридизации атомов и геометрию молекул.
Ќа аналитическом уровне получени€ знаний:
ќбучить студента:
1. ќценивать основные свойства газов, жидких и твердых веществ на основании знаний о химических св€з€х в их молекулах;
2. ѕрогнозировать физические и химические свойства твердого вещества по природе частиц и типу химической св€зи между ними;
3. ќценивать донорно-акцепторные свойства ионов и атомов элементов.
‘актический материал:
I. ќсновное условие образовани€ химической св€зи между атомами -выброс энергии из системы взаимодействующих атомов, рассмотреть на примере функциональной зависимости энергии системы от меж€дерного рассто€ни€ при образовании молекулы водорода. ѕривести основные виды химической св€зи в веществе: ковалентна€ (непол€рна€, пол€рна€), ионна€, металлическа€.
|
|
|
ћеханизмы образовани€ ковалентной св€зи:
1) ќбменный механизм, основные положени€ теории химической св€зи Ц метода валентных св€зей (¬—): а) взаимодействие одноэлектронных атомных орбиталей двух атомов с антипараллельными спинами с образованием общей электронной пары; б) возникновение в меж€дерном пространстве области увеличенной электронной плотности, несущей избыточный отрицательный зар€д; в) прит€жение положительно зар€женный €дер атомов к области увеличенной электронной плотности при строго фиксированном меж€дерном рассто€нии, которое соответствует минимальному энергетическому запасу возникшей молекулы.
2) ƒонорно-акцепторный механизм, пон€тие донора и акцептора (на примере образовани€ молекулы водорода при взаимодействии двух ионов водорода 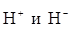 ).
).
II. »зложить основные характеристик ковалентной св€зи: а) что такое энерги€ св€зи и от чего зависит ее величина; б) длина св€зи (величина меж€дерного рассто€ни€), как вли€ет длина св€зи и ее энерги€ на прочность молекулы (энергию диссоциации молекулы на атомы); в) насыщаемость ковалентной св€зи, ковалентность атома (пон€тие валентности элемента, как количества квантовых орбиталей, предоставленных атомом на образование определенного количества общих электронных пар с другими атомами), рассмотреть на примере образовани€ водородных соединений бора, углерода и азота; г) направленность ковалентной св€зи (образование 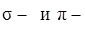 св€зи); д) пол€ризуемость ковалентной св€зи (образование непол€рной и пол€рной св€зи), характеристика пол€рности св€зи Ц дипольный момент молекулы. ѕон€тие электроотрицательности атома (как полусуммы энергий ионизации и сродства к электрону), определ€ющей сдвиг общей электронной пары на один из атомов при образовании св€зи. “аблица относительных значений электроотрицательности.
св€зи); д) пол€ризуемость ковалентной св€зи (образование непол€рной и пол€рной св€зи), характеристика пол€рности св€зи Ц дипольный момент молекулы. ѕон€тие электроотрицательности атома (как полусуммы энергий ионизации и сродства к электрону), определ€ющей сдвиг общей электронной пары на один из атомов при образовании св€зи. “аблица относительных значений электроотрицательности.
III. явление гибридизации валентных орбиталей атомов элементов второго периода (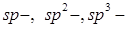 гибридизаци€), показать на примере углерода в его водородных соединени€х, графите и алмазе. ѕривести примеры и объ€снить пространственное строение и пол€рность: линейных непол€рных 3-х атомных молекул (
гибридизаци€), показать на примере углерода в его водородных соединени€х, графите и алмазе. ѕривести примеры и объ€снить пространственное строение и пол€рность: линейных непол€рных 3-х атомных молекул (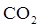 ), угловых 3-х атомных пол€рных молекул (
), угловых 3-х атомных пол€рных молекул (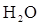 ), 4-х атомных непол€рных молекул (
), 4-х атомных непол€рных молекул (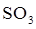 ), пол€рных (
), пол€рных (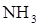 ).
).
IV. ѕредельный случай сильно пол€рной ковалентной св€зи €вл€етс€ св€зь ионна€, ее характеристики (ненаправленность и ненасыщенность). Ёнерги€ ионной св€зи, котора€ пропорциональна произведению зар€дов ионов и обратно пропорциональна длине ионной св€зи. Ќеполное разделение зар€дов в ионных соединени€х, взаимна€ пол€ризаци€ ионов, как следствие деформации электронных оболочек ионов. ‘акторы вли€ющие на пол€ризуемость ионов и пол€ризующую способность: а) величина ионного радиуса (чем больше значение радиуса, тем выше пол€ризуемость иона и меньше пол€ризующа€ способность); б)степень гидратации иона (чем выше степень гидратации, тем меньше его пол€ризуемость); в) величина зар€да иона (чем больше зар€д иона, тем выше пол€ризующа€ способность). “.к. размеры анионов,как правило, больше радиусов катионов, анионы обладают меньшей пол€ризующей способностью, но сильной пол€ризуемостью.
V. ƒать общее пон€тие о комплексных соединени€х, как соединени€х характеризуемых наличием двух видов св€зи: а) ионной (во внешней координационной сфере); б) ковалентной донорно-акцепторной (во внутренней координационной сфере). ѕривести координационную формулу комплексного соединени€ (например 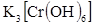 ). ратко изложить: а) теорию строени€ комплексов (пон€ти€: комплексообразователь, лиганд, координационное число); б)процессы первичной и вторичной диссоциации; в) количественную характеристику устойчивости комплексной частицы (выражение константы нестойкости).
). ратко изложить: а) теорию строени€ комплексов (пон€ти€: комплексообразователь, лиганд, координационное число); б)процессы первичной и вторичной диссоциации; в) количественную характеристику устойчивости комплексной частицы (выражение константы нестойкости).
VI. ќбщие представлени€ о теории молекул€рных орбиталей (расщепление энергии валентных орбиталей взаимодействующих атомов), на примере энергетических диаграмм образовани€ молекул водорода и кислорода. ќсновные положени€ зонной теории кристаллов металлов: а) образование непрерывной энергетической зоны (ЌЁ«); б) заполнение электронами энергетических уровней ЌЁ« согласно правилам квантовой механики; в) деление ЌЁ« на две подзоны (валентную зону и зону проводимости); г) возникновение электронного газа в кристалле, как совокупности делокализованных электронов в зоне проводимости. ѕон€тие металлической св€зи, как общей электронной плотности, обусловленной совокупностью делокализованных электронов. ќсновные физико-механические свойства кристаллов металлов, обусловленные наличием металлической св€зи: электропроводность, теплопроводность, пластичность (способность к упругой деформации), ковкость и др.
|
|
|
¬ыводы по теме:
1. ¬иды химичесих св€зей в зависимости от природы образующих их частиц подраздел€ютс€ на ковалентную, ионную, металлическую и водородную.
2. овалентна€ св€зь формируетс€ обменным и донорно-акцепторным взаимодействи€ми. ’арактеристиками св€зи €вл€ютс€ энерги€, длина, насыщаемость, направленность, кратность. —войства соединений определ€ютс€ типом их решетки.
3. »онна€ св€зь образуетс€ вследствие электростатического взаимодействи€ атомов диаметрально противоположной природы. »онные соединени€ представлены ионной кристаллической решеткой, параметры и характеристики которой определ€ют свойства ионных соединений.
4. ћеталлическа€ св€зь €вл€етс€ многоценровой, ненаправленной, ненасыщаемой. —войства металлической кристаллической решетки определ€ют свойства металлических тел..
¬опросы дл€ самопроверки:
1. —колько электронов участвует в образовании химических св€зей в молекуле аммиака:
а) 8; б)6; в)3.
2. ¬ыбрать вещества, все св€зи которых ковалентные:
а)NaCl, HCl,Cu,H2O;
б)CO2, CH4, H2SO4, J2;
в)SO2, HNO2, NaOH, PbO.
3. ¬ каком р€ду молекулы расположены в пор€дке увеличени€ пол€рности св€зей:
а)HF, HCl, HBr;
б) NH3, PH3, AsH3;
в)H2Se, H2S, H2O.
4. ќтметить формулы соединений с одинаковой степенью окислени€ азота:
а) Mg3N2; б)NO; в) NO2; г)NH3.
5. ¬ каких частицах наблюдаетс€ только sp3- гибридизаци€ центрального атома:
а) NH3, H2O, C2H4, [Zn(NH3)4]2+;
б)H2O, NH3, C2H2, [HgJ4]2-;
в)NH3, NH4+, CH4, [Zn(NH3)4]2+ .
”казать другие типы гибридизации в этих соединени€х.
6. ¬алентность атома азота численно равна его степени окислени€ в молекуле:
а) аммиака; б) азотной кислоты; в) азота; г) оксида азота (II).






