1. Ионное произведение воды - это:
2. Водородный показатель рассчитывается по формуле:
3. В химической реакции 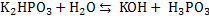 второй ступенью диссоциации будет уравнение:
второй ступенью диссоциации будет уравнение:
4. В химической реакции 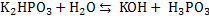 первой ступенью диссоциации является ионное уравнение:
первой ступенью диссоциации является ионное уравнение:
5. Водный раствор ляписа имеет _____ среду.
6. Водный раствор ацетата свинца имеет _____ среду.
7. pH 0,1 н раствора NaOH равен:
8. Раствор столового уксуса имеет pH = 3. Концентрации гидроксид - ионов и катионов водорода равны:
9. Водный раствор поташа имеет ______ среду.
10. Для 0,1 М раствора нитрита натрия, при рК = 3,16, характерна ________ среда.
11. Для понижения кислотности почвы можно использовать следующие вещества:
12. Для повышения кислотности почвы можно использовать следующие вещества:
14. При попадании щелочей на кожу, можно использовать для нейтрализации растворы солей:
15. Водный раствор гипосульфита натрия имеет ______ среду.
16. Водный раствор поваренной соли имеет ________ среду.
17. Водный раствор железного купороса имеет _________ среду.
18. Водный раствор чилийской селитры имеет _________ среду.
19. Чтобы ослабить или прекратить гидролиз трехвалентного хлорида железа, необходимо добавить:
20. Усилить гидролиз соли хлорида алюминия можно добавлением к раствору:
21. рН раствора ацетата аммония при рК кислоты = 4,73 и рК основания = 4,75 соответствует:
22. рН для 1 М раствора ацетата калия при рК кислоты = 4,74 соответствует:
23. [H+]в биологической жидкости равна 10-5 моль/л. Тогда [OH-] составляет:
24. pH 0,1 М раствора гидроксида калия будет:
25. Верхняя граница кислотности биологической жидкости (pH = 6).Тогда концентрация [OH-] равна ____ моль/л:
26. pH желудочного сока равен 3. Концентрация ионов водорода будет равна_____ моль/л:
27. Кислая среда характеризуется величиной pH:
28. pH 0,01 н раствора полностью диссоциированой соляной кислоты равен:
29. [H+] в растворе 0,001 моль/л. pH раствора будет:
30. Если pOH = 5,то среда ____.
31. pH 0,05 М раствора гидроксида кальция равен:
32. Окраска лакмуса в растворе pH которого равен 6:
33. pH 0,001 М раствора гидроксида лития:
34. Цвет фенолфталеина при pH = 4:
35. Цвет метилового оранжевого при pH раствора равным трём будет:
36. Индикатор метиловый оранжевый имеет область перехода pH:
37. Индикатор лакмус имеет область перехода pH:
38. Реакция среды при [ OH- ] = 10-8 будет:
39. Чем меньше значение рН, тем_____ концентрация катионов водорода.
40. Чем выше щелочность раствора, тем______ значение рН.
41. Гидролиз солей по катиону уменьшается в ряду:
42. Степень гидролиза по аниону увеличивается в ряду:
43. Для соли, образованной слабым основанием, сильной кислотой рН определяется по формуле:
44. При гидролизе по аниону, рН раствора определяется по формуле:
Тема: Строение атома.
1. Октет электронов на внешнем энергетическом уровне имеет:
2. Главное квантовое число равно 2, тогда магнитное будет:
3. Если n = 3, то l будет равно:
4. Строение внешнего слоя элемента 4s2 4p1, что соответствует атому:
5. Максимальное число электронов, которые могут заполнять 3d – орбиталь равно:
6. Наибольшее число электронов, которое может быть на 5р подуровне равно:
7. Максимальное число электронов на f подуровне будет:
д) 12
8. Число неспаренных электронов у иона Co 3+ равно:
9. Одинаковую электронную конфигурацию с атомом аргона имеет:
10. Одинаковое число протонов и нейтронов имеет атом:
11. Число электронов у иона Fe 3+ будет равно:
12.Частицей, имеющей больше протонов чем электронов, является:
13. Массовое число изотопа равно:
14. Число валентных электронов элемента с порядковым номером 12 равно:
15. Электронную конфигурацию инертного газа имеет:
16. Частица, имеющая в своем составе 18 электронов, 16 протонов, обладает зарядом равным:
17. Электронная конфигурация элемента 1s2 2s2 2p6 3s2 3p5, что соответствует атому:
18. Валентные электроны атома сурьмы находятся на орбиталях:
19. При радиоактивном излучении наибольшим проникающим эффектом обладают:
20. Гамма излучение представляет собой поток:
21. Число, характеризующее размер атомной орбитали и энергию электрона:
22. Атомы различных химических элементов, имеющих одинаковую массу, называются:
23. Ориентацию электронного облака в пространстве характеризует:
24. Квантовое число, определяющее собственное вращение электрона вокруг своей оси:
25. Если побочное квантовое число равно нулю, то магнитное будет:
26. Изобары – это:
27. Максимальное число электронов на энергетическом уровне можно определить по формуле ____.
28. Максимальное число электронов на энергетическом подуровне определяется формулой _____.
29. Атомы одного химического элемента, имеющие разную массу называются _____.
30. Атомы различных химических элементов, имеющие равное число нейтронов называются____.
31. Статическую модель строения атома предложил в 1903 г_____.
32. Планетарная модель строения атома была предложена ______.
33. Индивидуальной характеристикой химического элемента является ____ ядра.
34. Число нейтронов у трития равно _____.
35. Энергию электрона характеризуют квантовые числа:
36. Элемент с порядковым номером 29 может иметь валентности:
37. Наивысшая валентность марганца равна ____.
38. Электронным аналогом кремния будет атом:
39. В ядре изотопа водорода, входящего в состав живой воды, содержится число нейтронов:
40. В состав сверхтяжелой воды входит изотоп водорода, содержащий _____ нейтрона.
41. Главное квантовое число равно 2. Электронная формула для этого энергетического уровня:
42. Побочное квантовое число равно 3. Электронная формула для этого энергетического уровня:
43. Строение электронного внешнего слоя элемента выражается формулой 4s24p1. Это элемент ____.
44. Внешний электронный слой элемента выражается формулой 5s25p3. Это элемент под номером ____.
45. Внешний электронный слой элемента имеет формулу 4s23d5. Это элемент: ____.
46. Число электронов на внешнем уровне у химических элементов увеличивается в ряду:
47. Радиусы атомов химических элементов возрастают в порядке:
48. Атому аргона в основном состоянии соответствует электронная конфигурация:
49. Атомную кристаллическую решетку имеет:
50. В порядке усиления металлических свойств простые вещества расположены в ряду:
51. В порядке возрастания атомного радиуса расположены элементы:
Тема: Химическая связь.
1. Примером неполярной молекулы является:
2. Полярная ковалентная связь находится в молекуле:
3. Соединение, имеющее одновременно ионную и ковалентную связи, является:
4. Наиболее ярко выраженный характер ионной связи имеется в паре:
5. π - ковалентную связь образуют перекрытия электронных облаков:
6. В молекуле силана гибридизация:
7. Молекула аммиака имеет форму:
8. Форма молекулы бромида бериллия:
9. В молекуле воды имеет место гибридизация:
д) sp2d3
10. В молекуле сульфата калия имеются связи:
11. Донорно – акцепторная ковалентная связь присутствует в:
12. Водородная связь образуется при помощи:
13. Ионная связь образуется за счет:
14. Угол в молекуле хлорида бериллия составляет:
15. В молекуле углекислого газа угол между связями равен:
16. Металлическая связь образуется за счет:
17. Образование π – связи возникает при:
18. В молекуле атмосферного азота присутствует связь:
19. Молекула водорода образуется по реакции гидрида натрия и соляной кислоты, при этом наблюдается механизм образования ковалентной связи:
20. Между атомами с порядковым номером 35 образуется связь:
21. В катионе аммония имеются связи:
22. По определению Л. Полинга: «Двухэлектронная, двухцентровая связь называется ____.
23. Связь между атомом цезия и элементом с порядковым номером 53 является _____.
24. Расстояние между центрами ядер характеризует такое свойство связи как ______.
25. Способность атомов образовывать ограниченное число ковалентных связей называется ____.
26. Количество энергии необходимое для разрыва связи определяется ____.
27. Пространственную структуру молекул, их геометрическую форму обуславливает ____связи.
28. Угол в молекуле углекислого газа составляет 180o, при этом гибдридизация атомных орбиталей углерода будет _____.
29. Значения дипольных моментов увеличиваются в порядке:
30. Длина ковалентной связи увеличивается в порядке:
31. Кратная связь присутствует в молекулах веществ:
32. Наибольшей энергией связи обладает молекула:
33. В соединении NH4Cl имеются виды связи:
34. В соединении CuCl2 имеется ____ связь.
35. В молекуле ВCl3 _____ гибридизация.
36. Угол между электронными облаками в молекулах уменьшается в ряду:
37. Межмолекулярной и внутримолекулярной является _______ связь.
38. В молекуле ВеН2 гибридизация:
39. Гибридизация в молекуле СН4 будет:






