Биохимический показатель обеспеченности витамином – концентрация витамина или его метаболита (коферментной формы) в биологических жидкостях, величина экскреции с мочой, активность витаминзависимых ферментов и др.
Критерий адекватной обеспеченности витамином (нижняя граница нормы) – конкретная величина каждого показателя, относительно которой оценивают обеспеченность организма витамином.
Для количественного определения витаминов используют методы:
1. Физико-химические методы определения содержания витаминов как химических веществ (нг, мкг, мг).
2. Микробиологические методы – по скорости роста микроорганизмов в присутствии витамина судят об его количестве.
3. Биологические методы – определяют минимальное количество пищи или лекарственного препарата, способное предохранить животное (находящееся на диете, в которой отсутствует изучаемый витамин) от заболевания. Это количество пищи или витаминного препарата принимают за витаминную единицу.
Эффективность витаминизации оценивают, определяя показатели витаминной обеспеченности до и после приема витаминов.
Жирорастворимые витамины
К жирорастворимым витаминам относят витамины А, Д, Е, К.
Витамин А (ретинол, антиксерофтальмический)
1. Структура. Витамин А является полиизопреноидом, содержащим циклогексенильное кольцо. В группу витамина А входят ретинол, ретиналь и ретиноевая кислота. Только ретинол обладает полной функцией витамина А. Термин «ретиноиды» включает природные и синтетические формы ретинола. Растительный предшественник β-каротин обладает 1/6 активности витамина А.
2. Транспорт и метаболизм. Эфиры ретинола растворяются в жирах пищи, эмульгируются желчными кислотами и всасываются кишечным эпителием. Всосавшийся b-каротин расщепляется на две молекулы ретиналя. В клетках эпителия ретиналь восстанавливается в ретинол и небольшая часть ретиналя окисляется в ретиноевую кислоту. Большая часть ретинола эстерифицируется насыщенными жирными кислотами и в составе хиломикронов поступает через лимфу в кровь. После липолитической трансформации ремнанты хиломикронов захватываются печенью. В печени витамин А запасается в виде эфиров. Для транспорта к периферическим тканям эфиры ретинола гидролизуются и свободный ретинол связывается в сыворотке крови с плазменным ретинолсвязывающим протеином (ПРСП). Ретиноевая кислота транспортируется альбуминами. Внутри периферических клеток ретинол связывается с клеточным ретинолсвязывающим протеином (КРСП). Токсическое действие витамина А проявляется при появлении свободной формы витамина, т.е. после исчерпания мощности КРСП. Ретинол и ретиналь взаимопревращаются друг в друга с помощью НАДФ-зависимых дегидрогеназ или редуктаз. Ретиноевая кислота не может превращаться в ретинол или ретиналь, поэтому ретиноевая кислота может поддерживать рост и дифференцировку тканей, но не может заменить ретиналь в зрении или ретинол в функционировании репродуктивных органов.
 |
Ретинол
 |
Ретиналь
 |
Ретиноевая кислота
3. Биологическая роль.
3.1. Ретинол действует подобно гормонам, проникающим в клетку, – связывается с ядерными белками и регулирует экспрессию определенных генов. Ретинол необходим для осуществления нормальной репродуктивной функции.
3.2. Ретиналь участвует в акте зрения. 11-цис-ретиналь связан с белком опсином и образует родопсин. На свету родопсин диссоциирует и цис-ретиналь переходит в транс-ретиналь. Реакция сопровождается конформационными изменениями мембран палочек и открытием кальциевых каналов. Быстрый вход ионов кальция инициирует нервный импульс, который передается в зрительный анализатор. Для повторного восприятия (т.е. в темноте) транс-ретиналь восстанавливается алкогольдегидрогеназой в транс-ретинол (здесь возможны потери витамина А). Транс-ретинол изомеризуется в цис-ретинол (здесь возможно восполнение убыли витамина А). Цис-ретинол окисляется в цис-ретиналь, который, соединяясь с опсином, образует родопсин. Система светоощущения готова к восприятию следующего кванта света.
3.3. Ретиноевая кислота участвует в синтезе гликопротеинов, усиливает рост и дифференцировку тканей.
3.4. Ретиноиды обладают антиопухолеввой активностью и ослабляют действие канцерогенов.
3.5. b-каротин – антиоксидант и способен обезвреживать пероксидные свободные радикалы (ROO·) в тканях с низким парциальным давлением кислорода.
4. Источники. Витамин А содержится только в продуктах животного происхождения (печень, почки, сливочное масло, рыбий жир). Из печени пресноводных рыб выделен витамин А2, который отличается наличием еще одной двойной связи в 3-4 положении и называется 3-дегидроретинол. Биологическая активность витамина А2 для млекопитающих соответствует примерно 40% активности витамина А1. В растениях есть пигменты – a-, b- и g-каротины, которые могут превращаться в витамин А (морковь, томаты).
5. Суточная потребность. 1-2,5 мг витамина А (5000-7000 МЕ). 1 МЕ = 0,344 мкг ретинолацетата. Частично потребность в витамине А может покрываться за счет каротина (2-5 мг), причем 1 мг каротина = 0,67 мг ретинола.
6. Гиповитаминоз. Проявляется в виде нарушения зрения при слабом освещении -куриной слепоты – гемералопия. Это наиболее ранний признак недостаточности витамина А: человек нормально видит при дневном освещении и очень плохо различает предметы при скудном освещении (в сумерках). Авитаминоз характеризуется падением массы тела, остановкой роста, пролиферацией и ороговеванием эпителия, сухости кожи и слизистых, слущиванием эпителия, нарушением репродуктивной функции. Сухость роговицы глаза называется ксерофтальмия (отсюда название витамина – антиксерофтальмический). Повреждение эпителия мочевых путей, кишечника приводит к развитию воспалительных заболеваний. Важнейшей причиной недостаточности витамина А являются нарушения всасывания и транспорта липидов. При введении высоких доз витамина А развивается гипервитаминоз А.
Витамин D (кальциферол, антирахитический)
1. Структура. В растительных продуктах содержится эргостерол, который при действии ультрафиолетовых лучей превращается в витамин D2 (эргокальциферол). В животных тканях распространен 7-дегидрохолестерол, который в коже при облучении ультрафиолетовыми лучами превращается в витамин D 3 (холекальциферол) (рис. 27.1).
2. Метаболизм. Витамин D пищи всасывается в составе мицелл. В крови транспортируется в связи со специфическим транспортным глобулином. В гепатоцитах гидроксилируется в 25-гидроксихолекальциферол (25-ОН- D 3). Это главная резервная в печени и транспортная в крови форма витамина D. Часть 25-ОН-D3 участвует в энтеро-печеночной циркуляции (как желчные кислоты). При ее нарушении может возникать дефицит витамина D. В почках, плаценте и костях 25-ОН- D3 может гидроксилироваться в положении 1 с образованием 1,25-дигидроксихолекальциферола или кальцитриола. Продукция кальцитриола регулируется собственной концентрацией, паратгормоном и сывороточными фосфатами.
3. Биологическая роль. Кальцитриол функционирует подобно проникающим гормонам. Кальцитриол – единственный регулятор перемещения кальция через мембрану энтероцитов против градиента концентрации. Кальцитриол стимулирует биосинтез в энтероцитах кальций-связывающего белка, что обеспечивает всасывание кальция и фосфатов в тонком кишечнике. Витамин D3 усиливает реабсорбцию фосфатов в почечных канальцах, что способствует поддержанию нормального соотношения Са2+ и НРО43- в плазме и внеклеточных жидкостях. Это необходимо для кальцификации молодой растущей костной ткани.

Рис. 10.1. Схема образования витамина D и его активной формы кальцитриола.
Подписи: 7-Дегидрохолестерол; Ультрафиолетовые лучи; Провитамин D3; Витамин D3 (Холекальциферол); Кальцитриол (1,25-дигидроксихолекальциферол)
4. Источники: рыбий жир, печень рыб и животных, сливочное масло, яичный желток, молоко.
5. Суточная потребность. Потребность в витамине D зависит от возраста и состояния организма и составляет 12-25 мкг (500-1000 МЕ) в сутки (1 мкг=40 МЕ).
6. Гиповитаминоз. При недостатке витамина D у детей развивается заболевание рахит: нарушение минерализации костей, позднее развитие зубов, гипотония мышц. При недостатке витамина D у взрослых развивается остеопороз. Для профилактики D-гиповитаминоза используют ультрафиолетовое облучение кожи и пищи. При передозировке витамина D (в дозах, превышающих лечебные в 2-3 тысячи раз 1 500 000 МЕ) развивается гипервитаминоз: у детей остановка роста, рвота, исхудание, повышение артериального давления, возбуждение с переходом в ступор. В основе – гиперкальциемия и кальцификация внутренних оранов.
Витамин Е (токоферол, антистерильный)
1. Структура. К витамину Е относится группа соединений – производных токола, обладающих витаминной активностью. Известно 8 видов токоферолов – α, β, γ, δ и т.д. Наибольшей активностью обладает a-токоферол (5,7,8-триметилтокол).

2. Транспорт и метаболизм. Витамин Е не метаболизируется в организме. Нарушение всасывания липидов может приводить к дефициту токоферола, поскольку токоферол растворяется в жирах пищи, высвобождается и всасывается во время их переваривания. Токоферол всасывается в кишечнике и в составе хиломикронов через лимфу поступает в кровь. Токоферол попадает в ткани, в капиллярах которых хиломикроны подвергались действию липопротеинлипазы, а в печень витамин Е поступает в составе ремнантов хиломикронов. Токоферол транспортируется из печени к периферическим тканям в составе ЛПОНП. Депонируется витамин в жировой ткани, печени и мышцах.
3. Биологическая роль.
3.1. Витамин Е накапливается в мембранах клеток и действует как антиоксидант, прерывая цепи свободно-радикальных реакций. Антистерильный эффект связан с антиоксидантным действием витамина Е, когда он, препятствуя пероксидному повреждению мембран, обеспечивает нормальный контакт между клетками (предотвращает преждевременное отделение сперматогоний при созревании сперматозоидов или обеспечивает имплантацию оплодотворенной яйцеклетки в слизистую матки).
В отличие от других витаминов, витамин Е повторно не используется и после своего действия должен заменяться новыми молекулами токоферола.
Антиоксидантное действие токоферола эффективно при высокой концентрации кислорода, поэтому он находится в мембранах клеток с высоким парциальным давлением кислорода (мембраны эритроцитов, клеток респираторных органов). Потребность в витамине Е повышается при увеличении потребления ненасыщенных жирных кислот.
3.2. Витамин Е и селен (Se) действуют как синергисты. Se входит в состав глютатионпероксидазы, которая обеспечивает обезвреживание пероксидных радикалов. Se необходим для нормального функционирования поджелудочной железы. При нарушении ее функции нарушается переваривание и всасывание липидов и вторично витамина Е.
3.3. Витамин Е может участвовать в функционировании SH-содержащих ферментов, влиять на биосинтез КоQ, участвовать в механизмах переноса электронов по дыхательной цепи митохондрий
4. Источником витамина Е для человека являются растительные масла, а также зерновые продукты, ягоды шиповника, салат, капуста.
5. Суточная потребность. 20-30 мг.
6. Дефицит витамина Е. При дефиците витамина Е нарушается образование сперматозоидов у мужчин и развитие плода у женщин. Отмечаются дегенеративные изменения клеток репродуктивных органов, мышечная дистрофия, дегенеративные изменения клеток спинного мозга, жировое перерождение печени, дислипопротеинемии. У новорожденных может развиваться анемия, поэтому витамин Е необходимо добавлять к пище беременных и кормящих грудным молоком женщин. Анемия развивается из-за уменьшения продукции гемоглобина и сокращения продолжительности жизни эритроцитов. При нарушении переваривания и всасывания липидов развивается гиповитаминоз Е, ведущий к неврологическим заболеваниям.
Витамин К (филлохинон, антигеморрагический)
1. Структура. Три соединения обладают биологической активностью витамина К. Витамин К1 (филлохинон) является производным 2-метил-1,4-нафтохинона, содержащий в положении 3 боковую цепь (фитол). Выделен из люцерны. Витамин К2 (менахинон) выделен из гниющей рыбной муки. Синтезируется кишечной микрофлорой. Отличается от витамина К1 строением боковой цепи, представленной фарнезилдигеранилом. Витамин К3 (менадион, синтетический) не имеет боковой цепи в положении 3. На его основе А.Б.Палладин синтезировал водорастворимый препарат викасол (натриевая соль бисульфитного производного 2-метил-1,4-нафтохинона).
2. Транспорт и метаболизм. Для всасывания природных витаминов группы К (нафтахинонов) требуются желчные кислоты. В кровь они поступают в составе хиломикронов через лимфу. Викасол может всасываться без желчных кислот и прямо поступает в воротную вену и печень. Витамин К вначале аккумулируется в печени, но быстро расходуется.

3. Биологическая роль.
3.1. Витамин К стимулирует биосинтез в печени четырех белковых факторов свертывания крови (II-протромбин; VII-проконвертин; IX-фактор Кристмаса, или антигемофильный глобулин В; Х-фактор Стюарта-Прауэра).
3.2. Витамин К действует как кофактор карбоксилазы на этапе посттрансляционной модификации глутаминовых остатков протромбина. Протромбин содержит 10 таких остатков, которые карбоксилируются витамин К-зависимой карбоксилазой. Образуется γ-карбоксиглутамат, который затем хелатируется кальцием, что важно для свертывания крови.
3.3. Реакция карбоксилирования требует СО2 и восстановленной (гидрохиноидной) формы витамина К. В эндоплазматическом ретикулуме есть цикл восстановления продукта карбоксилазной реакции витамина К (т.е. хиноидной формы в гидрохиноидную). Центральное место занимают две редуктазные реакции (в первой используются дитиоловый восстановитель, во второй – НАДФ-зависимая редуктаза).
3.4. Описано участие витамина К в окислительном фосфорилировании, его многостороннее анаболическое действие, функционирование в составе мембран.
5. Основной источник витамина К – микрофлора кишечника. Возможно поступление нафтохинонов с пищей (шпинат, тыква, капуста, ягоды рябины, печень животных).
6. Суточная потребность. Суточная потребность условно выражается 0,2-0,3 мг.
7. Дефицит витамина К. При нормальной микрофлоре кишечника у взрослых дефицита витамина К не бывает. Основная причина гиповитаминоза К – это стерилизация кишечника антибиотиками и сульфаниламидными препаратами. У новорожденных возможен дефицит витамина К, так как плацента его не пропускает, а кишечник стерилен. После родов содержание витамина К в плазме падает, но после еды восстанавливается. Если уровень протромбина низкий, возможно развитие геморрагического синдрома. Гиповитаминоз К бывает при мальабсорбции, дисфункции гепато-билиарной и панкреатической систем, при атрофии слизистой кишечника. Основные проявления гиповитаминоза К связаны с нарушением внутрисосудистого свертывания крови и кровоточивостью.
Водорастворимые витамины
К водорастворимым витаминам относят витамины группы В, С, Р, Н.
н С (аскорбиновая кислота, антискорбутный витамин)
1. Структура. Витамин С по структуре представляет собой g-лактон, имеющий 2 ассиметричных атома углерода. Биологически активной является L-форма аскорбиновой кислоты.

Аскорбиновая кислота Дегидроаскорбиновая кислота
Кислые свойства аскорбиновой кислоты обусловлены наличием 2-х енольных гидроксильных групп. L-аскорбиновая кислота обратимо подвергается окислению с образованием дегидроаскорбиновой кислоты под действием фермента аскорбатоксидазы. Восстановление дегидроаскорбиновой кислоты в аскорбиновую осуществляется с участием редуктазы и восстановленного глутатиона. Аскорбиновая и дегидроаскорбиновая кислоты являются биологически активными формами витамина. При гидратации в присутствии кислорода дегидроаскорбиновая кислота необратимо окисляется в 2,3-дикетогулоновую кислоту, которая не обладает биологической активностью и распадается до щавелевой и треоновой кислот. Скорость разрушения витамина возрастает с повышением температуры, в щелочной среде, под действием УФ-лучей, в присутствии солей тяжелых металлов (например, меди). Аскорбиновая кислота разрушается в процессе приготовления пищи и хранения продуктов.
2. Метаболизм. Аскорбиновая кислота всасывается путем простой диффузии на всем протяжении желудочно-кишечного тракта, но преимущественно в тонком кишечнике. В организме не накапливается.
3. Биологическая роль.
3.1. Окислительно-восстановительные реакции. Аскорбиновая кислота является сильным восстановителем с окислительно-восстановительным потенциалом +0,08 В и участвует в восстановлении молекулярного кислорода, нитратов и цитохромов а и с.
3.2.Витамин С участвует в гидроксилировании остатков пролина и лизина в процессе биосинтеза коллагена. ОН-группы гидроксипролина необходимы для стабилизации структуры коллагена, формируя водородные связи между цепями триплетной спирали зрелого коллагена. Гидроксилизин в коллагене служит для образования участков связывания с полисахаридами. Витамин С необходим для формирования костной ткани, поскольку основными компонентами костной ткани являются органический матрикс, коллаген, неорганический кальций и фосфаты.
3.3.Витамин С участвует в метаболизме тирозина. При синтезе катехоламинов норадреналина и адреналина из тирозина в надпочечниках и центральной нервной системе происходит окисление Cu+ в Cu2+; для обратного процесса восстановления меди необходима аскорбиновая кислота. Кроме того, аскорбиновая кислота требуется для окисления p-гидроксифенилпирувата в гомогентизиновую кислоту.
3.4.Витамин С необходим для гидроксилирования триптофана в гидрокситриптофан при биосинтезе серотонина.
3.5. Витамин С участвует в биосинтезе желчных кислот из холестерола.
3.6. Синтез кортикостероидных гормонов. В коре надпочечников содержится высокая концентрация витамина С, особенно в период стресса. Предполагают, что витамин С необходим для синтеза кортикостероидов.
3.7. Метаболизм железа и гемоглобина. Аскорбиновая кислота повышает всасывание железа из кишечника путем его восстановления в Fe2+. Витамин С участвует в образовании ферритина и высвобождении железа из связи его с транспортным белком крови трансферрином. Витамин С способствует восстановлению метгемоглобина в гемоглобин и участвует в деградации гемоглобина до желчных пигментов.
3.8. Метаболизм фолиевой кислоты. Активной формой фолиевой кислоты является тетрагидрофолиевая кислота (ТГФК). Витамин С необходим для образования ТГФК. Вместе с ТГФК аскорбиновая кислота участвует в созревании эритроцитов.
3.9. Витамин С является водорастворимым антиоксидантом и защищает клетки от повреждения свободными радикалами. Антиоксидантная функция аскорбиновой кислоты объясняется ее способностью легко отдавать два атома водорода, используемых в реакциях обезвреживания свободных радикалов.
4. Источники. В организме человека, обезьян, морских свинок и некоторых птиц витамин С не синтезируется. Источником витамина С служит растительная пища. Особенно им богаты перец, черная смородина, укроп, петрушка, капуста, щавель, цитрусовые, земляника.
5. Суточная потребность 70-120 мг.
6. Гиповитаминоз. Проявляется повышенным утомлением, снижением аппетита, сниженной устойчивостью к простудным заболеваниям, кровоточивостью десен. Авитаминоз приводит к заболеванию цингой (скорбутом). Главными симптомами цинги являются нарушение проницаемости капилляров, обусловленное недостаточностью гидроксилирования пролина и лизина в коллагене, расшатывание и выпадение зубов, отеки и боли в суставах, поражение костей, нарушение заживления ран. Смерть обычно наступает от кровоизлияния в полость перикарда. При гиповитамизозе С развивается железодефицитная анемия из-за нарушения всасывания железа и использования его запасов при синтезе гемоглобина.
Витамин В1 (тиамин, антиневритный витамин)
1. Структура. Витамин В1 был первым витамином, выделенным в кристаллическом виде К.Функом в 1912 г. Позже был осуществлен его химический синтез. Свое название – тиамин – получил из-за наличия в составе его молекулы атома серы и аминогруппы. Тиамин состоит из 2-х гетероциклических колец – аминопиримидинового и тиазолового. Последнее содержит каталитически активную функциональную группу – карбанион (относительно кислый углерод между серой и азотом).

Тиамин устойчив в кислой среде и выдерживает нагревание до высокой температуры. В щелочной среде витамин быстро разрушается.
2. Транспорт и метаболизм. В желудочно-кишечном тракте различные формы витамина гидролизуются с образованием свободного тиамина. Большая часть тиамина всасывается в тонком кишечнике с помощью специального механизма активного транспорта, остальное количество расщепляется тиаминазой кишечных бактерий. С током крови всосавшийся тиамин попадает вначале в печень, где фосфорилируется, а затем переносится в другие органы и ткани.
тиаминпирофосфаткиназа
 АТФ + тиамин тиаминпирофосфат + АМФ
АТФ + тиамин тиаминпирофосфат + АМФ
Витамин В1 присутствует в различных органах и тканях как в форме свободного тиамина, так и его фосфорных эфиров: тиаминмонофосфата, тиаминдифосфата и тиаминтрифосфата. Основной коферментной формой (60-80% от общего внутриклеточного) является тиаминдифосфат, или тиаминпирофосфат (ТДФ, или ТПФ). Роль тиаминмонофосфата и тиаминтрифосфата пока неизвестна. Возможно они и аденилированная форма тиаминтрифосфата участвуют в реакциях приспособительного характера, путем переключения метаболических потоков углеводов.
После распада коферментов свободный тиамин выделяется с мочой и определяется в виде тиохрома.
3. Биологическая роль
3.1. ТПФ является коферментом 3-х полиферментных комплексов, которые катализируют окислительное декарбоксилирование кетокислот:
- Пируватдегидрогеназный комплекс участвует в окислительном декарбоксилировании пирувата, что является одной из ключевых реакций в обмене углеводов. В результате этой реакции образуется ацетил-КоА, который включается в цикл трикарбоновых кислот, где окисляется до углекислоты и воды. Благодаря этой реакции создаются условия для полного окисления углеводов и утилизации всей заключенной в них энергии. Кроме того, образующийся ацетил-КоА служит источником для синтеза многих биологических продуктов: жирных кислот, холестерола, стероидных гормонов, кетоновых тел и т.д.
- 2 -Оксоглуторатдегидрогеназный комплекс входит в состав ЦТК и катализирует окислительное декарбоксилирование 2-оксоглутарата с образованием сукцинил-КоА.
- Дегидрогеназа кетокислот с разветвленным углеродным радикалом участвует в метаболизме валина, изолейцина и лейцина.
3.2. ТПФ является коферментом транскетолазы – фермента пентозофосфатного пути окисления углеводов, основными продуктами которого являются НАДФН и рибоза.
3.3. Витамин В1 принимает участие в синтезе ацетилхолина, катализируя в пируватдегидрогеназной реакции образование ацетил-КоА.
4. Источники. Довольно много витамина содержится в пшеничном хлебе из муки грубого помола, в оболочке семян хлебных злаков, в сое, фасоли, горохе, дрожжах. Из продуктов животного происхождения наиболее богаты тиамином печень, нежирная свинина, почки, мозг, яичный желток.
5. Суточная потребность составляет 2-3 мг.
6. Гиповитаминоз. Проявляется слабостью, снижением аппетита, тошнотой, нарушением периферической чувствительности, онемением пальцев, ощущением ползанья «мурашек», болями по ходу нервов. При авитаминозе развивается заболевание бери-бери, что в переводе с индийского означает овца, так как походка больного человека напоминает поступь овцы. У больных бери-бери концентрации пирувата и 2-оксоглутарата в крови выше, чем в норме. Низкая активность транскетолазы в эритроцитах является лабораторным критерием бери-бери. Характерно поражение сердечно-сосудистой и нервной систем. Особая чувствительность нервной ткани к недостатку тиамина объясняется тем, что коферментная форма этого витамина необходима нервным клеткам для усвоения глюкозы.
Витамин В2 (рибофлавин)
1. Структура. Витамин В2 отличается от других витаминов желтым цветом (flavus – желтый). Рибофлавин впервые был выделен из кисломолочной сыворотки. Молекула рибофлавина состоит из гетероциклического изоаллоксазинового ядра, к которому в 9-м положении присоединен спирт рибитол (производное D-рибозы). Термином флавины обозначаются многие производные изоаллоксазина, обладающие В2-витаминной активностью.
Биосинтез флавинов осуществляется растительными и многими бактериальными клетками, а также плесневыми грибками и дрожжами. Благодаря микробному биосинтезу рибофлавина в желудочно-кишечном тракте жвачные животные не нуждаются в этом витамине. У других животных и человека синтезированных в кишечнике флавинов недостаточно для предупреждения гиповитаминозов. Витамин В2 хорошо растворим в воде, устойчив в кислой среде, но легко разрушается в нейтральной и щелочной, а также под действием видимого и УФ-света. Витамин В2 легко подвергается обратимому восстановлению, присоединяя водород по месту двойных связей (1 и 10), превращаясь из оранжево-желтого раствора в бесцветную лейкоформу.
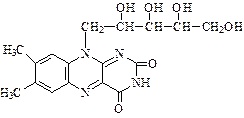
2. Метаболизм. В пище витамин В2 находится преимущественно в составе своих коферментных форм, связанных с белками – флавопротеинов. Под влиянием пищеварительных ферментов витамин высвобождается и всасывается путем простой диффузии в тонком кишечнике. В клетках слизистой кишечника, крови, печени и других тканях рибофлавин фосфорилируется до флавинмононуклеотида (ФМН) и флавинадениндинуклеотида (ФАД).
3. Биологическая роль. Основное значение витамина В2 состоит в том, что он входит в состав флавиновых коферментов – ФМН и ФАД. Различают два типа реакций, катализируемых флавопротеинами:
3.1. Простые дыхательные системы – это прямое окисление субстрата с участием кислорода, перенос на него атомов водорода с образованием Н2О2 и выделением энергии в виде тепла: оксидазы L- и D-аминокислот, ксантиноксидаза (разрушение пуриновых азотистых оснований), альдегиддегидрогеназа (деградация альдегидов).
3.2. Участие в сложных дыхательных системах
- ФАД во втором комплексе цепи переноса электронов во внутренней мембране митохондрий (сукцинатдегидрогеназа и ацил-КоА-дегидрогеназа - дегидрирование метаболита ЦТК сукцината и ацил-КоА при окислении жирных кислот);
- НАДН-дегидрогеназа (перенос протонов и электронов от НАДН+Н+ матрикса на ФМН первого комплекса цепи переноса электронов во внутренней мембране митохондрий);
- дигидролипоилдегидрогеназа (ФАД – кофактор фермента окислительного декарбоксилирования α-кетокислот пирувата и 2-оксоглутарата).
4. Источники. Основными источниками рибофлавина являются печень, почки, желток куриного яйца, творог. В кислом молоке витамина содержится больше, чем в свежем. В растительных продуктах витамина В2 мало (исключение – миндальные орехи). Частично дефицит рибофлавина восполняется кишечной микрофлорой.
5. Суточная потребность 2-3 мг.
6. Гиповитаминоз. Недостаток витамина В2, как и других витаминов, проявляется слабостью, повышенной утомляемостью, склонностью к простудным заболеваниям. К специфическим проявлениям недостаточности рибофлавина относятся воспалительные процессы в слизистых оболочках. Слизистая губ и полости рта становится сухой, язык приобретает ярко-красный цвет, в углах рта появляются трещины. Отмечается повышенное шелушение эпителия кожи, особенно на лице.
Витамин РР (никотиновая кислота, никотинамид, ниацин; антипеллагрический витамин)
1. Структура. Витамин РР выделен К.Эвельгеймом в 1937 г. Его введение предохраняло от заболевания пеллагра или излечивало ее. РР означает противопеллагрический (preventive pellagra).
Никотиновая кислота является пиридин-3-карбоновой кислотой, никотинамид – ее амидом. Оба соединения в организме легко превращаются друг в друга и поэтому обладают одинаковой витаминной активностью.

Витамин РР плохо растворим в воде, но хорошо в водных растворах щелочей.
2. Метаболизм. Поступающий с пищей витамин РР быстро всасывается в желудке и кишечнике в основном путем простой диффузии. С током крови никотиновая кислота попадает в печень и другие органы, несколько медленнее проникает в них никотинамид. В тканях оба соединения преимущественно используются для синтеза коферментных форм НАД+ и НАДФ+. Часть никотинамидных коферментов синтезируется в организме животных из триптофана. Однако этот путь, в который вовлекается до 2% метаболического пула триптофана, значительно уступает по эффективности первому (т.е. из прямого витаминного предшественника).
3. Биологическая роль. Значение витамина РР определяется ролью коферментов НАД+ и НАДФ+.
3.1. НАД+ входит в состав дегидрогеназ, катализирующих окисительно-востановительные превращения пирувата, изоцитрата, 2-оксоглутарата, малата и др. Эти реакции чаще локализованы в митохондриях и служат для освобождения энергии в сопряженных митохондриальных цепях переноса протонов и электронов.
3.2.НАДФ+ входит в состав дегидрогеназ (редуктаз), которые чаще локализованы в цитозоле или эндоплазматическом ретикулуме и служат для восстановительных синтезов (НАДФ-зависимые дегидрогеназы пентозофосфатного пути, синтеза жирных кислот и холестерола, митохондриальные монооксигеназные системы для синтеза желчных кислот, кортикостероидных гормонов) и обезвреживания ксенобиотиков (микросомальное окисление, оксигеназы со смешанной функцией).
3.3. НАД+ и НАДФ+ - аллостерические регуляторы ферментов энергетического обмена.
4. Источники. Продукты животного (печень, мясо) и растительного происхождения (рис, хлеб, картофель). Молоко и яйца содержат следы ниацина, но в них содержится триптофан, что может компенсировать недостаточное поступление никотинамида с пищей.
5. Суточная потребность составляет 15-25 мг.
6. Гиповитаминоз. Характерным признаком недостаточности витамина РР является симптомокомплекс «три Д»: дерматит, диарея и деменция. В основе заболевания лежит нарушение пролиферативной активности и энергетики клеток. Дерматит чаще всего отмечается на открытых участках кожи, которая под действием солнечных лучей краснеет, покрывается пигментными пятнами (на лице в виде крыльев бабочки) и шелушится. Язык становится ярко-красным и болезненным, утолщается, на нем появляются трещины. Расстройство пищеварения проявляется тошнотой, отсутствием аппетита, болями в животе. Нарушается функция периферических нервов и центральной нервной системы.
Симптомы гиповитаминоза развиваются:
1. У лиц с недостатком белка в диете. Объясняется это тем, что животные белки содержат оптимальное количество аминокислоты триптофана, витамина В6 и некоторые другие компоненты, необходимые для синтеза ниацина.
2. При постоянном питании маисом, где ниацин находится в связанной форме.
3. При постоянном питании сорго, зерна которого содержат высокую концентрацию лейцина – ингибитора ключевого фермента превращения триптофана в НАД+.
4. При дефиците витамина В6 и его коферментной формы пиридоксальфосфата, необходимого для синтеза из триптофана коферментных форм витамина РР.
Пантотеновая кислота
Пантотеновая кислота широко распространена в природе, название от panthos – повсюду. Витамин открыт Р.Вильямсом в 1933 г., спустя десятилетие от уже был синтезирован химическим путем.
1. Структура. Пантотеновая кислота состоит из пантоевой кислоты (α,γ,-дигидрокси-β,β-диметилмасляная кислота) и β-аланина.

Пантотеновая кислота представляет собой вязкую светло-желтую жидкость, хорошо растворимую в воде. Она малоустойчива и легко гидролизуется по месту пептидной связи под действием слабых кислот и щелочей.
2. Метаболизм. Пантотеновая кислота с током крови поступает в ткани после всасывания на всем протяжении тонкого кишечника и в толстой кишке (в зависимости от концентрации путем простой диффузии или активного транспорта). Пантотеновая кислота фосфорилируется с использованием АТФ до 4’-фосфопантотената. Присоединение цистеина и его декарбоксилирование приводит к образованию тиоэтаноламина, из которого образуется 4’-фосфопантотеин – простетическая группа кофермента А (HS-КоА) и ацилпереносящего белка (АПБ).
3. Биологическая роль. Тиоловая группа в НS-КоА и АПБ действует как переносчик ацильных радикалов.
HS-КоА участвует в важнейших метаболических процессах:
а) в обмене углеводов – окислительное декарбоксилирование пирувата в ацетил-КоА и 2-оксоглутарата в сукцинил-КоА;
б) в β-окислении жирных кислот на этапах активации до образования ацил-КоА и тиолитическом расщеплении с выделением ацетил-КоА и укороченного на 2 углеродных атома ацил-КоА;
в) в форме ацетил-КоА переносится остаток ацетила на холин с образованием медиатора ацетилхолина;
г) сукцинил-КоА участвует в синтезе порфиринов;
д) в биосинтезе жирных кислот – функцию переносчика метаболитов в пальмитатсинтазном комплексе выполняет 4-фосфопантетеин;
ж) ацетил-КоА используется для синтеза кетоновых тел, холестерола и стероидных гормонов.
Ацетил-КоА занимает центральное место в процессах взаимосвязи обменов углеводов, аминокислот и жирных кислот.
4. Источники. Пантотеновая кислота широко распространена в продуктах животного (печень, почки, яйца, мясо, молоко и др.) и растительного (картофель, капуста, фрукты и др.) происхождения. Синтезируется кишечной микрофлорой.
5. Суточная потребность. 10-15 мг
6. Гиповитаминоз. В связи с широким распространением витамина в продуктах питания авитаминоз не встречается. Симптомы гиповитаминоза не специфичны: дерматиты, невриты, язвы слизистых пищеварительного тракта, нарушения продукции стероидных гормонов и др.
Витамин В6 (пиридоксин, пиридоксол, антидерматитный витамин)
1. Структура. Витамин В6 включает три природных производных пиридина, обладающих одинаковой витаминной активностью: пиридоксина, пиридоксаля, пиридоксамина, отличающихся друг от друга наличием соответственно спиртовой, альдегидной или аминогруппы. Витамин В6 открыт в 1934 г. А.Сент-Дьердьи. Пиридоксин хорошо растворяется в воде и этаноле, устойчив в кислой и щелочной среде, но легко разрушается под действием света при рН 7,0.
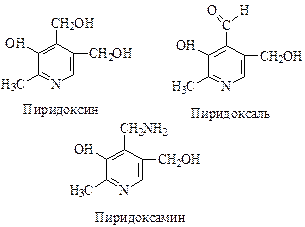
2 Метаболизм. Всосавшись в тонком кишечнике, все формы витамина с током крови разносятся к тканям и, проникая в клетки, фосфорилируются с участием АТФ. Коферментные функции выполняют два фосфорилированных производных пиридоксина: пиридоксальфосфат и пиридоксаминфосфат.
3. Биологическая роль. Витамин В6 характеризуется широким спектром биологического действия. Он принимает участие в регуляции белкового, углеводного и липидного обменов, биосинтезе гема и биогенных аминов, гормонов щитовидной железы и других биологически активных соединений. Коферментные формы витамина В6 входят в состав следующих ферментов:
- Аминотрансфераз аминокислот, катализирующих обратимый перенос NH2-группы от аминокислоты на α-кетокислоту (образование заменимых аминокислот, непрямое дезаминирование и восстановительное аминирование аминокислот).
- Декарбоксилаз аминокислот, отщепляющих карбоксильную группу аминокислот, что приводит к образованию биогенных аминов.
- Ферментов, осуществляющих неокислительное дезаминирование серина, треонина, триптофана, серусодержащих аминокислот.
- Мышечной фосфорилазы (распад гликогена).
4. Источники. Витамином В6 богаты бобовые, зерновые культуры, мясные продукты, рыба, картофель. Он синтезируется кишечной микрофлорой, частично покрывая потребность организма в этом витамине.
5. Суточная потребность. 2-3 мг
6. Гиповитаминоз. Основными проявлениями недостаточности витамина В6 являются гипохромная анемия и судороги. Отмечается развитие сухого себорейного дерматита, стоматита и глоссита. Чаще всего пиридоксиновая недостаточность наблюдается:
а) у маленьких детей при искусственном вскармливании стерилизованным молоком (разрушается витамин В6), у беременных при токсикозах;
б) при групповой недостаточности витаминов группы В;
в) при подавлении микрофлоры кишечника антибиотиками;
г) у алкоголиков, поскольку ацетальдегид стимулирует дефосфорилирование пиридоксальфосфата.
Витамин Н (биотин)
Биотин – это первое вещество, которое было определено как необходимый ростовой фактор для микроорганизмов. Позже было показано токсическое действие сырого яичного белка на крыс. Употребление печени или дрожжей снимало этот эффект. Фактор, предотвращающий развитие токсикоза, был назван витамином Н или биотином (от греч. bios – жизнь).
1.
 |
Структура. Молекула биотина состоит из имидазольного и тиофенового колец и боковой цепи, представленной остатком валериановой кислоты. В пище биотин представлен биоцитином, который высвобождается путем протеолиза.
2. Метаболизм
2.1. Биотин не модифицируется в организме, но ковалентно связывается с ферментами, в которых выполняет функцию простетической группы.
2.2. Биотин связывается через свободную карбоксильную группу с остатком лизина апофермента. Комплекс биотин-фермент взаимодействует с СО2 в присутствии АТФ (источник энергии) с образованием комплекса карбоксибиотин-фермент.
2.3. Биотинидаза катализирует удаление биотина от фермента во время метаболизма белков, что позволяет использовать биотин повторно.
3. Биологическая роль. Биотин действует как кофермент реакций карбоксилирования, в которых служит переносчиком СО2. В организме 4 фермента используют биотин как кофермент.
- Пируваткарбоксилаза. В результате карбоксилирования пирувата образуется оксалоацетат, который используется в глюконеогенезе и ЦТК.
- Ацетил-КоА-карбоксилаза катализирует карбоксилирование ацетил-КоА с образованием малонил-КоА. Реакция используется при биосинтезе высших жирных кислот.
- Пропионил-КоА-карбоксилаза превращает пропионил-КоА в D-метилмалонил-КоА, который превращается в сукцинат (вступает в ЦТК).
- β-метил-кротонил-КоА-карбоксилаза, участвующая в катаболизме лейцина и веществ, имеющих в составе изопреноидные структуры.
4. Источники. Биотин в достаточном количестве синтезируется микрофлорой кишечника. Пищевые источники: печень, сердце, яичный желток, отруби, бобы, соя, цветная капуста и др.
5. Суточная потребность. 150-200 мкг.
6. Дефицит. Причинами гиповитаминоза являются:
а)применение антибиотиков, которые подавляют рост кишечной микрофлоры;
б) поступление в организм большого количества авидина – гликопротеина присутствующего в белке куриных яиц, который нарушает всасывание биотина из-за образования нерастворимого комплекса;
в) длительное парэнтеральное питание;
г)наследственный дефект фермента, который присоединяет биотин к лизиновым остаткам апофермента.
Симптомы гиповитаминоза включают себорейный дерматит, тошноту, выпадение волос, боли в мышцах.
Фолиевая кислота (фолацин, витамин В9, витамин Вс)
Витамин обнаружили в 1930 г., когда было показано, что люди с определенным типом мегалобластической анемии могли быть излечены включением в пищу дрожжей или экстракта печени. В 1941 г. фолиевая кислота была выделена из зеленых листьев (лат. folium - лист, отсюда и название витамина). Витамином Вс это соединение назвали из-за его способности излечивать анемию у цыплят (от англ. chicken – цыпленок).
1. Структура. Фолиевая кислота состоит из птеридина, связанного с p-аминобензойной кислотой (ПАБК) и глутаминовой кислотой.

Фолиевая кислота плохо растворима в воде и органических растворителях, но хорошо в щелочных растворах. Разрушается под действием света, при обработке и консервировании овощей.
2. Метаболизм. Фолат в пище присутствует в форме полиглутамата. Внешние остатки глутамата удаляются в кишечнике до всасывания, главным образом, в тонком кишечнике. Коферментной формой фолиевой кислоты является 5,6,7,8-тетрагидрофолиевая кислота (ТГФК), которая образуется из фолиевой кислоты под действием фермента дигидрофолатредуктазы и с использованием НАДФН+Н+ как донора атомов водорода.
3. Биологическая роль.
3.1. Фолиевая кислота является переносчиком одноуглеродных радикалов (групп): метильного (-СН3), метиленового (=СН2), метенильного (≡СН), формильного (-СНО), оксиметильного (-СН2ОН) и формиминового (-СН=NH). Одноуглеродные фрагменты связываются с ТГФК в положениях N5 или N10. Присоединение формильного радикала в 5 положении приводит к образованию N5-формилТГФК, которая известна как фолиниковая кислота. МетиленТГФК образуется при взаимодействии ТГФК с глицином, серином или холином.
3.2. Фолат необходим для синтеза пуриновых нуклеотидов (2 и 8 атомы углерода) и синтеза тимина. N5,N10-метиленТГФК вводит метильную группу при синтезе тимидилата, необходимого для синтеза ДНК и образования эритроцитов.
3.3. Участвует в метаболизме глицина, серина и этаноламина.
3.4. N-формилметионин является инициирующей аминокислотой в биосинтезе белка у прокариот.
3.5. В крови ТГФК присутствует как N5-метилТГФК. Витамин В12 необходим для превращения N5-метилТГФК в ТГФК в реакции превращения гомоцистеина в метионин. Эта реакция необходима для освобождения свободной ТГФК и повторного использования в одноуглеродном метаболизме. При дефиците витамина В12 блокируется превращение N5-метилТГФК в ТГФК («фолатная ловушка»).
4. Источники: кишечная микрофлора, свежие овощи – салат, капуста, морковь, помидоры, лук.
5. Суточная потребность: 50-200 мкг.
6. Дефицит. При дефиците ТГФК снижается синтез пуринов и тимина, что приводит к нарушению синтеза ДНК. Это проявляется развитием мегалобластической анемии, которая характеризуется появлением в крови незрелых ядросодержащих форм эритроцитов.
Витамин В12 (кобаламин, антианемический витамин)
Злокачественная анемия (болезнь Аддисона-Бирмера) оставалась смертельным заболеванием до 1926 г., когда впервые для ее лечения применили сырую печень. Поиски содержащегося в печени антианемического фактора привели к успеху и в 1955 г. Дороти Ходжкин расшифровала структуру этого фактора и его пространственную конфигурацию с помощью метода рентгеноструктурного анализа.
1. Структура. Структура витамина В12 отличается от строения всех других витаминов наличием в молекуле иона металла – кобальта. Кобальт связан координационными связями с атомами азота, входящими в состав четырех пиррольных колец, которые образуют планарную (плоскую структуру), называемую коррином. I, II, III пиррольные кольца связаны через метиленовые мостики, IV и I – непосредственно. Перпендикулярно плоскости коррина расположен нуклеотид, содержащий 5,6-диметилбензимидазол, α-D-рибозу и остаток фосфорной кислоты, который связан координационной связью с атомом кобальта (рис. 10.2). В пище кобаламин содержит атом кобальта в окисленной форме (III). Для образования активных коферментных форм атом кобальта восстанавливается до Со (I).
В витамине В12 атомы углерода пиррольных колец замещены метильными, ацетамидными и пропионамидными радикалами. Пропионамидный радикал в IV кольце через изопропиловый спирт связан с фосфатным остатком нуклеотида.
Атом кобальта трехвалентен и ковалентно связан с группой CN-. Вся структура получила название цианокобаламина или кобаламина, поскольку считают, что цианид-ион является артефактом, зависящим от способа выделения.
Кобаламины растворимы в воде, термостабильны и устойчивы в присутствии растворов кислот при рН 4,0.
2. Транспорт и метаболизм
2.1. Витамин В12, содержащийся в пище, называют внешним фактором Кастла. Всасывается витамин в тонком кишечнике в комплексе с внутренним фактором Кастла (гликопротеин, секретируемый париетальными клетками желудка).
Витамин В12 находится в пище в комплексе с белками. В желудке под действием соляной кислоты и пепсина витамин В12 высвобождается из комплекса с белками и связывается с кобалофилином (R-протеин, гаптокоррин) – белком, секретируемым слюной. В двенадцатиперстной кишке комплекс распадается, кобалофилин гидролизуется панкреатическими протеазами, витамин В12 связывается с внутренним фактором Кастла. Комплекс витамин В12-внутренний фактор Кастла всасывается в дистальной части подвздошной кишки через рецепторы (кубилины), которые связывают комплекс, но не связывают свободный фактор или свободный витамин. Другой белок – мегалин – связан с кубилином и обеспечивает процесс эндоцитоза для всасывания комплекса
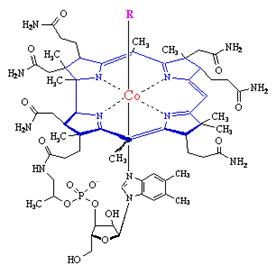
Рис. 10.2. Витамин В12.
2.2. Витамин транспортируется в крови в комплексе с белками, называемыми транскобаламинами и превращается в метилкобаламин и 5-дезоксиаденозилкобаламин в печени, клетках костного мозга и ретикулоцитах. Транскобаламин I участвует в хранении и резервировании водорастворимого витамина в печени и плазме крови (циркулирующий резерв). Транскобаламин II транспортирует витамин в крови. Комплекс транскобаламин II-витамин В12 поступает в периферические клетки путем эндоцитоза. В лизосомах клеток транскобаламин II разрушается, витамин высвобождается в виде гидроксикобаламина, который либо превращается в цитозоле в метилкобаламин, либо в митохондриях – в 5-дезоксиаденозилкобаламин. В печени запасается около 4-5 мг витамина и этих запасов достаточно для обеспечения организма витамином в течение 4-6 лет.
3. Биологическая роль.
В организме человека витамин необходим для 2-х важнейших реакций:
3.1. 5-дезоксиаденозилкобаламин является коферментом метилмалонил-КоА-мутазы, который превращает метилмалонил-КоА в сукцинил-КоА. Метилмалонил-КоА образуется как промежуточный продукт катаболизма валина и карбоксилирования пропионил-КоА, синтезирующегося при катаболизме изолейцина, холестерола, жирных кислот с нечетным числом атомов углерода или прямо из пропионовой кислоты (продукт микробиологической ферментации в кишечнике). В результате этой реакции метилмалонил-КоА превращается в сукцинил-КоА.
3.2. Метилкобаламин является коферментом гомоцистеинметилтрансферазы – фермента, катализирующего метилирование гомоцистеина в метионин. Кобаламин забирает метильные группы от N5-метилтетрагидрофолиевой кислоты и превращает ее в тетрагидрофолат. Метаболическое значение этой реакции состоит в том, что сохраняются запасы метионина и тетрагидрофолата, что необходимо для синтеза пуриновых, пиримидиновых нуклеотидов и синтеза нуклеиновых кислот. При дефиците витамина В12 фолат постоянно находится в форме N5-метил-ТГФК («фолатная» или метильная ловушка).
3.3. Витамин В12 требуется для превращения D-рибонуклеотидов в дезокси-D-рибонуклеотиды. Эту реакцию у прокариот катализирует специфическая рибонуклеотидредуктаза.
4. Источники. Основным источником витамина являются микроорганизмы. В растительной пище витамин В12 отсутствует. В небольших количествах витамин образуется бактериями на поверхности фруктов. Значительное количество витамина содержится в печени, дрожжах, молоке, яичном желтке.
5. Суточная потребность. 2-5 мкг.
6. Дефицит.
1. Энтеропеченочная циркуляция витамина В12 обеспечивает организм достаточным количеством витамина, и дефицит может развиваться при отсутствии витамина в диете в течение нескольких лет. При заболеваниях желудка или подвздошной кишки дефицит витамина может развиваться быстрее.
2. Пернициозная анемия является следствием дефицита витамина В12 и характеризуется нарушением синтеза ДНК, образования эритроцитов и появлением незрелых ядерных форм эритроцитов (мегалобластов).
3. Длительное вегетарианство может приводить к дефициту витамина В12.
Витаминоподобные вещества
Кроме витаминов, описанных выше, в пище присутствуют другие компоненты, которые являются незаменимыми факторами.
Холин
Best и Huntsman (1934) обнаружили, что дефицит холина у крыс вызывает жировое перерождение печени. Тем не менее, холин может адекватно синтезироваться в организме (из серина) и содержится во многих продуктах (молоко, яйца, печень, злаковые и др.).
1. Структура. По химическому строению холин – аминоэтиловый спирт, содержащий 3 метильные группы у атома азота.

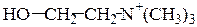
2. Биологическая роль.
2.1. Является компонентом фосфолипидов (лецитины), которые являются компонентами мембран и участвуют в транспорте липидов.
2.2. Предотвращает накопление липидов в печени (липотропный фактор), что объясняется участием в синтезе фосфолипидов и липопротеинов, транспортирующих жиры из печени.
2.3. Участвует в метаболизме одноуглеродных радикалов из-за наличия в структуре трех метильных групп.
2.4. Предшественник для синтеза ацетилхолина, который участвует в передаче нервного импульса.
3. Суточная потребность. Источники. Пищевым источником являются мясо и злаковые растения. Суточная потребность составляет в среднем 0,5 г.
4. Недостаточность. Проявления недостаточности холина у человека не описаны. У животных отмечаются жировая инфильтрация печени, повреждение кровеносных сосудов.
Инозит
1. Структура. По химическому строению – шестиатомный циклический спирт циклогексана, хорошо растворимый в воде.

2. Биологическая роль.
2.1. Необходим для синтеза фосфатидилинозитола (компонент клеточных мембран).
2.2. Действует как липотропный фактор (вместе с холином) и предотвращает накопление жиров в печени.
2.3. Является посредником в действии некоторых гормонов (инозитол-1,4,5-трифосфат). Инозитолтрифосфат способствует высвобождению кальция из эндоплазматического ретикулума.
2.4. Высокая концентрация отмечена в сердечной мышце, хотя функция не известна.
3. Суточная потребность. Источники. Инозитол находится во всех продуктах животного и растительного происхождения, особенно много его в печени, мозге, мясе, яичном желтке, а также в хлебе, картофеле, зеленом горохе, грибах. Суточная потребность приблизительно 1,0 -1,5 г.
4. Недостаточность инозитола у животных проявляется жировой дистрофией печени и падением содержания в ней фосфолипидов, облысением и анемией. У молодых особей наблюдается задержка роста
Липоевая кислота (витамин N)
1. Структура. В 1951 г. было выделено вещество, которое активно участвовало в обмене пирувата и ацетил-КоА – ключевых метаболитов клетки. Оно было названо липоевая кислота, так как хорошо растворялось в неполярных растворителях (lipid – жир). По химическому строению липоевая кислота является серосодержащей жирной кислотой (6,8-дитиооктановая кислота). Существует в окисленной и восстановленной формах.
2. Биологическая роль.
2.1. Участвует в реакциях окислительного декарбоксилирования вместе с другими витаминами (тиамин, ниацин, рибофлавин и пантотеновая кислота), в результате которых пируват превращается до ацетил-КоА и 2-оксоглутарат до сукцинил-КоА.
2.2. Является антиоксидантом и эффективна при защите организма от повреждающего действия радиации и токсинов.
3. Гипо- и гипервитаминозы липоевой кислоты у человека не описаны.
4. Суточная потребность. Источники. Наиболее богаты липоевой кислотой дрожжи, мясные продукты, молоко. Суточная потребность предположительно 1-2 мг.
Парааминобензойная кислота (ПАБК)
1. Структура. Является структурным компонентом фолиевой кислоты. Химическое строение ПАБК:
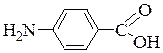
ПАКБ плохо растворяется в воде, хорошо – в спирте и эфире, химически устойчива.
2. Биологическая роль.
2.1. Витаминные свойства ПАБК связаны с тем, что она входит в состав молекулы фолиевой кислоты и, следовательно, принимает участие во всех реакциях метаболизма, где необходима фолиевая кислота.
2.2. Оказывает антигипоксическое, антиатерогенное действие, препятствует окислению адреналина, положительно влияет на функцию щитовидной железы.
3. Суточная потребность. Источники. ПАБК содержится практически во всех продуктах питания. Наиболее богаты ее печень, мясо, молоко, яйца, дрожжи. Суточная потребность не установлена.
Витамин Р (рутин, биофлавоноиды)
1. Структура. В 1936 г. А.Сент-Дьердьи из кожуры лимона выделил действующее начало, уменьшающее ломкость, проницаемость капилляров. Оно получило название витамин Р (от permeability – проницаемость).
Биофлавоноиды – разнообразная группа растительных полифенольных соединений, в основе структуры которых лежит дифенилпропановый углеродный скелет.

В растениях обнаружено свыше 4000 флавоноидов с идентифицированной химической структурой. Они делятся на 6 групп: флавонолы, флавоны, флавононы, катехины, антрагликозиды, антоцианы.
2. Биологическая роль.
2.1. Биофлавоноиды могут использоваться для синтеза биологически важных соединений в клетке (например, убихинона).
2.2. Рутин и кверцетин – полифенолы, обладающие Р-витаминной активностью, являются эффективными антиоксидантами. Флавоноиды (катехины) зеленого чая способны оказывать выраженное цитопротективное действие, в основе которого лежит их свойство обезвреживать свободные радикалы. В отличие от витамина Е, биофлавоноиды кроме прямого антирадикального действия могут также связывать ионы металлов с переменной валентностью, ингибируя, тем самым, процесс пероксидного окисления липидов мембран.
2.3. Достаточно изученным является капилляроукрепляющее действие витамина Р, обусловленное его способностью регулировать образование коллагена (синергизм с витамином С) и препятствовать деполимеризации основного вещества соединительной ткани гиалуронидазой.
3. Суточная потребность. Источники. Р-витаминные вещества содержатся в тех же растительных продуктах, что и витамин С. Наиболее богаты ими черноплодная рябина, черная смородина, яблоки, виноград, лимоны, чайный лист и плоды шиповника. Биофлавоноид цитрон придает кожуре лимона желтый цвет. Потребление флавоноидов в составе натуральных продуктов (фруктов, соков и виноградных вин), где они могут находиться в виде комплексов с металлами, может быть более эффективным, чем использование очищенных витаминных препаратов. Суточная потребность 25-50 мг.
4. Гиповитаминоз. Симптоматика недостаточности биофлавоноидов сводится к явлениям повышенной проницаемости и ломкости капилляров, петехиям (точечным ковоизлияниям), кровоточивости десен.
Витамин U
1. Структура. Витамин U был обнаружен в 1950 г. в сырых овощах. Поскольку сок сырых овощей, особенно капусты, обладал способностью предотвращать или задерживать развитие экспериментальных язв желудка, выделенный из него витамин назвали противоязвенным, или витамином U (от лат. ulcus – язва). По химическому строению он представляет собой S-метилметионин:

Витамин U хорошо растворим в воде. При варке пищи легко разрушается, особенно в нейтральной и щелочной среде.
2. Биологическая роль.
Подобно метионину витамин U является донором метильных групп в реакциях синтеза холина и креатина.
3. Недостаточность витамина у человека не описана. Цыплята, которым скармливался алкалоид цинкофен с целью моделирования язвы желудка, излечивались, если им в корм добавлялся свежий овощной сок.
4. Суточная потребность. Источники. Источниками витамина U являются свежая капуста, петрушка, морковь, лук, перец, зеленый чай, свежее молоко, печень.
Витамин F
В группу витамина F входят полиеновые жирные кислоты: линолевая, линоленовая, арахидоновая. При достаточном поступлении в организм линолевой и линоленовой кислот осуществляется синтез арахидоновой кислоты, являющейся предшественником эйкозаноидов (простагландинов, простациклинов, тромбоксанов и лейкотриенов). Одним из эффективных источников ω3 полиненасыщенных жирных кислот является льняное масло (α-линоленовая кислота – 52%). Для стабилизации ненасыщенных жирных кислот в масле присутствуют лигнаны, обладающие антиоксидантным и эстрогенным действиями.
Кофермент Q
В группу кофермента Q относят убихиноны. Убихинон Q10 может синтезироваться на конечных стадиях синтеза холестерола. Поэтому при применении классических статинов (ингибиторов ГМГ-редуктазы) могут проявляться эффекты недостаточности кофермента Q. В настоящее время разработаны статины второго поколения, которые блокируют синтез холестерола ниже места ответвления синтеза кофермента Q.
Кофермент Q находится в мембранах, является переносчиком электронов в липидной фазе мембран (цепи переноса электронов). Недостаточность кофермента Q проявляется в виде гипоэнергетического состояния и сопряженных с этим разнообразных функциональных нарушений.
Кофермент Q входит в состав многих биологически активных добавок к пище с целью оптимизации пищевой поддержки метаболизма.






