Восстановления цинка из расплавов происходит прямым и двухстадийным восстановлением:
(ZnO) + C = Zn + CO
С + CO2 = 2CO
(ZnO) + CО = Zn + CO2
(МеO) + C = Zn + CO
Несмотря на большое количество работ в настоящее время отсутствует единая точка зрения о доли прямого и двухстадийного (косвенного) восстановления.
Реакционная способность восстановителей по их отношению к ZnO в температурном интервале 850-1850К приведена на рисунке 11, из которого следует, что при 1700К восстановителей реакционная способность углерода выше чем СН4, Н2 и СО.
Кинетические кривые восстановления цинка из расплава оксидом углерода (II) при 12500С приведены на рисунке 11, из которого следует, что в течение 15 минут степень восстановления цинка составляет 92%.
Из рисунка следует, что при увеличении в расплаве FeO степень восстановления в цинка возрастает, и процесс восстановления цинка заканчивается при 12500С за 10 минут. Это объясняется тем, что железо, восстанавливающееся из цинка, реагирует с ZnO, восстанавливая его до металла: FeO + СО = Fe + СО2, Fe + ZnO = Zn + FeO

| 42%FeO |
| 35%FeO |
| Время, мин |
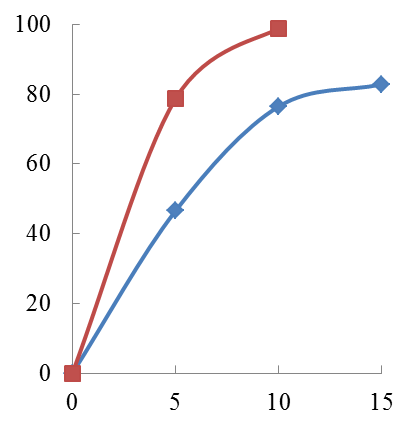
Рисунок 11. Кинетика восстановления цинка из расплава
При восстановлении цинка из шлаковых расплавов найдено, что СаF2, Na2O заметно ускоряют процесс, а Р2О5 снижает скорость восстановления. Это Влияние отражается и на «кажущуюся» энергию активации (таблица 1).
Таблица 9- Влияние добавок на Екаж газового (w) восстановления ZnO
| Температура, 0С | Екаж, ккал/моль | ||
| Без добавки | Na2O | Р2О5 | |
| 1250-1270 | 20,4 | 16,7 | 27,0 |
| 1270-1300 | 16,7 | 12,7 | 22,3 |
| 1300-1330 | 16,0 | 7,3 | 17,2 |
Одной из причин, вызывающей изменение скорости восстановления при введении поверхностно активных добавок, будет некоторое изменение поверхностной структуры расплава. При введение в шлак Р2О5 происходит перераспределение анионов кислорода. Сильный катион фосфора отрывает анионы кислорода от сиботаксисов Fe2+ и от силикатных комплексов. В результате строение последних усложняется, что приводит к снижению поверхностной активности железа и цинка и повышению поверхностной вязкости. Все это вместе взятое усиливает диффузионные затруднения при миграции катионов железа и цинка к реакционной границе с газом. Наоборот введение в шлак одновалентных ионов Na+ и F- сопровождается разрушением в поверхностном слое кремнекислородных комплексов. Так, структура исходного шлака будет разрушена добавками Na2O и СаF2.
Указанные явления, развиваются преимущественно в поверхностном слое, т.к. все добавки поверхностно активны.
В случае углетермического восстановления расплавов с теми же добавками положительный эффект введения Na2O и СаF2 возможно был усилен вследствие ускорения реакции регенерации окиси углерода на угле.
Процесс углетермического восстановления цинковистых расплавов может быть описан следующими уравнениями:
2ZnO + C = 2Zn + CO2 (а),
ZnO + C = Zn + CO (б),
2FeO + С = 2Fe + СО2 (в), (1)
FeO + С = Fe + СО (г),
Согласно современным взглядам, углетермическое восстановление протекает через промежуточный продукт – окись углерода, образующий новую фазу, в результате чего формируются две поверхности раздела: газ-шлак и газ-углерод. Роль окиси углерода при этом сводится в основном к доставке восстановителя к поверхности газ-расплав.
Система углерод-газ-шлак не равновесна в реальном процессе, причем скорость восстановления не является, строго говоря, функцией начального и конечного состояния, а зависит от пути, пройденного системой.
Поскольку перенос реагентов к поверхности взаимодействия осуществляется при участии трех фаз (углерод, газ, шлак), можно предполагать, что в зависимости от условий восстановления (температуры и состава шлака, определяющих подвижность ZnO и FeO в нем, крупности и текстуры частиц углерода, гидро- и аэродинамических факторов), общая скорость процесса может контролироваться скоростью одной или нескольких из ниже перечисленных стадий:
1) Диффузией ZnO и FeO в шлаке;
2) Подводом Со к поверхности расплава;
3) Адсорбцией СО на поверхности расплава;
4) Взаимодействием СО с окисью цинка или закисью железа;
5) Отводом продуктов реакции (СО2, Zn, Fe) от поверхности взаимодействия;
6) Регенерацией СО2 на поверхности углерода.
При большом избытке восстановителя, когда скорость реакции определяется в основном концентрацией МеО, получим:
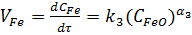 ,
,
 ,
,
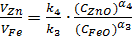 ,
,
При диффузионном режиме восстановления ZnO и FeO относительная скорость 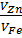 может быть увеличена путем перемешивания расплава, если α4>α3.
может быть увеличена путем перемешивания расплава, если α4>α3.
При α3 = α4 отношение 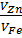 не зависит от условий перемешивания расплава.
не зависит от условий перемешивания расплава.
При α3 > α4 отношение 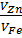 растет с уменьшением скорости конвективного переноса МеО к поверхности реакции.
растет с уменьшением скорости конвективного переноса МеО к поверхности реакции.
Во всех рассмотренных случаях отношение  увеличивается с ростом температуры, если при этом k2 и k4 возрастают быстрее, чем k1 и k3 соответственно. Если же энергия активации реакции восстановления ZnO ниже, чем энергия активации реакции восстановления FeO, отношение
увеличивается с ростом температуры, если при этом k2 и k4 возрастают быстрее, чем k1 и k3 соответственно. Если же энергия активации реакции восстановления ZnO ниже, чем энергия активации реакции восстановления FeO, отношение  уменьшается с ростом температуры.
уменьшается с ростом температуры.
Оборудование, технические инструментальные средства:
Схема установки, на которой проводится работа, приведена на рисунке 12. Установка состоит из трансформатора ОСУ-80, собственно одноэлектродной дуговой печи с графитовым тиглем механизма перемещения электрода, устройства плавного регулирования мощности, контрольно- измерительных приборов, вытяжного вентилятора.

|
Рисунок 12. Схема лабораторной установки для электроплавки цинковых руд
1 – Кожух печи, 2 - хромомагнезитовая футеровка, 3 - углеграфитовая подина, 4 - графитовый тигель. 5 - углеграфитовая «подушка», 6 -трансформатор ОСУ-80, 7 - терристорный регулятор, 8 - графитовый электрод, 9 - нижний токопровод, 10 - 13 – контролирующие амперметры и вольтметры, 14 - механизм перемещения электрода, 15 - гибкая часть короткой сети, 16 - крышка печи, 17- разъединитель.
Порядок проведения работы
Найденные посредством расчета количество компонентов шихты (цинковая руда, кокс и известь) взвешиваются и перемешиваются в сырьевом коробе. Общее количество шихты не должно превышать 1,5кг. Предварительно, в течение 60-80минут происходит разогрев дугой графитового тигля при J=500-600A и U=30-40B. После прогрева тигля в него порциями (по 100-200г) через каждые 5-7 минут загружается вся шихта. Плавка производится в течение 60минут в присутствии преподавателя и МОП. В период плавки можно наблюдать за расплавлением шихты и собственно выплавки ферросилиция. Смотреть в печь можно только через защитные очки. Работать у печи можно только в халате, в коксе. Руки должны быть защищены суконными перчатками.
После окончания плавки электрод поднимается. Печь отключается от трансформатора. Выемка тигля из печи производится после его охлаждения в течение 8-10 часов. Затем он разламывается. После охлаждения продукты восстанавливаются из тигля. Шлак и металлизированный сплав тщательно отделяются друг от друга и раздельно взвешиваются, далее анализируются на цинк и железо. Степень извлечения цинка в газовую фазу рассчитывают по формуле:
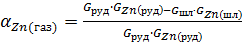
где Gруд, Gшл - соответственно количество руды и шлака, кг,
GZn(руд), GZn(шл) - соответственно содержание цинка в руде и шлаке, %.
Необходимые расчеты
В качестве цинксодержащей руды используют руду месторождения Шайморден, содержащую: 55,6% ZnCO3; 0,9% PbCO3; 3,3% FeCO3; 1,8% ZnS; 7,5%СаСО3·MgCO3; 5,2% Al2O3; 25,7% SiO2.
Восстановителем служит кок, который содержит: 85,1%С; 5,1% SiO2; 2,0%СаО; 0,8%MgО; 3,8%Fe2О3; 0,8%S; 1,4%Н2О; 1,0% Al2O3.
Степень извлечения цинка составляет 96-98%.
Степень восстановления железа - 96-98%.
Степень восстановления кремния - 3-6%.
Отношение СаО / SiO2 в шихте должно быть равным (0,8-1,4): 1.






