X. ПРИМЕР ТЕПЛОВОГО РАСЧЕТА
10.1. По заданному литражу выбираем прототип:
ГАЗ – 3111-113;
Размеры цилиндров и скорость поршня.
Ход поршня рассчитываем исходя из заданного литража (2,52 л) и отношения S / D. Принимаю S / D = 1, т.е. короткоходный двигатель.
D =100· 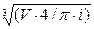 = 92,91 мм;
= 92,91 мм;
Принимаем: S = 93 мм — ход поршня;
D = 93 мм — диаметр поршня.
Степень сжатие задана ε = 10,1.
Vср = S ∙ nN / 3·104 = 93·4500/ 3·104 = 13,95 м/с.
10.3. Расчётные режимы по частоте (заданы).
n min = 875 min – ¹ – минимальная частота;
nМ = 2250 min – ¹ – частота при максимальном моменте;
nN = 4500 min – ¹ – частота при максимальной мощности;
n max = 4950 min – ¹ – максимальная частота.
Марка топлива.
АИ – 92, где 92 – октановое число установленное по исследовательскому методу.
Определяем низшую теплоту сгорания топлива, параметры рабочего тела
при заданном ε = 10,1 и бензине АИ – 92 средний элемент, состав и молекулярная масса бензина по формуле:
C = 0,855; H = 0,145; m т = 115 кг/кмоль.
Н u = 33,91C +125H – 10,89(O – S) – 2,51(9H + W),
где W = 0; O = 0; S = 0.
Отсутствует влага и сера.
Подставим:
Н u = 33,91· 0,855 + 125,6· 0,145 – 2,51·(9· 0,145 + 0) = 43,93 кДж/кг·топлива
Параметры рабочего тела.
а) Определяем количество воздуха для полного сгорания топлива.
L o = (1/0,208)(C/12+H/4 – O/32),
L o = (1/0,208)·(0,85/12 + 0,145/4) = 0,517 кмоль воздуха/кг топлива.
б)
l o = (1/0,23)·(8/3·C + 8·H – 0),
l o = (1/0,23)·(8/3·0,855+8·0,145) = 14,957 кг воздуха/кг топлива.
Коэффициент избытка воздуха.
α = L g/ L o = l g / l o,
где L g, l g — соответственно количество кмолей и количество кг воздуха содержащегося в составе свежей смеси; L o, l o — соответственно количество кмолей и количество кг воздуха теоретически необходимого (стехиометрическое) для полного сгорания одного кг топлива.
Значение величин α задано в задании при соответствующих частотах
n min = α = 0,96; nМ = α = 1; nN = α =1; n max = α = 0,98.
Количество свежей смеси.
M 1 = α· L o + 1/ m т ,
где α – коэффициент избытка воздуха, m т = 115 кг/кмоль – молекулярная масса топлива.
M 1 (n min) = 0,96·0,517+1/115 = 0,5049 кмоль свежей смеси/кг топлива;
M 1(nМ ) = 1·0,517 +1/115 = 0,52552 кмоль свежей смеси/кг топлива;
М 1(nN ) = 1·0,517+1/115 = 0,52552 кмоль свежей смеси/кг топлива;
M 1(n max) = 0,84·0,517+1/115 = 0,51519 кмоль свежей смеси/кг топлива.
Количество отдельных компонентов продуктов сгорания.
Принимаем K = 0,47 (для бензина K = 0,45 … 0,5),
где K — коэффициент, определяющий отношение количество водорода (H2) к количеству окиси углерода (CO) содержащегося в продуктах сгорания.
M СО2= (C/12) – 2·((1– α)/(1 + K))·0,208· L о; M СО = 2·1– α/1 + K ·0,208· L o;
M H2O = (H/2) – 2 K ·((1– α)/(1+ K))·0,208· L o; M H2= 2 K ·1– α/1 + K ·0,208· L o;
M N2= 0,792·α· L o;
M СО2(n min) = (0,855/12) – 2·[(1– 0,96)/(1 + 0,47)]·0,208·0,517 = 0,0654 кмоль CO2 /кг топлива;
M СО (n min) = 2· [(1 – 0,96)/(1 + 0,47)]·0,208·0,517 = 0,00585 кмоль CO /кг топлива;
M H2O (n min) = (0,145/2) – 2·0,47·[(1 – 0,96)/(1 + 0,47)]·0,208·0,517 = 0,07 кмоль
H2O /кг топлива;
M H2(n min) = 2·0,47·[(1 – 0,96)/(1 + 0,47)]·0,208·0,517 = 0,00275 кмоль H2 /кг топлива;
M N2(n min) = 0,792·0,96·0,517 = 0,39295 кмоль N2 /кг топлива.
M СО2(nМ) = (0,855/12) – 2·[(1 – 1)/(1 + 0,47)]·0,208·0,517 = 0,07125 кмоль CO2 /кг топлива;
M СО (nМ) = 2·[(1 – 1)/(1 + 0,47)]·0,208·0,517 = 0 кмоль CO /кг топлива;
M H2O (nМ) = (0,145/2) – 2·0,47·[(1 – 1)/(1 + 0,47)]·0,208·0,517 = 0,073 кмоль H2O /кг топлива;
M H2(nМ) = 2·0,47·[(1 – 1)/(1 + 0,47)]·0,208·0,517 = 0 кмоль H2 /кг топлива;
M N2(nМ) = 0,792·1·0,517 = 0,40933 кмоль N2 /кг топлива.
M СО2(nN) = (0,855/12) – 2·[(1 – 1)/(1 + 0,5)]·0,208·0,517 = 0,07125 кмоль CO2 /кг топлива;
M СО (nN) = 2·[(1 – 1)/(1 + 0,47)]·0,208·0,517 = 0 кмоль CO /кг топлива;
M H2O (nN) = (0,145/2) – 2·0,47·[(1 – 1)/(1 + 0,47)]·0,208·0,517 = 0,073 кмоль H2O /кг топлива;
M H2(nN) = 2·0,47·[(1 – 1)/(1 + 0,47)]·0,208·0,517 = 0 кмоль H2 /кг топлива;
M N2(nN) = 0,792·1·0,517 = 0,40114 кмоль N2 /кг топлива.
M СО2(n max) = (0,855/12) – 2·[(1 – 0,98)/(1 + 0,5)]·0,208·0,517 = 0,06832 кмоль
CO2 /кг топлива;
M СО (n max) = 2·[(1 – 0,98)/(1 + 0,47)]·0,208·0,517 = 0,00293 кмоль CO /кг топлива;
M H2O (n max) = (0,145/2) – 2·0,47·[(1 – 0,98)/(1 + 0,47)]·0,208·0,517 = 0,071 кмоль
H2O /кг топлива;
M H2(n max) = 2·0,47·[(1 – 0,98)/(1 + 0,47)]·0,208·0,517 = 0,001375 кмоль H2 /кг
топлива;
M N2(n max) = 0,792·0,98·0,517 = 0,40114 кмоль N2 /кг топлива.
Общее количество продуктов сгорания.
M 2 = M СО2+ M СО + M H2O + M H2+ M N2,
M 2 (n min) =0,0654 + 0,00585034 + 0,06975 + 0,00275 + 0,39295 = 0,53670385 кмоль продуктов сгорания/кг топлива;
M 2(nМ ) = 0,07125 + 0 + 0,0725 + 0 + 0,40933 = 0,55307692 кмоль продуктов сгорания/кг топлива;
M 2(nN) = 0,07125 + 0 + 0,0725 + 0 + 0,40933 = 0,55307692 кмоль продуктов сгорания/кг топлива;
M 2(n max) = 0,06832 + 0,00292517 + 0,07113 + 0,00137 + 0,40114 = 0,54489038 кмоль продуктов сгорания/кг топлива.
Таблица 10.1
Результаты расчётов количества продуктов сгорания.
| параметры | n min | nМ | nN | n max | |
| n, min – 1 | |||||
| α | 0,96 | 0,98 | |||
| M 1 | 0,50485 | 0,52552 | 0,52552 | 0,51519 | |
| M СО2 | 0,0654 | 0,07125 | 0,07125 | 0,06832483 | |
| M СО | 0,00585 | 0,00292517 | |||
| M H2O | 0,06975 | 0,0725 | 0,0725 | 0,071125 | |
| M H2 | 0,00275 | 0,001375 | |||
| M N2 | 0,392954 | 0,409327 | 0,409327 | 0,40114 | |
| M 2 | 0,536704 | 0,55308 | 0,55308 | 0,54489 |
Процесс впуска.
Параметры окружающей среды.
Принимаем P o = 0,1 МПа – давление окружающей среды;
T o = 293 °K – температура окружающей среды;






