«адание 1. «апишите в тетрадь уравнение реакции вашего варианта (см. табл. 1).
1. «апишите кинетическое уравнение реакции.
2. ѕо значени€м констант скоростей реакции k 1 и k2 при двух температурах определите энергию активации и предэкспоненциальный множитель (k 0).
3. –ассчитайте константу скорости при температуре “ 3. —делайте вывод о вли€нии температуры на скорость реакции.
4. ќпределите концентрацию вещества, израсходованного за врем€ t при “ 3, если начальные концентрации равны с 0.
5. –ассчитайте период полупревращени€ реакции при “ 3.
«адание 2. «апишите в тетрадь уравнение реакции вашего варианта (см. табл. 2а):
1. –ассчитайте стандартные энтальпию и энтропию химической реакции, установите знак теплового эффекта.
2. ƒаны концентрации веществ. с 0(—) и с 0(D) равны нулю. ќпределите неизвестные (исходные или равновесные) концентрации исходных веществ и продуктов реакции.
3. «апишите кинетическое уравнение реакции.
4. –ассчитайте скорость пр€мой реакции, а также изменение скорости при одновременном изменении концентрации и температуры реакции (табл. 2 б).
5. ”кажите направление смещени€ равновеси€ при изменении одного из факторов (—, – или “).
“ а б л и ц а 1
“аблица вариантов
| є варианта | –еакци€ | “ 1, | k 1 | T 2, K | k 2 | T 3, K | t, мин | — 0, моль/л | ||||
| —Ќ3—6Ќ4N2Cl + H2O Ѓ ЃCH3C6H4OH + N2 + HCl | 9×10Ц3 минЦ1 | 13×10-3 минЦ1 | 100 | 0,1 | ||||||||
| NaBO3 + H2O Ѓ Ѓ NaH2BO3 +1/2 O2 | 2,2×10Ц3 минЦ1 | 4,1×10Ц3 минЦ1 | 0,05 | |||||||||
| —ќ(—Ќ2—ќќЌ)2 Ѓ Ѓ —ќ(—Ќ3)2 + 2—ќ2 | 2,46×10Ц5 минЦ1 | 5,76×10Ц3 минЦ1 | 2,5 | |||||||||
| CH3CO2C2H5 + NaOH Ѓ Ѓ CH3CO2Na + C2H5OH | 2,37 л/(моль×мин) | 3,204 л/(моль×мин) | 0,8 | |||||||||
| —2Ќ6 Ѓ —2Ќ4 + Ќ2 | 2,5×10Ц5 сЦ1 | 141,5×10Ц5 сЦ1 | ||||||||||
 6 6
| —6Ќ5—Ќ2Br + —2Ќ5ќЌ Ѓ —6Ќ5—Ќ2ќ—2Ќ5 + ЌBr | 1,44 л/(моль×мин) | 2,01 л/(моль×мин) | 2,6 | ||||||||
| (C2H5)3N + CH3I Ѓ Ѓ [(C2H5)3CH3N]I | 3,29×10Ц2 л/(моль×с) | 8,1×10Ц2 л/(моль×с) | 0,02 | |||||||||
| —Ќ3—ќќ—Ќ3 Ѓ Ѓ —2Ќ4 + Ќ2 + —ќ2 | 2,59×10Ц2 минЦ1 | 3,43×10Ц2 минЦ1 | 2,5 | |||||||||
| —12Ќ22ќ11 + Ќ2ќ Ѓ Ѓ —6Ќ12ќ6(глюкоза) +—6Ќ12ќ6(фруктоза) | 5,03×10Ц2 минЦ1 | 2,1×10Ц2 минЦ1 | 1,5 | |||||||||
| Cu + (NH4)2S2O8 Ѓ Ѓ CuSO4 + (NH4)2SO4 | 9,6×10Ц3 л/(моль×мин) | 39,96×10Ц3 л/(моль×мин) | 0,01 | |||||||||
| 2 HI Ѓ H2 + I2 | 666,8 | 0,256 см3/(моль×с) | 698,6 | 67,0 см3/(моль×с) | 0,5 | |||||||
| H2 + I2 Ѓ 2 HI | 666,8 | 15,59 см3/(моль×с) | 698,6 | 67,0 см3/(моль×с) | 0,05 | |||||||
| Ќ—Ќќ + Ќ2ќ2 Ѓ Ќ—ќќЌ + Ќ2ќ | 0,75 л/(моль×ч) | 0,94 л/(моль×ч) | ||||||||||
| —Ќ3—ќќ—Ќ3 + Ќ2ќ Ѓ Ѓ —Ќ3—ќќЌ + —Ќ3ќЌ | 0,563×10Ц3
| 1,663×10Ц3 л/(моль×мин) | 1,5 |
ќ к о н ч а н и е т а б л. 1
| є варианта | –еакци€ | “ 1, | k 1 | T 2, K | k 2 | T 3, K | t, мин | — 0, моль/л |
| Ќ2 + Br2 Ѓ 2 HBr | 1,59×10Ц2 л/(моль×мин) | 2,6×10Ц3 л/(моль×мин) | 0,09 | |||||
| 2NO Ѓ N2 + O2 | 4.76×104 л/(моль×мин) | 1,07×103 л/(моль×мин) | 2,8 | |||||
| 2NO2 Ѓ N2 + 2O2 | 6,72 л/(моль×мин) | 977 л/(моль×мин) | 1,75 | |||||
| –Ќ3 Ѓ –г + 3/2 Ќ2 | 3,05×10Ц4 л/(моль×с) | 6,33×10Ц5 л/(моль×с) | 0,8 | |||||
| SO2Cl2 Ѓ SO2 + Cl2 | 1,02×10Ц6 л/(моль×с) | 2,2×10Ц5 л/(моль×с) | 2,5 | |||||
 20 20
| —2Ќ5ONa + CH3I Ѓ Ѓ C2H5OCH3 +NaI | 0,0336 л/(моль×с) | 2,125 л/(моль×с) | 0,9 | ||||
| —H2OHCH2Cl + KOH Ѓ ЃCH2OHCH2OH + KCl | 1,13×10Ц2 л/(моль×с) | 8,72×10Ц2 л/(моль×с) | ||||||
| N2O5 Ѓ N2O4 +1/2 O2 | 0,203×102 л/(моль×мин) | 0,475×10Ц3 л/(моль×мин) | ||||||
| —H2ClCOOH + H2O Ѓ Ѓ CH2OHCOOH + HCl | 0,222×10Ц4 л/(моль×мин) | 0,237×10Ц2 л/(моль×мин) | 0,5 | |||||
| CH3COOCH3 + H2O Ѓ Ѓ CH3COOH + CH3OH | 1,609×10Ц2 л/(моль×мин) | 3,784×10Ц2 л/(моль×мин) | 3,0 | |||||
| 2 HI Ѓ H2 + I2 | 0,942×10Ц6 л/(моль×мин) | 0,31×10Ц2 л/(моль×мин) | 2,3 |
“ а б л и ц а 2а
“аблица вариантов
| Ќомер варианта | ”равнение реакции | с 0(ј) моль/л | с 0(¬) моль/л | [A] моль/л | [B] моль/л | [C] моль/л | [D] моль/л | с прор. (ј) |
| —ќ2(г) + —(к) = 2 —ќ(г) | 0,5 | Ц | ||||||
| 2Ќ2 (г) + —(к) = —Ќ4 (г) | Ц | 0,5 | ||||||
| 2 H2S(г)+ SO2(г) = 3S(к) + 2 Ќ2ќ(г) | 0,5 | |||||||
| —Ќ4(г) + Ќ2ќ(г) = —ќ(г) + 3Ќ2(г) | 1,5 | 0,6 | ||||||
| 3O2(г) + 2 H2S(г) = 2 Ќ2ќ(ж) + 2 SO2(г) | ||||||||
| I2(г) + H2S(г) = 2HI (г) + S(к) | 0,4 | Ц | ||||||
| —2Ќ6(г) + 7/2ќ2 = 2—ќ2(г) + 3Ќ2ќ(ж) | 2,3 | 0,6 | ||||||
| —ќ(г) + Ќ2 (г) = —(к) + Ќ2ќ (г) | ||||||||
| SO2(г) + —l2(г) = SO2Cl2(ж) | Ц | 0,25 | ||||||
| ќ2 (г) + 2 NO (г) = 2NO2(г) | 1,75 | 0,5 | Ц | |||||
 11 11
| FeO(к) + —ќ(г) = —ќ2 (г) + Fe(к) | 0,5 | 0,2 | |||||
| —ќ(г) + Ќ2ќ(г) = —ќ2 (г) + Ќ2(г) | 0,5 | |||||||
| Ќ2(г) + —l2(г) = 2 HCl(г) | Ц | |||||||
| Ќ2(г) + I2(г) = 2 HI (г) | 0,5 | Ц | 0,5 | |||||
| —l2(г) +2HI(г) = I2(г) + 2HCl(г) | 1,5 | |||||||
| Fe2O3(к) + 3Ќ2(г) = 2 Fe(к) + 3Ќ2ќ(г) | 0,5 | |||||||
| CH4(г) + 4 Cl2(г) = ——l4(г) + 4 ЌCl(г) | 0,5 | |||||||
| —Ќ4(г) + 2 ќ2 (г) = —ќ2 (г) + 2 Ќ2ќ(г) | ||||||||
| 2 NO2 (г) + 4Ќ2(г) = N2(г) + 4 Ќ2ќ(г) | 0,3 | 0,1 | ||||||
| 4 HCl (г) + ќ2 (г) = 2 Ќ2ќ(г) + 2Cl2(г) | 0,5 | 0,2 | ||||||
| SO2(г) +2H2S (г) = 3 S(к) + 2 Ќ2O(ж) | 0,1 | |||||||
| MgO(к) + Ќ2(г) = Mg(к) + Ќ2ќ(ж) | 0,5 | |||||||
| 2ZnS (к) + 3ќ2(г) = 2ZnO(т) + 2SO2 | 0,5 | |||||||
| 2 PH3(г) + 4ќ2(г) = –2ќ5(к) + 3Ќ2ќ(ж) | 1,4 | |||||||
| Ќ2ќ2(ж) + Ќ2(г) = 2Ќ2ќ (г) | 0,5 | 0,2 |
|
|
|
 |
“ а б л и ц а 2б
“аблица вариантов
| Ќомер варианта | ”равнение реакции | с (ј), моль/л | с (¬), моль/л | D“ | g | »зменение условий с рi “ | ||
| (см. табл. 2а) | ½ сј | сј увеличить | ||||||
| 3/2 сј | сј увеличить | |||||||
| 2 сј | ½ с¬ | 1,5 | ”величить | |||||
| ½ сј | 2 с¬ | 2,5 | ”меньшить | |||||
| 3 сј | 2 с¬ | ”меньшить | ||||||
| ½ сј | 3 с¬ | ”величить | ||||||
| 4 сј | 1,5 | с¬ уменьшить | ||||||
| 2 сј | ½ с¬ | ”величить | ||||||
| ½ сј | ¼ с¬ | ”меньшить | ||||||
| 2 сј | 3/2 сј | 1,5 | ”величить | |||||
| Ц | 3 с¬ | ”величить | ||||||
 12 12
| 2 с¬ | 1,5 | ”меньшить | |||||
| 2 сј | 3 с¬ | ”величить | ||||||
| 2 сј | ”величить | |||||||
| ½ сј | 3 с¬ | с¬ уменьшить | ||||||
| Ц | 2 с¬ | ”величить | ||||||
| 4 сј | 3/2 с¬ | с¬ увеличить | ||||||
| 2 сј | ”величить | |||||||
| ½ сј | 3 с¬ | ”меньшить | ||||||
| 2 сј | ½ с¬ | ”меньшить | ||||||
| 2 сј | 3 с ¬ | с¬ увеличить | ||||||
| 3 с¬ | 1,5 | ”меньшить | ||||||
| 2 с¬ | 2,5 | ”меньшить | ||||||
| 2 сј | ½ с¬ | ”меньшить | ||||||
| 2 сј | 3 с¬ | ”величить |

–астворы. гидролиз солей
–ј—“¬ќ–џ Ц однородные смеси переменного состава двух или большего числа веществ (компонентов). ћогут быть газовыми (например, воздух), жидкими и твердыми (например, многие сплавы).
¬ жидких растворах компонент, наход€щийс€ в избытке, называетс€ растворителем, все остальные компоненты Ц растворенные вещества. ¬ растворах протекают многие природные и промышленные про-цессы; изучение свойств растворов св€зано с такими практическими проблемами, как разделение веществ (газов, нефтей), глубока€ очистка, подбор растворителей дл€ реализации технологических процессов.
|
|
|
ќсновной количественной характеристикой растворов €вл€етс€ концентраци€, котора€ отражает содержание растворенных веществ в единице массы, единице объема раствора или растворител€. ѕо концентрации растворенного вещества растворы подраздел€ют на насыщенные, ненасыщенные и перенасыщенные.
ћол€рна€ концентраци€ (с в) Ц число молей растворенного вещества
в 1 л раствора
 краткое обозначение Ц ћ.
краткое обозначение Ц ћ.
ћол€рна€ концентраци€ эквивалента (с экв) Ц число молей эквивалентов растворенного вещества в 1 л раствора
 краткое обозначение Ц н.
краткое обозначение Ц н.
ћол€льность (сm) Ц число молей растворенного вещества в 1000 г растворител€


ћассова€ дол€ Ц отношение массы растворенного вещества к массе всего раствора (в % Ц число граммов растворенного вещества в 100 г раствора)

“итр (“ в) Ц число граммов растворенного вещества в 1 мл раствора

¬ажной количественной характеристикой растворов €вл€етс€ растворимость ср, котора€ численно равна концентрации насыщенного раствора вещества при данной температуре. –астворимость выражаетс€ в г/л и моль/л.
∆идкие растворы подраздел€ют на растворы электролитов, способные проводить электрический ток, и растворы неэлектролитов, которые не электропроводны. ѕроцесс распада электролита на ионы под действием молекул растворител€ называетс€ электролитической диссоциацией. оличественно диссоциаци€ характеризуетс€ степенью диссоциации a, котора€ равна отношению концентрации молекул, распавшихс€ на ионы (с), к общей концентрации растворенного электролита (с 0): a = с / с 0. ѕо величине a электролиты дел€тс€ на две группы: слабые сa < 3 % и сильные с a > 30 %.
сильным электролитам в водных растворах относ€т гидроксиды s- элементов (кроме ¬е(ќЌ)2, Mg(OH)2)), гидроксиды лантаноидов типа La(OH)3, почти все соли (кроме ZnCl2, ZnI2, CdCl2, CdI2, Mg(CN)2, HgCl2, Fe(CNS)3, Hg(CN)2 и др.), неорганические кислоты Ц HNO3, HCl, HBr, HI, HClO4, HMnO4, разбавленна€ H2SO4.
слабым электролитам в водных растворах относ€тс€ основани€ d-, f-, p- элементов, органические и многие неорганические кислоты, вода и комплексные ионы.
¬ растворе слабого электролита устанавливаетс€ равновесие, характеризуемое константа диссоциации (K дисс) Ц отношение произведени€ равновесных концентраций ионов в степени соответствующих стехиометрических коэффициентов к концентрации недиссоциированных молекул. K диссхарактеризует способность вещества распадатьс€ на ионы: чем выше K дисс, тем больше концентраци€ ионов в растворе.
ƒиссоциации слабых многоосновных кислот или многокислотных оснований протекают по ступен€м, соответственно дл€ каждой ступени существует сво€ константа диссоциации.
«ависимость степени диссоциации от концентрации электролита выражаетс€ уравнением ќствальда

ѕрименительно к очень слабым электролитам (aї 0), счита€ что 1 Ц aї 1:

ƒл€ описани€ свойств реальных растворов используетс€ активность а Ц мера реального поведени€ вещества в растворе; степень отклонени€ поведени€ реального раствора от идеального выражаетс€ коэффициентом активности. јктивность а иона св€зана с его концентрацией с через коэффициент активности f формулой:
а = с× f.
оэффициент активности зависит от ионной силы I раствора соотношением 
»онна€ сила раствора учитывает различные электростатические взаимодействи€ между ионами и определ€етс€ как полусумма произведений мол€льных концентраций ст всех ионов в растворе на квадрат их зар€да z:
I = ½ × S z 2 × cт.
»онна€ сила сказываетс€ на равновесии в системе малорастворимый электролит Ц раствор. ≈сли малорастворимый электролит находитс€ в растворе, содержащем другие ионы с высокой их концентрацией, то вместо концентраций следует пользоватьс€ активност€ми ионов, тогда выражение произведени€ растворимости записываетс€
в виде
|
|
|
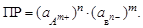
–астворимость вещества ср св€зана с ѕ– соотношением:

¬ водных растворах концентрации Ќ+ и ќЌЦ взаимосв€заны выражением константы диссоциации воды

“ак как [H2O] величина при н.у. посто€нна€ величина, равна€ 55,49 моль/л, то произведение Ќ+ и ќЌЦ Ц также посто€нна€ дл€ данной температуры величина, котора€ называетс€ ионным произведе - нием воды Kw и равна 10Ц14. ¬ чистой воде [Ќ+] = [ќЌЦ] =
= 10Ц7 моль/л Ц среда нейтральна€; если [H+] > 10Ц7 Ц среда кисла€, в щелочной среде [OHЦ] > 10Ц7 моль/л.
¬еличина, равна€ отрицательному логарифму концентрации Ќ+,называетс€ водородным показателем
рЌ = Цlg[H+].
ƒл€ расчета рЌ сильных кислот используют формулу
рЌ = Цlgа(H+) = Цlg(f× [H+]).
ƒл€ расчета рЌ сильных оснований справедливо
рЌ = р w Ц р ќЌ = 14 + lg a (OH Ц).
ѕри расчете рЌ слабых кислот и оснований учитывают, как правило, только 1-ю ступень диссоциации слабого электролита и провод€т по приближенной формуле рЌ = Ц lg[H+]и р ќЌ = Ц lg[ќHЦ]. ѕри этом равновесные концентрации ионов Ќ+ иќЌЦ рассчитывают, исход€ из соответствующих констант диссоциации.
√идролиз солей. √идролизом солей называют реакции обмена между молекулами воды и ионами соли с образованием слабых электролитов. ѕри этом также образуетс€ некоторый избыток либо ионов водорода, либо ионов гидроксида, и рЌ раствора гидролизующейс€ соли отличен от нейтрального.
√идролитическое равновесие реакции гидролиза можно описать соответствующей константой равновеси€ Ц константой гидролиза г. онстанта гидролиза св€зана с ионным произведением воды и констан-той диссоциации слабого электролита соотношением г = w / дисс; если соль образована слабым основанием и слабой кислотой, то
г = w /( а × b),где а и b Цконстанты диссоциации слабой кислоты и слабого основани€ соответственно.
оличественной характеристикой глубины протекани€ гидролиза €вл€етс€ степень гидролиза b: b = с г/ с 0, где с г Ц равновесна€ концентраци€ гидролизованных ионов; с 0 Ц исходна€ концентраци€ ионов соли, подвергающихс€ гидролизу. ѕо определению, b < 1.
—тепень гидролиза св€зана с г и исходной концентрацией гидролизующихс€ ионов соотношением, аналогичным закону ќствальда:

≈сли b << 1, то гї b2 × с 0.
–ассчитывают рЌ растворов гидролизующихс€ солей учитыва€, как правило, только 1-ю ступень гидролиза. –авновесную концентрацию Ќ+ или ќЌЦ наход€т, исход€ из констант гидролиза или степени гидролиза.
¬ случае соли, образованной слабым основанием и слабой кислотой, степень гидролиза и концентраци€ ионов водорода не завис€т от исходной концентрации соли и определ€ютс€ по формулам:



ѕримеры решени€ задач
1. »меетс€ раствор сульфата алюмини€ с массовой долей w = 10 % и плотностью r= 1,105 г/см3. аковы мол€рна€ концентраци€, мол€рна€ концентраци€ эквивалента, титр, мол€льность и мол€рна€ дол€ этого раствора.
–ешение. Ќайдем массу 1 л раствора
т р-ра = rр-ра × V р-ра = 1,105 г×смЦ3× 1000 см3 = 1105 г.
ѕо определению массовой доли, в 100 г раствора содержитс€ 10 г Al2(SO4)3, следовательно, в 1105 г будет содержатьс€ (1105×10)/100 =
= 110,5 г Al2(SO4)3.
–ассчитаем мол€рную массу Al2(SO4)3 и определим мол€рную концентрацию раствора.
ћ(Al2(SO4)3) = 342 г/моль.
“аким образом, в 1 л раствора содержитс€ 
 моль и мол€рна€ концентраци€ составит 0,32 моль/л.
моль и мол€рна€ концентраци€ составит 0,32 моль/л.
Ёквивалент молекулы Al2(SO4)3 равен 1/6 молекулы. —оответ-ственно 1 моль-эквивалент составл€ет 1/6 часть мол€ Al2(SO4)3. —ледовательно, в одном моле Al2(SO4)3 содержитс€ шесть моль-эквива-лентов, а в 1 л данного раствора 0,32 × 6 = 1,92 моль-экв Al2(SO4)3.
“аким образом, мол€рна€ концентраци€ эквивалента с экв равна
1,92 моль/л (1,92 н.).
Ќайдем титр раствора, т.е. содержание Al2(SO4)3 в 1 мл:
 г/мл.
г/мл.
ѕо условию в 100 г раствора содержитс€ 10 г Al2(SO4)3 и 90 г Ќ2ќ. “огда на 1 кг, т.е. на 1000 г воды приходитс€ (1000×10)/90 = 111,11 г Al2(SO4)3. Ёто составл€ет 111,11/342 = 0,325 моль. —ледовательно,
в 1000 г растворител€ Ќ2ќ содержитс€ 0,325 моль растворенного вещества Al2(SO4)3 и мол€льность раствора сm по определению равна 0,325 моль/1000г = 0,325 моль/кг воды.
Ќайдем массу воды: т воды = m р-ра Ц т в-ва = 1105 Ц 110,5 = 994,5 г.
Ёто составл€ет 994,5/18 = 55,25 моль.
ћол€рна€ дол€ Al2(SO4)3 в растворе составит:

2. „ему равна массова€ дол€ 0,2 ћ раствора (NH4)2SO4 с плот-ностью r = 1,015 г/см3?
|
|
|
–ешение. “ребуетс€ перейти от концентрации, выраженной в моль/л, к отношению масс растворенного вещества и раствора.
¬ыразим массу вещества сульфата аммони€ из формулы мол€рной концентрации:
 .
.
ѕодставим это выражение в формулу дл€ определени€ массовой доли и преобразуем:
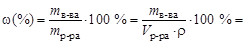
 .
.
ѕо формуле взаимосв€зи мол€рной концентрации с ви массовой доли wнаходим последнюю величину:

3. –ассчитать водородный показатель 0,005 н. раствора хлороводородной кислоты, содержащего 0,01 моль/л хлорида натри€.
–ешение. ƒанный раствор содержит сильные электролиты, которые диссоциируют по уравнени€м:
HCl = H+ + ClЦ
NaCl = Na+ + ClЦ .
¬одородный показатель такого раствора определ€етс€ активностью иона Ќ+:
рЌ = р а (Ќ+) = Ц lg a (H+).
јктивность иона водорода определ€етс€ как
а (Ќ+) = f× с в(Ќ+).
ћол€рна€ концентраци€ раствора HCl равна с в = с экв/ z экв =
= 0,005 моль/л, следовательно, концентраци€ с (Ќ +) = 0,005 моль/л;
с (Na)= 0,01 моль/л; с (Cl Ц) = 0,01 + 0,005 = 0,015 моль/л.
ѕлотность очень разбавленного раствора можно прин€ть равной плотности воды rї 1000 г/л, поэтому при вычислении ионной силы I раствора, а также активности иона, вместо мол€льных концентраций можно использовать приблизительно равные им мол€рные концент-рации:
I = ½(c (Ќ +) × z 2(Ќ +) + с (—l Ц) × z 2(Cl Ц) + c (Na +) × z 2(Na +) =
= ½ × (0,005×12 + 0,015×12 + 0,01×12) = 0,015.
ѕо уравнению предельного закона ƒеба€Ц’юккел€ определ€ем средний коэффициент активности ионов в данном растворе:

—ледовательно, f = 0,867.
Ќаходим активность ионов водорода:
а (Ќ+) = f × с в(Ќ +) = 0,867×0,005 = 0,0043.
“огда, рЌ = Ц lg4,3×10Ц3 = 2,37.
4. –ассчитайте рЌ 0,1 ћ раствора циановодородной кислоты HCN. ќпределите, как изменитс€ рЌ, если к 1 л раствора добавить
0,1 моль цианида натри€ NaCN, кажуща€с€ степень диссоциации которого 0,85?
–ешение. —лаба€ циановодородна€ кислота диссоциирует согласно уравнению: HCN ó H+ + CNЦ.
”читыва€, что константа диссоциации HCN а = 4,93×10Ц10, степень диссоциации кислоты в растворе без добавлени€ соли можно вычислить по упрощенному выражению закона разведени€ ќствальда:

–авновесна€ мол€рна€ концентраци€ иона водорода составит:
[H+] = a × с HCN = 7,02×10Ц5×0,1 = 7,02×10Ц6 моль/л.
—ледовательно, водородный показатель исходного раствора равен:
рЌ = Ц lg[H+] = 5,15.
ѕри добавлении в раствор соли NaCN равновесие диссоциации кислоты, согласно принципу Ће ЎательеЦЅрауна, сместитс€ влево
(в сторону образовани€ кислоты) в результате по€влени€ в растворе большого количества ионов CNЦ за счет диссоциации сильного электролита:
NaCN = Na+ + CNЦ.
ѕри этом уменьшитс€ концентраци€ ионов водорода в растворе, т.е. диссоциаци€ слабой кислоты будет подавлена. Ќовую концентрацию ионов водорода можно обозначить через х (моль/л) концентраци€ ионов CNЦ, вносимых солью с концентрацией 0,1 моль/л:
c (CNЦ) = a× c (NaCN) = 0,1× 0,85 = 0,085 моль/л.
ќбща€ концентраци€ цианид-ионов в новом растворе составит
[CNЦ] = x + c (CNЦ) = x + 0,085.
ѕодставл€€ концентрации ионов в выражение а и учитыва€, что из-за очень незначительной диссоциации кислоты концентраци€ недиссоциированной кислоты [HCN] практически совпадает с исходной концентрацией, получают

–еша€ уравнение, находим х = [H+] = 5,8×10Ц10 моль/л.
—ледовательно, новое значение водородного показател€ раствора
рЌ = Ц lg 5,8×10Ц10 = 9,24.
“аким образом, после добавлени€ соли среда раствора изменилась и вместо слабокислой стала слабощелочной, что обусловлено не только подавлением диссоциации слабой кислоты HCN, но и гидролизом по аниону соли NaCN.
5. ќцените степень диссоциации a в 0,005 ћ и 0,05 ћ растворах сернистой кислоты H2SO3.
–ешение. ƒл€ решени€ следует использовать закон разведени€ ќствальда и значени€ констант диссоциации (из приложени€). —ерниста€ кислота Ц слабый электролит, диссоциирует ступенчато:
 ; а I= 1,7×10Ц2 (1-€ ступень),
; а I= 1,7×10Ц2 (1-€ ступень),
 ; а II= 6,3×10Ц8 (2-€ ступень).
; а II= 6,3×10Ц8 (2-€ ступень).
ѕоскольку II < K I, то диссоциацией кислоты по 2-й ступени можно в 1-м приближении пренебречь и рассчитывать a дл€ 1-й ступени диссоциации.
— другой стороны, значение K I относительно велико, поэтому рас-чет a следует проводить по строгой формуле ќствальда. ƒл€ 0,005 ћ раствора


–асчет по приближенной формуле а ~ a2 × с приводит к величине больше 1, что не имеет смысла. ƒл€ 0,05 ћ раствора получим:

–асчет по приближенной формуле дает a ~ 0,58, что существенно отличаетс€ от рассчитанного выше. Ќетрудно видеть, что с уменьшением концентрации слабого электролита a увеличиваетс€.
6. ¬ычислить константу гидролиза г, степень гидролиза bг и рЌ 0,1 ћ раствора цианида натри€.
–ешение. —оль NaCN, €вл€€сь сильным электролитом, полностью диссоциирует на ионы Ц NaCN Ѓ Na+ + CNЦ. —оль NaCN образована сильным основанием NaOH и слабой кислотой HCN, поэтому гидролизуетс€ по аниону. «аписываем ионно-молекул€рное и молекул€рное уравнение гидролиза:
CNЦ + H-OH ó HCN + OHЦ
NaCN + H-OH ó HCN + NaOH
√идролитическое равновесие характеризуетс€ константой гидролиза, которое выводитс€ с использованием ионного уравнени€ гидролиза:
 .
.
“ак, константа диссоциации HCN а = 4,93×10Ц10. “огда

ѕоскольку г мала, то степень гидролиза определ€етс€ по формуле:

¬ соответствии со стехиометрией реакции гидролиза [OHЦ] =
= bг × с в = 1,42×10Ц3. ќпределим гидроксидный показатель и рЌ раствора:
рќЌ = Ц lg1,42×10Ц3 = 2,85, тогда рЌ = 14 Ц рќЌ = 11,15.
7. ќпределить значение рЌ 0,01 ћ раствора хлорида цинка.
–ешение. —оль ZnCl2 образована слабым основанием Zn(OH)2
и сильной кислотой HCl, поэтому гидролизуетс€ по катиону:
I ступень
Zn2+ + H-OH ó ZnOH+ + H+
ZnCl2 + H-OH ó ZnOHCl + HCl
II ступень
ZnOH+ + H-OH ó Zn(OH)2 + H+
ZnOHCl + H-OH ó Zn(OH)2 + H+
ќпределим константы гидролиза дл€ каждой ступени:


Ќаходим концентрации ионов водорода, образующихс€ на I и II ступен€х гидролиза:
 [H+]I = (2,04×10Ц8×10Ц2)1/2 = 1,43×10Ц8,
[H+]I = (2,04×10Ц8×10Ц2)1/2 = 1,43×10Ц8,
 (7,58×10Ц10×10Ц2)1/2 = 2,75×10Ц6.
(7,58×10Ц10×10Ц2)1/2 = 2,75×10Ц6.
—ледовательно,
[H+] = [H+]I + [H+]II = 1,705×10Ц5 и рЌ = Ц lg[H+] = 4,77.
—реда кисла€.
ƒл€ I ступени гидролиза рЌ можно рассчитать по формуле:
рЌ = Ц ½ ×lg( г(I) × с) = Ц ½×lg (2,04×10Ц8×10Ц2) = 4,85,
значит, при приближенном расчете рЌ раствора солей II-й ступенью гидролиза можно пренебречь.
«афиксировать величину рЌ данного раствора лучше всего можно с помощью лакмуса, который изменит свою окраску с синей на красную.
8. –ассчитать объем воды, необходимый дл€ растворени€ 2,35 г йодида серебра AgI при “ = 298 .
–ешение. «аписываем уравнение гетерогенного равновеси€:
AgI = Ag+ + IЦ.
—в€зь между величиной произведени€ растворимости ѕ– и растворимостью S,выраженной в моль/л, определ€етс€ выражением:
ѕ–AgI = [Ag+]×[IЦ] = S 2.
ќтсюда растворимость AgI:

и масса AgI в 1 л насыщенного раствора (массова€ концентраци€)
с масс.AgI = S AgI ×M AgI = 9,22×10Ц9×235 = 2,17×10Ц6 г/л.
”читыва€, что основной объем раствора занимает вода, объем воды, необходимый дл€ растворени€ 2,35 г AgI, вычисл€ют по формуле:







