Теорію, яка пояснює будову і властивості тіл на основі закономірностей руху і взаємодії молекул, називають молекулярно-кінетичною теорією (МКТ). Значний внесок у створення МКТ зробили: Лавуаз'є, Ломоносов, Больцман (друга половина ХІХ ст.).
Основні положення МКТ речовини:
1. Будь-які речовини мають дискретну (переривчасту) будову. Вони складаються з найдрібніших частинок молекул і атомів.
Молекула (від латинського «молес» - маса, «кула» - зменшувальний суфікс) – це найменша частинка речовини, яка здатна самостійно існувати і зберігає хімічний склад цієї речовини.
Молекули складаються з атомів (від грецького «атомос» - неподільний) хімічних елементів.
Атом – це найменша частинка хімічного елементу. Атом не ділиться при хімічних реакціях. Атом складається з позитивно зарядженого ядра і негативно заряджених електронів. Електрони постійно рухаються в електричному полі ядра. Атоми з'єднуються в молекулу за рахунок хімічних зв'язків.
У природі є 92 хімічні елементи. Разом із штучними наразі налічується 105 елементів. Число атомів в молекулах змінюється від 2, 3, 4 до сотень і тисяч.
Наприклад, Н 2О – молекула води, яка складається з 2 атомів водню, 1 атому кисню.
Якщо при якому-небудь природному явищі молекули залишаються незмінними, то речовина зберігає свої властивості. Якщо ж молекули змінюють свою будову або ж розпадаються на окремі атоми, то з'являються нові речовини з іншим хімічним і фізичним складом.
Речовину, яка побудована з атомів лише одного виду, називають елементом (водень, кисень, азот тощо). Кожен елемент має свій номер Z в таблиці Менделєєва. Число Z визначає кількість протонів у ядрах атомів і електронів, що рухаються в атомі навколо ядра.
2. Молекули знаходяться в стані неперервного хаотичного (невпорядкованого) руху, що називається тепловим.
Під час нагрівання речовини швидкість теплового руху і кінетична енергія його частинок збільшуються, а під час охолодження зменшуються. Ступінь нагрітості тіла характеризує його температура, яка є мірою середньої кінетичної енергії хаотичного поступального руху молекул цього тіла.
3. Молекули взаємодіють одна з одною із силами електромагнітної природи, причому на великих відстанях вони притягуються, а на малих - відштовхуються. Сили притягання і відштовхування між молекулами діють постійно.
Ці сили мають електромагнітну природу. Розділення сил взаємодії на «сили притягання» та «сили відштовхування» умовне. Вважають, що сили притягання позитивні, а сили відштовхування негативні.
Сили притягання діють на відстанях між центрами молекул порядку r = 10-9 м. При зближенні молекул сили притягання збільшуються. Ці сили є короткодіючими – вони швидко зменшуються при збільшенні відстані між молекулами.
Сили відштовхування діють на відстанях порівняних з лінійними розмірами неорганічних молекул r = 10-10 м. Сили відштовхування зменшуються при збільшення відстані між молекулами ще швидше, ніж сили притягання.
Агрегатні стани речовини.
Молекули різних речовин по-різному взаємодіють одна з одною. Ця взаємодія залежить від типу молекул і відстані між ними Залежно від характеру руху і взаємодії молекул розрізняють три стани речовини: твердий, рідкий, газоподібний.
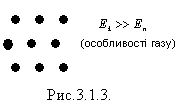
Гази. Для газів характерні великі міжмолекулярні відстані, малі сили притягання, тому гази можуть необмежено розширюватись. Молекули газу хаотично рухаються, співударяються одна з одною і зі стінками посудини (мал.3.1.3). молекули газу розлітаються у різні боки, при цьому займають весь об’єм посудини. Гази не мають певного об'єму і форми і легко стискуються під дією зовнішньої сили.
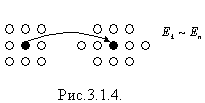
У рідинах молекули розміщені тісно і коливаються навколо положення рівноваги, а також перескакують з одного рівноважного положення в інше (ближній порядок) (мал. 3.1.4). Рідини мають певний об'єм, але не мають певної форми (приймають форму посудини).
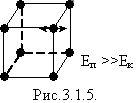
У твердих тілах сили взаємодії кожної молекули із сусідніми настільки великі, що молекула здійснює малі коливання навколо деякого сталого положення рівноваги - вузла кристалічних грат - дальній порядок (мал.3.1.5). Тверді тіла мають форму і об'єм.
Молекули так мали, що уявити собі їх розміри можна тільки за допомогою порівнянь. Наприклад, молекула води у стільки разів менша за розміри великого яблука, у скільки разів яблуко менше земної кулі.
Відносною молекулярною (або атомною) масою речовини (Мr) називається відношення маси молекули (або атома) даної речовини (m0) до 1/12 маси атома вуглецю (moc):
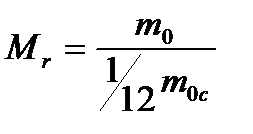
Відносна молекулярна маса — величина безрозмірна.
На практиці маси молекул виражаються малими і незручними для розрахунків числами. Тому як еталон для порівняння використовують спеціальну одиницю - атомну одиницю маси (а.о.м.):
Атомною одиницею маси (а.о.м.) називають 1/12 маси атома вуглецю С12. Маси всіх атомів і молекул порівнюють з атомною одиницею маси.
1 а.о.м. = 1,66·10-27 кг
Чим більше атомів або молекул в тілі, тим більше речовини міститься у ньому. Кількість речовини природно було б вимірювати числом молекул або атомів в тілі. Але у зв'язку з дуже великою кількістю молекул у будь-якому тілі. Тому зручно вказувати не абсолютне число атомів і молекул, а відносне. Прийнято порівнювати число молекул або атомів в даному телі з числом атомів в 0,012 кг вуглецю.
В Міжнародній системі одиниць кількість речовини виражаються у молях.
Один моль – це кількість речовини, що містить стільки ж часток (атомів, молекул), скільки міститься атомів в 0,012 кг вуглецю С12 Таке число молекул називається числом Авогадро і дорівнює
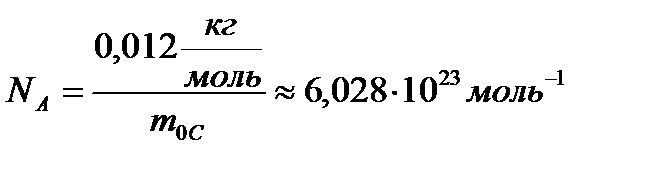
Таким чином, число Авогадро визначає кількість молекул в одному молі речовини. Одиниця кількості речовини — моль — входить до числа основних одиниць системи СІ (поряд з кг, м, с).
Кількість речовини ν дорівнює відношенню числа молекул N у даному тілі до постійної Авогадро NА, тобто числу молекул в 1 молі речовини:
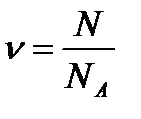
Звідки можна визначити кількість молекул в довільній масі речовини:
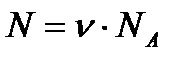
Поряд з відносною молекулярною масою Мr в фізиці та хімії використовується й молярна маса М.
Молярна маса – це маса речовини, узята в кількості одного моля.(це маса одного моля речовини)
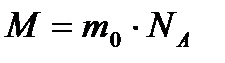
Маса m будь-якої кількості речовини дорівнює добутку маси однієї молекули m0 на число молекул N в тілі:
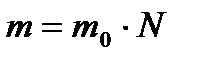
З урахуванням формул кількість речовини можна визначити:
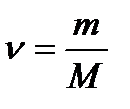
Кількість речовини дорівнює відношенню маси речовини до її молярної маси.
Число молекул можна визначити:
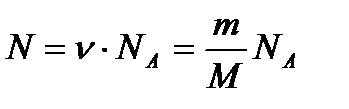
Зв'язок між молярною та молекулярною масами:
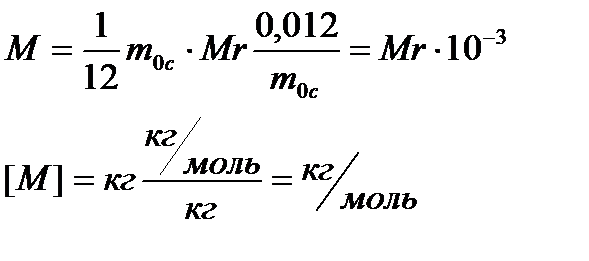
При вивченні властивостей газу за допомогою експериментів було встановлено, що один моль будь-якого газу при нормальних умовах має об’єм:
Vм=22,4·10-3 м3, чи Vм=22,4л.
Цей результату повній відповідності з відомим хімічним законом Авогадро: у рівних об’ємах різних газів при однакових температурах та тиску міститься однакове число молекул.






