Липиды – называются органические в-ва которые содержатся в живых клетках и могут быть экстрагированы из клеток с помощью растворителей.
Липиды выполняют различные функции:
1.Макроэргические вещества. Липиды — наиболее важный из всех питательных веществ источник энергии.В количественном отношении липиды — основной энергетический резерв организма. В основном жир содержится в клетках в виде жировых капель, которые служат метаболическим «топливом». Липиды окисляются в митохондриях до воды и диоксида углерода с одновременным образованием большого количества АТФ (ATP).
2. Структурные блоки. Ряд липидов принимает участие в образовании клеточных мембран. Типичными мембранными липидами являются фосфолипиды, гликолипиды и холестерин. Следует отметить, что мембраны не содержат жиров.
3. Изолирующий материал. Жировые отложения в подкожной ткани и вокруг различных органов обладают высокими теплоизолирующими свойствами. Как основной компонент клеточных мембран липиды изолируют клетку от окружающей среды и за счет гидрофобных свойств обеспечивают формирование мембранных потенциалов.
4. Прочие функции липидов. Некоторые липиды выполняют в организме специальные функции Стероиды, эйкозаноиды и некоторые метаболиты фосфолипидов выполняют сигнальные функции. Они служат в качестве гормонов, медиаторов и вторичных переносчиков (мессенджеров), Отдельные липиды выполняют роль «якоря», удерживающего на мембране белки и другие соединения. Некоторые липиды являются кофакторами, принимающими участие в ферментативных реакциях, например, в свертывании крови или в трансмембранном переносе электронов. Светочувствительный каротиноид ретиналь играет центральную роль в процессе зрительного восприятия. Поскольку некоторые липиды не синтезируются в организме человека, они должны поступать с пищей в виде незаменимых жирных кислот и жирорастворимых витаминов.
Свойства. Некоторые вещества, которые относятся к липидам обладают биол. активностью (жирорастворимые витамины, некоторые гормоны). Основное св-во липидов – это их амфифильность, и в структуре выделяют полярную часть, а также гидрофобные углеводородные цепи. Большинство свойств определяются нейтральными жирами, которые очень слабо полярны и имеют сродство к воде. Они находятся в клетке в безводном состоянии и служат энергетическим резервом.
Классификация. Делятся на 4-ре класса:
I. Жирные кислоты. называются карбоновые кислоты с углеводородной цепью не менее 4 атомов углерода. Они присутствуют в организмах всех видов в виде сложных эфиров (например, с глицерином и холестерином). Многие жирные кислоты имеют одну или несколько двойных связей. К наиболее распространенным ненасыщенным кислотам относятся олеиновая и линолевая. Из двух возможных цис- и транс- конфигурации двойной связи в природных липидах присутствует лишь цис- форма. Разветвленные жирные кислоты встречаются только в бактериях. К незаменимым жирным кислотам относятся те из них, которые не синтезируются в организме и должны поступать с пищей. Речь идет о сильно ненасыщенных кислотах, в частности арахидоновой (20:4;5,8,11,14), линолевой (18:2;9,12) и линоленовой (18:3;9,12,15).
II. Глицерин содержащие липиды.
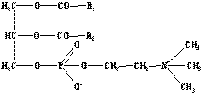
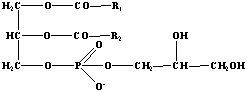
1. Глицерофосфолипиды. Наиболее простая форма фосфолипидов, фосфатидовые кислоты – исходным веществом для синтеза других фосфолипидов. Остаток фосфорной кислоты может образовывать сложноэфирную связь с гидроксильными группами аминоспиртов (холин, этаноламин или серин) или полиспиртов (миоинозит). В качестве примера здесь приведен фосфатидилхолин. При взаимодействии с глицерином двух остатков фосфатидовой кислоты образуется дифосфатидилглицерин.
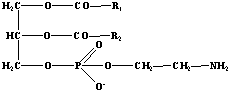
|
|
|
| Фосфатидилхолин | Фосфатидилэтаноламин | Фосфатидилглицерин |
2. нейтральные жиры (моно-, ди-, три-ацетилглецирин; простые эфиры глицерина; гликозилглицериды). Так как молекулы жиров не несут заряда. Углеродные атомы глицерина в молекулах жиров не эквивалентны. При введении одного заместителя в группу CH2OH центральный атом углерода становится асимметрическим.
III. Липиды не содержащие глицерин.
1. Сфинголипиды. В их структуре имеется сфингозин или дигидроксисфингозин.
| СН3- (СН2)12- СН = СН - СН - СН - СН2-ОН | | ОН NH2 сфингозин |
а) церамиды; (производная сфингозина, здесь аминогруппа ацилирована жирной кислотой. По строению выделяют сфингомиелин.
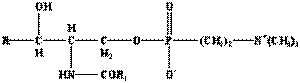
б) гликосфинголипиды. явл-ся производной церамидов, но не содержит фосфат в своём составе и азотистых оснований. В эту структуру входит один или несколько остатков углеводов.
в) ганглиозиды.
2. Алифатические спирты и воска. Алифатические спирты образуют сложные эфиры с жирными кислотами. СН3(СН2)14СН2ОН цетиловый спирт.
3. Терпены. Изопрены это 2-метилбутадиен, у многих из этих соед. число углеродных атомов кратно 5. Поэтому структуру можно разбить на пятичленные. Терпены входят в состав эфирных масел. к терпенам относят: каучук, смоляные кислоты. Родственный к терпену это витамин Е.
4. Стероиды. Структурно стероиды сходны с терпенами, однако разнообразие их биол. свойств сделала их более изученным классом в-в биол. происхождения. К стероидам относятся соединения, имеющие в своей структуре стерановое ядро. Характеристика: все циклы являются насыщенными; обязательное присутствие ОН-группы в положении С3; наличие метильных групп в С18, С19 связаны с углеводными атомами С10,С13. Однако у эстрогенов кольца А явл-ся арамотическим и отсутствует метильная группа связанная с С10. Наличие алифатических заместителей в положении С17, по структуре этого заместителя стероиды классифицируют след. образом: а) стерины – содержит связанную из 8-9 или 10 углеводородных атомов (холестерин). б) желчные кислоты – из 5 атомов(холевая к-та). в) адренокортикостероиды – 2 атома углерода и прогестрон.
IV. Липиды связанные с веществами других классов.
Липопротеины – это комплексы из липидов со специфическими белками.
Протеолипиды, фосфотиды, липополисахарид и др.
42 Структурно-функциональная организация биомембран, механизмы повреждения их структуры и функции
Блиологические мембраны мембраны играют важную роль по ряду причин. Они отделяют клеточное содержимое от внешней среды, регулируют обмен между клеткой и средой, и делят клетки на компартменты, предназначенные для тех или иных метаболических путей. Некоторые химические реакции протекают на самих мембранах. На мембранах также располагаются рецепторные участки для распознавания внешних стимулов (гормонов или др.хим. в-ств), поступающих из окружающей среды или из другой части самого организма. Известно, что мембраны способны пропускать лишь воду и другие малые молекулы, например молекулы газов. Это свойство было названо избирательной проницаемостью.
Выяснилось, что мембраны состоят почти целиком из белков и липидов. Липиды в мембране представлены гликолипидами, фосфолипидами и стеролами. 2 слоя липидных молекул образуют бимолекулярный слой. Полярные головки фосфолипидов – гидрофильны и обращены наружу и внутрь клетки, где среда гидрофильная. А хвосты фосфолипидов – гидрофобны, соответственно они обращены друг к другу, между полярными головками, где среда гидрофобная. Биомембрана - это динамическая структура, белки плавают в липидном «море» подобно островам, иногда свободно, а иногда на привязи – их удерживают микрофиламенты, проникающие в цитоплазму. Липиды также могут перемещаться меняя своё положение.
Некоторые мембранные белки лишь частично погружены в мембрану (полуинтегральные), тогда как другие пронизывают всю её толщу (интегральные). В белковых молекулах или между соседними белковыми молекулами имеются гидрофильные каналы или поры. Эти поры пронизывают мембрану, так что по ним сквозь мембрану могут проходить полярные молекулы. Кроме того в мембранах имеются гликопротеины. У них на свободных поверхностях находятся гликозильные группы – разветвлённые олигосохаридные цепи, напоминающие антенны. Эти «антенны», состоящие из нескольких моносахаридных остатков имеют самую разнообразную конформацию. Функция антенн связана с распознавание внешних сигналов, благодаря этому клетки правильно ориентируются и образуют ткани в процессе дифференцировки. С распознавание связана деятельность различных регуляторных систем, а также иммунный ответ, в котором гликопротеины играют роль антигенов. Многие рецепторы пересекают мембрану не один раз, а именно 7 (оптимально).
Постоянно происходит и диффузия белка в сторону (латеральная). 2 вида взаимодействия:
1) белок-белковое
2) белок-липидное
Состав мембранных липидов варьирует и это влияет на такие их свойства как жидкое состояние и проницаемость. У ненасыщенных липидов в углеводородных хвостах молекул имеются так называемые «изломы». Эти изломы препятствуют слишком плотной упаковке молекул и делают структуру мембраны более рыхлой. От этого состояния зависит активность мембран и, в частности, лёгкость слияния отдельных мембран друг с другом, а также активность, связанных с мембраной ферментов и транспорт белков.
Итог:
7) разные типы мембран различаются по соей толще, но в большинстве случаев толщина мембран 5-10 нм.
8) Мембраны – это липопротеиновые структуры (липид+белок). К некоторым липидным и белковым молекулам, на внешних поверхностях присоединены углеводные компоненты (гликозильные группы)
9) Липиды спонтанно образуют бислой. Это объясняется тем, что их молекулы имеют полярные головы и неполярные хвосты
10) Мембранные белки выполняют разнообразные функции (рецепторы, переносчики, преобразователи энергии)
11) Две стороны мембраны могут отличатся одно от другой и по составу, и по свойствам
12) Мембранные липиды и белки быстро диффундируют в плоскости мембраны, если только они как-нибудь не закреплены или не ограничены в своём передвижении.
20. Внутриклеточный транспорт
Целенаправленный транспорт необходим каждой клетке. Особенно это важно для больших клеток, где развита компартментализация. У прокариот транспорт внутри клетки происходит проще (вспомните амёбу). Итак, виды внутриклеточного транспорта:
а) диффузия. Может происходить в случае существования градиента концентрации
б) целенаправленный транспорт макромолекул:
участвуют пучки микротрубочек (тубулин) (+)-----------------(-) а по ним «идут» молекулы динеина (белок из семейства белков миозина: динеин, кинезин, миозин), которые «несут на себе» транспортируемую молекулу белка. Нужно сказать, что динеин имеет глобулярную часть, которая и прикрепляется к микротрубочке. Таким образом, пучки микротрубочек выполняют роль РЕЛЬС! Вспомните как двигаются поезда!? Ну, как впечатляет? ….кстати понятно, что здесь написано? Мне – с трудом. Главное – это ВАШЕ ВООБРАЖЕНИЕ!
в) транспорт в мембранной упаковке:
- везикулы d=0,1 – 1,5 мкм; эта везикула прикрепляется к своеобразной молекуле диненина вышеописанным способом.
- транспорт в лизосомах
Не относится к транспорту в мембранной упаковке циклоз пластид и митохондрий
г) да, не забывайте про активный транспорт (электрохимический градиент, Na-K насосы)
43. Избирательная проницаемость биомембраны
Перенос вещества в клетку может происходить по нескольким механизмам: методом простой диффузии, которая можно разделить на диффузию мелких незаряженных молекул (спирт, углеводороды, лекарства) и диффузию ионов (истинная диффузия, канальный транспорт, перенос с помощью переносчика-ионофора); методом облегченной диффузии (оба метода идут без затраты энергии) и путем активного транспорта, идущего с затратой энергии АТФ.
Диффузия. Поток вещества идет по градиенту диффузии и подчиняется закону Фика:
Dm/dt=-DS(dc/dx),
D-коэффициент диффузии, s-площадь, dm-масса, проходящего вещества, но если предположить простейший случай, когда t и S=1, тогда получаем упрощенную формулу: поток вещества в единицу времени через единицу площади равен движущей силе или градиенту концентрации.
I= -D(dc/dx)
При прохождении ионов через канал или с помощью ионофоров скорость движения зависит от 1) диэлектрической проницаемости, 2) наличия фиксированного заряда, 3) размера и числа пор в мембране, 4) заряда иона. Движущей силой в данном случае служит не только разность концентраций, но и градиент зарядов на поверхности мембраны и определяется электродиффузным уравнением Нэрнста-Планка.
I= -D (dc/dx) + ZF(dj/dx) (последнее слагаемое – электрический градиент)
Еще один способ миграции – по ионным каналам. Они представляют собой интегральные белки или липопротеины с порой внутри. Для каждого иона имеется свой канал, т.е. этим достигается селективность (Na – 0,31-0,51 нм, К – 0,45 нм). Селективность задается только размерами канала, особенностью является однорядность движения. Поступление ионов в канал сопровождается замещение с гидратных молекул на молекулы, выстилающие внутри канал. Ион, проходя через канал, способен индуцировать электрическое поле, а это тормозит прохождение иона, т.о. ион проходит ряд энергетических барьеров и впадин. Вход в канал для иона облегчается выходом его предшественника. Проходимость линейно зависит от концентрации, но это справедливо только для низких концентраций.
Скорость потока ионов зависит от 1) просвета (лучше проходят те ионы, размер которых соответствует размеру поры), 2) т.к. пора представляет собой белок, то внутри существует неоднородное поле, создающее энергетические ямы и барьеры, 3) сильное электрическое поле иона вызывает поляризацию и переориентацию близлежащих групп белка. Все это лежит в основе селективности работы каналов (для Na, K, Cl).
Существуют различные способы управления ионными каналами:
1) ионный канал, управляемый электрическим полем (сенсор, расположенный в молекуле белка образующего пору реагирует на напряженность электрического поля на мембране и в зависимости от этого открывается или закрывается канал. Это потенциалзависимый канал).
2) ионный канал, управляемый непосредственно химическим стимулом (сигнальная молекула ацетилхолина, имеющая рецептор на поверхности канала, взаимодействует с ним и открывает канал. Это N-холинорецепторный канал. Канал закрывается с диссоциацией ацетилхолина от рецептора).
3) ионный канал, регулируемый опосредованно химическим стимулом.
Перенос веществ через мембрану можно осуществить с помощью ионофоров. Было в частности обнаружено, что для К таким переносчиком служит валиномицин. Ионофоры имеют специфическую структуру, что позволяет им формировать гранулу, внутри которой заключен переносимый ион, а снаружи содержится гидрофобная область, благодаря чему такая структура свободно проникает через липидную мембрану.
Облегченная диффузия. Таким образом в клетку попадают простые сахара, аминокислоты. Примером может служить поступление в клетку глюкозы.
Активный транспорт. Живая клетка отличается наличием градиентов. Поддержание этих насосов обеспечивается действием насосов. Так, например, К значительно больше внутри клетки, а Na снаружи, и такое соотношение поддерживается постоянным действием насосов, на работу которых требуется энергия АТФ. Для животной клетки характерны следующие процессы: перенос Na-K, перенос Ca, перенос H. K-Na-АТФаза встроена в плазматическую мембрану, Ca-АТФаза встроена в структуры Са депо – саркоплазматический ретикулум, диски палочек и колбочек сетчатки. Транспорт протонов водорода на электросопрягающих мембранах осуществляется с помощью Н-АТФазы.
Са-АТФаза. Состоит из одной субъединицы, представленной одной полипептидной цепочкой, упакованной в мембране, Mr 100кДа, содержит много гидрофобных аминокислот, что позволяет прочно закрепиться в мембране. Процесс переноса заключается в следующем: 1) две молекулы Са садятся на Са-связывающие места, а молекула Mg и АТФ – на активный центр. 2) происходит гидролиз АТФ, образуется промежуточный макроэрг. 3) конформационная перестройка за счет избытка энергии. Са-связывающие места из положения наружу переходят в положение во внутрь, меняется характер связывания Са с Са-связывающими местами, происходит замещение макроэргической связи на простую, Са-связывающие участки освобождаются от Са, остаток энергии возвращает фермент в исходное состояние. При таком переносе энергия АТФ расходуется на снижение константы связывания ионов на наружной поверхности с 107 до 103 на внутренней стороне, а также к повышению константы диссоциации. Таким образом для переноса двух молекул Са требуется одна молекула АТФ.
Na-K-АТФаза. Представляет собой интегральный белок на цитоплазматической мембрнае, состоящийиз 2 полипептидных цепей, большая представляет a-субъединицу, активный центр расположен на цитоплазматической стороне мембраны, b-субъединица полуинтегральна, это гликозилированная субъединица, на наружной поверхности которой располагаются сахарные остатки. Центры связывания Na находятся на a-субъединице, К – на b-субъединице. Процесс переноса: 1) на внутренней стороне мембрнаы происходит связывание молекул Mg и АТФ с активным центром и связь ионов с соответствующими центрами. 2) связывание АТФ с активным центром приводит к его гидролизу и образованию фосфорилированного белка, образуется макроэргическая связь, при этом происходит конформационная перестройка молекулы белка: a-субъединица остается на месте, а b-субъединица максимально погружается в мембрану, происходит обмен ионами. Макроэргичность исчает, но остаток фосфорной кислоты остается прикрепленным, происходит обратный отток субъединицы. Диссоциация фосфатного остатка энергетически обеспечивает высвобождение К внутрь, а Na наружу и возврат в исходное состояние. Таким образом, одна молекула АТФ обеспечивает перенос трех молекул Na и двух К.
Транспорт протонов происходит на внутренних энергосопрягающих мембранах (мембранах митохондрий, хлоропластов). Перенос Н осуществляется тремя механизмами: 1) с помощью подвижного переносчика-ионофора, 2) за счет конформационных переходов мембранного белка при связывании Н на одной стороне и испускании на другой, 3) по протонным каналам. Протонная АТФаза содержит 4 субъединицы и является самой сложной из всех АТФаз.






