1s2 2s2 2p6 3s2 3p6 3d10 4s2 ?
Составьте формулу его высшего оксида, определите его характер.
8. В ряду элементов Cl – Br – I неметаллические свойства:
а) усиливаются;
б) не изменяются;
в) ослабевают;
г) нет верного ответа
9. Порядковый номер элемента показывет:
а) атомную массу;
б) число нейтронов в ядре;
в) заряд ядра;
г) нет верного ответа
10. Элемент №14 может проявлять валентность:
а) IV;
б) II, VI;
в) II, IV;
г) IV,VI
11. Сколько литров газа выделяется при при реакции 10,6г карбоната натрия с соляной кислотой? (н.у.)
Вариант 9
1. Как можно определить число электронов на внешнем уровне у элементов главных подгрупп:
а) по номеру периода;
б) по номеру группы;
в) по номеру элемента;
г) нет верного ответа
2. У какого элемента наиболее ярко выражены неметаллические свойства:
а) сера;
б) кислород;
в) селен;
г) теллур
3. Какой элемент образует высший оксид Э2О5 и гидроксид HЭО3:
а) хлор;
б) азот;
в) иод;
г) стронций
4. Сколько электронов на внешнем уровне в атоме элемента №31:
а) 2;
б) 3;
в) 4;
г) 6
5. Какая формула соответствует конфигурации атома кремния:
а) 1s2 2s2 2p2;
б) 1s2 2s2 2p6 3s2;
в) 1s2 2s2 2p6 3s2 3p2;
г) 1s2 2s2 2p6
6. Атом какого элемента имеет строение внешнего уровня 2s2 2p1:
а) №13; б) №15; в) №5; г) №7
7. В состав амфотерного гидроксида Э(OH)3 входит:
а) натрий;
б) кальций;
в) алюминий;
г) бром
8. Из данных элементов Sn, Sb, Te, I самыми сильными неметаллическими свойствами обладает:
а) Sb;
б) I;
в) Sn;
г) Te
9. Какие элементы cодержатся в главной подгруппе VI группы? Напишите формулы их высших оксидов и укажите их характер. Какой из этих элементов обладает наиболее сильными неметаллическими свойствами?
а) Po;
б) S;
в) O;
г) Te
10. Элемент №15 может проявлять валентности:
а) III и II;
б) III и VI;
в) II и IV;
г) III и V
11. Cколько грамм осадка образуется при реакции 8г гидроксида натрия с сульфатом железа (III)?
Вариант 10
1. Какой из элементов находится в главной подгруппе периодической системы:
а) №21;
б) №47;
в) №26;
г) нет верного ответа
2. Как изменяются свойства элементов в главных подгруппах:
а) металлические ослабевают;
б) неметаллические усиливаются;
в) не изменяются;
г) металлические усиливаются
3. Чем определяется место элемента в периодической системе:
а) массой атома;
б) зарядом ядра атома;
в) числом нейтронов в ядре;
г) нет верного ответа
4. Какова формула высшего оксида и гидроксида элемента №16:
а) Э2O3 и H2ЭO4;
б) ЭO3 и H2Э;
в) ЭO3 и H2ЭO4;
г) Э2O3 и H2ЭO3
5. Какая формула соответствует конфигурации атома алюминия:
а) 1s2 2s2 2p1;
б) 1s2 2s2 2p6 3s1;
в) 1s2 2s2 2p6 3s2 3p1;
г) 1s2 2s2 2p6
6. Атом какого элемента имеет строение внешнего уровня 2s2 2p3:
а) №9;
б) №11;
в) №20;
г) №7
7. С оксидом какого элемента взаимодействует оксид углерода (IV):
а) №14;
б) №16;
в) №20;
г) №17
8. Как изменяются неметаллические свойства в ряду Al – Si – P – S:
а) ослабевают;
б) не изменяются;
в) усиливаются;
г) нет верного ответа
9. Валентные электроны элемента с №88 находятся на орбиталях:
а) 7s27p1;
б) 8s2;
в) 7s2;
г) нет верного ответа
10. Элемент №6 может проявлять валентности:
а) II, VI; б) I, III, V; в) II, IV; г) IV
11. Сколько литров газа выделится при термическом разложении 80г карбоната алюминия?
Типы химической связи.
Степень окисления.
Окислительно-восстановительные реакции
Вариант 1
1. Как называется химическая связь, образующаяся между атомами за счет общих электронных пар:
а) ионная;
б) ковалентная;
в) металлическая
г) водородная
2. Какой из элементов имеет наименьшую ЭО:
а) N;
б) B;
в) Se;
г) O
3. Какая связь образуется между атомами неметаллов с одинаковой ЭО:
а) ионная;
б) металлическая;
в) ковалентная полярная;
г) ковалентная неполярная
4. Назовите вещество с ионной связью:
а) CH4;
б) CaCl2;
в) CO2;
г) нет верного ответа
5. Укажите вещество с ковалентной полярной связью:
а) NaF;
б) HI;
в) C;
г) MgO
6. Строение вещества изображается условно А+В-. Какого типа связь между частицами вещества:
а) ковалентная полярная;
б) ковалентная неполярная;
в) ионная;
г) металлическая
7. Как изменяется электроотрицательность элементов с ростом заряда ядра в группах, в главных подгруппах:
а) не изменяется;
б) усиливается;
в) уменьшается;
г) периодически повторяется
8. В каком из перечисленных соединений углерод имеет степень окисления +4:
а) Na2CO3;
б) CH4;
в) K4C;
г) СО
9. Определите степень окисления хлора в соединении NaClO2:
а) +2;
б) +3;
в) +4;
г) +1
10. Какой элемент называется окислителем:
а) отдающий электроны;
б) принимающий электроны;
в) не изменяющий степень окисления;
г) проявляющий степень окисления 0
11. Какой процесс называется окислением:
а) отдачи электронов;
б) присоединения электронов;
в) обмена электронами;
г) перехода электронов
12. Какая из реакций является окислительно-восстановительной:
а) CuO + H2 = Cu + H2O;
б) MgO + 2HJ = MgJ2 + H2O;
в) 2NaOH + H2SO4 = Na2SO4 + 2H2O;
г) FeCl2 + 2KOH = Fe(OH)2↓ + 2KCl
13. Какой из перечисленных процессов является окислением:
а) S-2 ® S+4;
б) S+6 ® S+4;
в) S+4 ® S0;
г) S+4 → S+2
14. Какой из данных элементов является восстановителем:
а) S0 ® S+4;
б) N+5 ® N+2;
в) Mg+2 ® Mg0;
г) C+4 → C+2
15. В какой реакции сера является восстановителем:
а) H2 + S = H2S;
б) 2SO2 + O2 = 2SO3;
в) Zn + H2SO4 = ZnSO4 + H2;
г) нет верного ответа
16. Сколько литров газа выделится при реакции 2,3г натрия с серной кислотой при н.у.:
а) 1,12л;
б) 11,2л;
в) 2,24л;
г) 4,48л
Вариант 2
1. Как называется способность атомов оттягивать к себе электроны от других атомов в соединениях:
а) металличность;
б) валентность;
в) степень окисления;
г) электроотрицательность
2. Какой из элементов имеет наибольшую ЭО:
а) N;
б) As;
в) Se;
г) F
3. Какая связь образуется между атомами с резко отличающейся ЭО:
а) ионная;
б) металлическая;
в) ковалентная полярная;
г) ковалентная неполярная
4. Назовите вещество с ионной связью:
а) Na;
б) S;
в) H2S;
г) CuCO3
5. Укажите вещество с ковалентной полярной связью:
а) SiO2;
б) P;
в) KBr;
г) CaO
6. Строение молекулы изображено условно Аб+:Вб- Какого типа связь наблюдается между частицами вещества:
а) ковалентная полярная;
б) ковалентная неполярная;
в) ионная;
г) нет верного ответа
7. Как изменяется электроотрицательность с ростом заряда ядра в периодах:
а) не изменяется;
б) усиливается;
в) уменьшается;
г) повторяется периодически
8. В каком из перечисленных соединений углерод имеет степень окисления +4:
а) CO2;
б) Al3C4;
в) CO;
г) С
9. Определите степень окисления хлора в соединении KClO3:
а) +1;
б) +2;
в) +3;
г) +5
10. Какой элемент называется восстановителем:
а) не изменяющий степень окисления;
б) отдающий электроны;
в) принимающий электроны;
г) изменяющий степень окисления
11. Какой процесс называется восстановлением:
а) отдача электронов;
б) приём электронов;
в) переход электронов;
г) обмен электронами
12. Какая из реакций является окислительно-восстановительной:
а) 3MgO + P2O5 = Mg3(PO4)2;
б) Zn + H2SO4 = ZnSO4 + H2;
в) 2KOH + H2S = K2S + 2H2O;
г) CaCl2 + 2AgNO3 = 2AgCl↓ + Ca(NO3)2
13. Какой из перечисленных процессов является окислением:
а) Mg0 ® Mg+2;
б) N+3 ® N+2;
в) N+5 ® N+4;
г) P+5 → P0
14. Какой из данных элементов является восстановителем:
а) Zn+2 ® Zn0;
б) Al0 ® Al+3;
в) P+5 ® P+3;
г) Ba+2 → Ba0 .
15. В какой реакции сера является восстановителем:
а) Cu + 2H2SO4 = CuSO4 + SO2 + 2H2O;
б) Mg + S = MgS;
в) 2SO2 + O2 = 2SO3;
г) нет верного ответа
16. Сколько литров газа выделится при реакции 3,9г. калия с соляной кислотой при н.у.:
а) 3,36л;
б) 1,12л;
в) 22,4л;
г) 4,48л
Электролитическая
Диссоциация
Вариант 1
1. Какие растворы проводят электрический ток?
а) раствор хлорида калия в воде;
б) раствор хлорида натрия в бензоле;
в) раствор бромида меди в ацетоне;
г) раствор сахара в воде;
2. Какое вещество диссоциирует в соответствии с данной схемой?
 |  | ||||||
 | |||||||
 | |||||||





 +
+
а) Вг2; б) НВr; в) КВr; г) К2S
3. Диссоциации какого вещества соответствует приведенное уравнение?
Н2А = 2Н+ + А2- (А — кислотный остаток)
а) Н2S, б) Н2O, в) НС1, г) правильного ответа нет
4. При диссоциации какого вещества не образуются гидроксид-ионы?
а) NаОН, б) Ca(NO3)2, в) Са(ОН)2 , г) АlOНSO4
5. Какое из приведенных веществ является слабым электролитом?
а) Nа2S04 , б) HNO3 , в) Н2S, г) НС1
6. Индикатор лакмус изменит окраску в водном растворе:
а) гидроксида железа (III)
б) гидроксида кальция
в) гидроксида цинка
г) гидроксида алюминия
7. Какие ионы могут находиться в растворе одновременно?
а) Nа+, Ва2+, NO 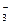 , ОН-
, ОН-
б) Н+, К+, С1-, ОН-
в) Ва2+ ,ОН-, СО 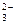 , С1-
, С1-
г) Н+, SO 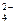 , НSO
, НSO 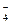 , SiO
, SiO 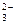
8. Водный раствор сульфата меди (II) не будет взаимодействовать с:
а) раствором КС1
б) раствором BaCl2
в) Fe
г) раствором NаОН
9. Гидроксид железа (III) будет взаимодействовать с:
а) раствором Nа2SO4
б) раствором NаОН
в) раствором НNОз
г) Са3(РO4)2
10. Разбавленная серная кислота будет реагировать с:
а) АgС1, б) NаС1, в) Н2S, г) Nа2S
11. Карбонат кальция образуется при реакции ионного обмена между:
а) СаО и СO2
б) раствором СаCl2 и раствором Nа2СОз
в) Са и Н2СОз
г) раствором Са(ОН)2 и ВаСОз
12. Гидроксид цинка можно получить взаимодействием:
а)Zn и Н2O, б) ZnO и Н2O, в) раствора Zn(NОз)2 и раствора КОН
г) раствора ZnCl2 и Н2SiOз
13. Составьте полное и сокращенное ионное уравнения реакций между гидроксидом железа (II) и азотной кислотой. Найдите суммы всех коэффициентов в полном и сокращенном ионном уравнениях соответствено:
а) 8 и 6, б) 10 и 6, в) 12 и 6, г) 12 и 3
14. Ионное уравнение Zn2+ + S2- = ZnS ¯
соответствует взаимодействию между:
а) Zn и S, б) Zn(ОН)2 и Н2S, в) раствором ZnCl2 и СuS, г) раствором Zn(NОз)2 и раствором К2S
15. Найдите количество вещества, выпадающего в осадок при сливании раствора, содержащего 0,2 моль хлорида железа (III), и раствора, содержащего 0,3 моль гидроксида натрия.
а) 1 моль, б) 0,1 моль, в) 0,2 моль, г) 0,3 моль






