Адиабатическим называется процесс, при котором отсутствует теплообмен (dQ=0) между системой и окружающей средой. К адиабатическим процессам можно от-
нести все быстропротекающие процессы. Например, адиабатическим процессом можно считать процесс распространения звука в среде, так как скорость распространения звуковой волны настолько велика, что обмен энергией между волной и средой произойти не успевает. Адиабатические процессы применяются в двигателях внутреннего сгорания (расширение и сжатие горючей смеси в цилиндрах), в холодильных установках и т. д.
Из первого начала термодинамики (dQ=dU+dA) для адиабатического процесса следует, что
dA=-dU, (55.1)
т. е. внешняя работа совершается за счет изменения внутренней энергии системы.
Используя выражения (52.1) и (53.4), для произвольной массы газа перепишем уравнение (55.1) в виде
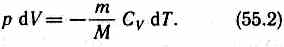
Продифференцировав уравнение состояния для идеального газа pV=(m/M)RT, получим

Исключим из (55.2) и (55.3) температуру Т:

Разделив переменные и учитывая, что Ср/Сv =g (см. (53.8)), найдем
dp/p=-gdV/V.
Интегрируя это уравнение в пределах от р 1до р 2и соответственно от V 1до V 2, а затем потенцируя, придем к выражению
p 2 /p l=(V1/V2)g.
или
p 1vg1 = p 2vg2.
Так как состояния 1 и 2 выбраны произвольно, то можно записать
рVg= const. (55.4)
Полученное выражение есть уравнение адиабатического процесса, называемое также уравнением Пуассона.
Для перехода к переменным Т, V или р, Т исключим из (55.4) с помощью уравнения Клапейрона — Менделеева
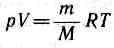
соответственно давление или объем:

Выражения (55.4) — (55.6) представляют собой уравнения адиабатического процесса. В этих уравнениях безразмерная величина (см. (53.8) и (53.2))
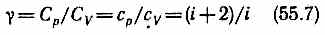
называется показателем адиабаты (или коэффициентом Пуассона). Для одноатомных газов (Ne, He и др.), достаточно хорошо удовлетворяющих условию идеальности, i = 3, g=1,67. Для двухатомных газов (Н2, N2, O2 и др.) i= 5, g=1,4. Значения g, вычисленные по формуле (55.7), хорошо подтверждаются экспериментом.
Диаграмма адиабатического процесса (адиабата) в координатах р, V изображается гиперболой (рис.83). На рисунке видно, что адиабата (pVg=const) более крута, чем изотерма (pV =const). Это объясняется тем, что при адиабатическом сжатии 1 — 3 увеличение давления газа обусловлено не только уменьшением его объема, как при изотермическом сжатии, но и повышением температуры.

Вычислим работу, совершаемую газом в адиабатическом процессе. Запишем уравнение (55.2) в виде

Если газ адиабатически расширяется от объема V 1до V 2, то его температура уменьшается от T 1до T 2и работа расширения идеального газа

Применяя те же приемы, что и при выводе формулы (55.5), выражение (55.8) для работы при адиабатическом расширении можно преобразовать к виду

Работа, совершаемая газом при адиабатическом расширении 1 — 2 (определяется площадью, выполненной в цвете на рис. 83), меньше, чем при изотермическом. Это объясняется тем, что при адиабатическом расширении происходит охлаждение газа, тогда как при изотермическом — температура поддерживается постоянной за счет притока извне эквивалентного количества теплоты.
Рассмотренные изохорный, изобарный, изотермический и адиабатический процессы имеют общую особенность — они происходят при постоянной теплоемкости. В первых двух процессах теплоемкости соответственно равны Cv и С р, в изотермическом процессе (d T= 0)теплоемкость равна ±¥, в адиабатическом (dQ=0) теплоемкость равна нулю. Процесс, в котором теплоемкость остается постоянной, называется политропным.
Исходя из первого начала термодинамики при условии постоянства теплоемкости (C = const) можно вывести уравнение политропы:
pVn = const, (55.9)
где n= (C- Ср)/(С-Cv) — показатель политропы. Очевидно, что при С = 0, n=g из (55.9) получается уравнение адиабаты; при С=¥, n=1 —уравнение изотермы; при С=СР, n = 0 — уравнение изобары, при С = Сv, n =±¥ —уравнение изохоры. Таким образом, все рассмотренные процессы являются частными случаями политропного процесса.






