Для розуміння хімічної структури і властивостей білків важливе значення має вивчення хімічної природи і властивостей їх елементарних ланок — амінокислот. У природі виявлено багато різних амінокислот, проте до складу більшості білків їх входить лише 20. Близько 10 амінокислот зустрічається у білках досить рідко. Всі амінокислоти, що входять до складу білків, часто називають протеїногенними. Решта
IS
Таблиця 4. Незамінні (:), напівнезамінні (±) і замінні (—) амінокислоти, необхідні для деяких видів організмів (за Любке та ін.)
| Потреба в амінокислотах | |||||||
| Амінокислота | X І X і | щурів | І Z | лосося | я І | Ті |
| — | — | ± | — | + | — |
| + | — | 4- | + | 4- | + |
| — | 4- | 4- | 4- | 4- | |
| + | + | ~ | 4- | 4- | -г |
| + | + | + | 4- | + | 4~ |
| + | + | 4- | + | 4- | 4- |
| і | 4- | 4- | j_ | ||
| ± | ± | + | 4- | 4- | |
| + | + | + | + | т | + |
| ± | ± | 4- | — | — | — |
| + | 4- | 4- | f | + | 4- |
| + | Т" | 4- | 4- | • + | 4- |
Гліцин —
Аланін —
Валін +
Лейцин +
Ізолейцин 4"
Цистеїн —
Метіонін -f-
Сернн —
Треонін -f-
Аспарагінова кислота —
Глутамінова кислота —
Лізин 4-
Аргінін ±
Фенілаланін -f
Тирозин ±
Гістидин ±
Триптофан 4-
Пролін —
амінокислот входить до складу фізіологічно активних речовин (гормонів, коферментів, антибіотиків) або знаходиться в органах та тканинах тварин і рослин у вільному стані — непротеїнпге^ні.
Усі амінокислоті/, які виявлено в складі білка, синтезуються в рослинних організмах. В організмі людини і тварин синтезується лише частина протеїногенних амінокислот, а деякі з них утворюються в недостатній кількості для нормального синтезу білка. В зв'язку з ним усі п ротеїногенні аміноки слоти поділяють на три групи: незамінні, напівіТеламінні і замінні.
Незамі ін — не такі амінокислоти, які в організмі
не синтезуються. Тому вони повинні обов'язково поступати в організм ззовні, в основному з їжею. Для організму людини повністю незамінними є вісім амінокислот: валін, лейцин, ізолейцин, треонін, лізин, метіонін, фенілаланін і триптофан.
До наиівдеІДМІннихдіалежать амінокислоти, які синтезуються в організмі в недостатній кількості. Такі амінокислоти повинні частково поступати з організм з їжею. Для організму людини такими амінокислотами є аргінін, тирозин і гістидин.
Заміни кислоти синтезуються в організмі з цілого ряду ор-
ганічних сполук, в тому числі з деяких амінокислот. Організм може певний час обходитися без таких амінокислот при умові, що з їжею поступатимуть речовини, з яких синтезуються замінні амінокислоти.
Разом з цим необхідно зауважити, то для деяких організмів необхідна більша кількість незамінних амінокислот, ніж вісім (табл. 4). Так, для організму щурів і мишей необхідно дев'ять незамінних амінокислот (до восьми вищеназваних амінокислот додається ще одна — гістидин). 6 певні відхилення і щодо визначення напівнезамінних амінокислот. Дані табл. 4 свідчать про те, що для різних видів організмів мають місце свої особливості у визначенні незамінних, напівнезамінних і замінних амінокислот.
Амінокислоти — похідні карбонових кислот аліфатичного або ароматичного ряду, в молекулах яких один чи кілька атомів водню заміщені на аміногрупу. Залежно від того, біля якого вуглецевого атома заміщено атом водню, розрізняють а-, р- і "^-амінокислоти.
В амінокислотах, які входять до складу білків, аміногрупа розміщена біля а-вугленевого атома, тобто усі вони є а-амінокислотами. Загальну формулу амінокислот можна записати так:
#_сн-соон.
І
Амінокислоти відрізняються між собою лише хімічною природою радикалів. Радикал — це угруповання атомів у молекулі амінокнс-
Таблиця 5. Фізичні властивості амінокислот
| Амінокислота | І зо- | |||||
| Молеку- | Розчинність | Температура | ||||
| лярна | в 100 г води | плавлення. | ря Ч НІ | |||
| назва | позначення | маса | при 25 fC | "С | ТОЧКа | |
| (РН) | ||||||
| Аланін | Ала | Ala A | 89,06 | 16,51 | 297 (розкл.) | 6,0 |
| Аргінін | Apr | Arq R | 174,14 | 15,00 | 10,76 | |
| Аспарагінова | ||||||
| кислота | Асп | Asp N | 133,06 | 0,50 | 2,77 | |
| Валін | Вал | Val V | 117,09 | 8,85 | 5,96 | |
| Гістидин | Гіс | His H | 155,09 | 4,29 | 7,59 | |
| Гліцин | Глі | Gly G | 75,05 | 24,99 | 5,97 | |
| Глутамінова кис- | ||||||
| лота | Глу | Glu E | 147,08 | 0,84 | 3,22 | |
| Ізолейцин | Іде | lie 1 | 131,11 | 4,12 | 280 (розкл.) | 6,02 |
| Лейцин | Лей | Leu L | 131,11 | 2,19 | 5,98 | |
| Лізин | Ліз | Lys К | 146,13 | Добра | 9,74 | |
| Метіонін | Мет | .Met M | 149,15 | 3,35 | 5,74 | |
| Пролін | Про | Pro P | 115,08 | 16,23 | 5,68 | |
| Серни | Сер | Ser S | 105,06 | 5,02 | 5,68 | |
| Тирозин | Тир | Туг У | 181,09 | 0,05 | 310 (розкл.) | 5,66 |
| Триптофан | Три | Trp W | 204,11 | 1,14 | 5,89 | |
| Трсонін | Тре | Thr T | 119,08 | 20,05 | 5,16 | |
| Цистеїн | Цис | Cys С | 121,12 | Дуже лобра | 258 (розкл.) | 5.07 |
| Цистин | Цис | 240,23 | 0,01 | 4,60 | ||
| Фенілаланін | Фен | Flie F | 165.09 | 3,00 | 283 (розкл.) | 5,91 |
| Аспарагін | Асн | Asn N | 132,22 | Г>,41 | ||
| Глутамін | Глн | Gin Q | 146,15 | 5,65 |
лоти, що зв'язане з а-вуглеиевим атомом, яке не бере участі у формуванні остова пол і пептид ного ланцюга. Радикалами є залишки жирних кислот, ароматичні ядра, різні гетероцикли та ін.
З білків виділено також амінокислоти, які містять більше ніж одну змінну або карбоксильну групу. При наявності у складі амінокислоти двох амі ногру ті одна з них розміщується в а-положенні, а друга —в (о-іюложенні, тобто біля першого вуглецевого атома з протилежного кінця від а-аміногрупи. Крім того, із продуктів гідролізу білків виділено амінокислоти, які містять групу — NH замість групи — NH2 і дістали назву імінокис.ют.
Виділені з білків амінокислоти — це безбарвні, кристалічні речовини, переважна більшість яких добре розчинна у воді і погано розчинна в органічних розчинниках. Основні фізичні константи амінокислот наведено в табл. 5, з якої видно, що усі амінокислоти плавляться при температурі, вищій ніж 200 СС, причому деякі з них при нагріванні розкладаються.
Амінокислоти є оптично активними сполуками. Тому кожна молекула амінокислоти може бути правообертаюча, яку позначають знаком плюс (+), або лівообертаюча, яку позначають знаком мінус (—).
Конфігурацію амінокислот визначають у порівнянні з гліцериновим альдегідом. Відомо D- і L-форми гліцеринового альдегіду:
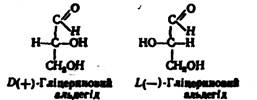
Якщо розташування атома водню біля вуглецю в а-положенні амінокислоти подібне до розташування водню в тому самому положенні D-гліцеринового альдегіду, то амінокислота належить до D-ряду. Якщо ж розміщення атома водню амінокислоти відповідає £-формі гліцеринового альдегіду, то і амінокислота належить до L-ряду:

D-Форма гліцеринового альдегіду завжди обертає площину поляризації вправо (■+•), а L-форма — вліво (—). Однак для деяких сполук, у тому числі і амінокислот, знаки D і L не співпадають, з напрямом обертання площини поляризації'. Разом з тим слід підкреслити, що знаки D і L характеризують не оптичну активність амінокислот, а на-
гл
лежність їх до групи споріднених сполук, які мають однакову просторову конфігурацію біля а-вуглецевого атома.
|
У тому випадку, коля в молекулі амінокислот є два центри асимет
рії, і якщо конфігурація другого асиметричного атома відрізняється
від конфігурації а-вуглецевого атома, то після знаків D і L ставиться
префікс алло. Зокрема, такі амінокислоти, як треонін, цистин і ізолей
цин, мають два центри асиметрії. Тому при хімічному синтезі цих
амінокислот одержують суміш чотирьох стереоізомерів. Два з них
позначають як D- і L-форми, а два інших, діастереоізомери, як D-алло-
і L-ялло-форми. Так, для треоніну відомі такі чотири стерео ізомер ні
форми: л
СООН СООН
NH2-C-H
СН3 СН3
і-алло-Треонін D-алло-Треонін
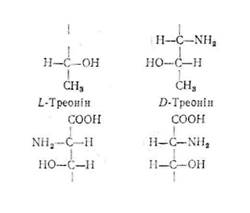
Необхідно підкреслити, що в білках рослинного і тваринного походження знайдено переважно амінокислоти L-ряду. Одна частина з них обертає площину поляризації вправо, а друга — вліво, тому біля D і L ставлять знак (+) або (—):
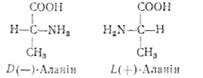
Оптичними антиподами природних амінокислот є амінокислоти D-ряду, які добувають у результаті хімічного синтезу. Зараз Оч{юр-ми деяких амінокислот виявлено як у вільному стані, так і в складі деяких антибіотиків, мікроорганізмів.
За певних умов може відбуватися зміна конфігурації груп — Н і — NH2 біля асиметричного а-вуглецевого атома амінокислот, внаслідок чого L-амінокислоти частково перетворюються на D-форму. Цей процес має назву рацемізації, а суміші речовини D- і L-ряду називають рацемічними. Застосовуючи спеціальні методи, з цих сумішей можна
виділити один з оптичних ізомерів у чистому вигляді. Процес рацемі-зації амінокислот частково має місце і в організмі людини і вищих тварин. Зокрема, є дані про те, що частина амінокислот L-ряду під дією (|)ерментів рацемаз перетворюється на /^-амінокислоти, але таке перетворення вивчено тільки для аланіну і глутамінової кислоти.
Амінокислоти — це амфотерні сполуки, які містять дві протилежні за властивостями функціональні групи — карбоксильну та змінну. Тому за звичайних умов можлива взаємодія між аміно- і карбоксильною групами амінокислот (у водних розчинах або в кристалічному стані): 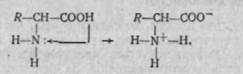
За цих умов молекула амінокислоти перетворюється на диполярний іон (цвіттеріон), який має два протилежних заряди —негативний, утворений внаслідок відщеплення позитивно зарядженого протона від карбоксильної групи, і позитивний, утворений внаслідок приєднання протона до аміногрупи. В результаті внутрішньомолекулярної взаємодії утворюється нейтральна сполука — внутрішня сіль амінокислоти, тому розчини амінокислот у більшості випадків мають нейтральний характер і на індикатори не діють (за винятком амінокислот, які містять у складі молекул кілька аміно- чи карбоксильних груп).
Амінокислоти в розчинах виявляють властивості амфотерних електролітів (амфолітів). Залежно від рН середовища вони можуть мати кислотні або лужні властивості. Так, у кислому середовищі (при надлишку іонів Н+) дисоціація карбоксильної групи пригнічується, молекула амінокислоти при цьому набуває позитивного заряду і реагує як катіон: У лужному середовищі, під дією іонів ОН", іонізація аміногрупи пригнічується, молекула амінокислоти набуває негативного заряду, тобто реагує як аніон:
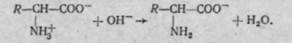
Значення рН середовища, при якому загальний сумарний заряд амінокислоти дорівнює нулю, має назву ізоєлектричної точки. У цьому випадку молекула амінокислоти електронейтральна і в електричному полі ні до анода, ні до катода не рухається. Для різних амінокислот ізоелектрична точка різна і залежить від наявності в їх складі здатних
5-3
до іонізації карбоксо- і аміногруп (див. табл. 5). Крім того, ступінь іонізації карбоксильних груп дещо вищий, ніж аміногруп. Тому ізо-електрична точка моноамінокарбонових кислот знаходиться при рН = = 6. Водні розчини цих амінокислот крім диполярних іонів містять невелику кількість аніонів та іонів водню.
Наявність у складі молекул амінокислот аміно- і карбоксильних груп зумовлює їх участь у хімічних реакціях, характерних для цих груп.
КЛАСИФІКАЦІЯ АМІНОКИСЛОТ
Амінокислоти, які входять до складу білків, часто класифікують за кількістю аміно- і карбоксильних груп (див. схему па с 55).
Зараз широко використовується класифікація амінокислот, яка грунтується на полярності їх радикалів. За цією ознакою амінокислоти поділяють на чотири класи: з неполярними радикалами, з незаря-дженими полярними радикалами, з негативно зарядженими полярними радикалами і з позитивно зарядженими полярними радикалами.
Амінокислоти з неполярними радикалами L +)-Аланін (а-амінопропіонова 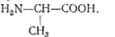 кислота):
кислота):
Вперше аланін було виділено у 1881 р. із фіброїну шовку. Пізніше його було виділено з продуктів гідролізу білків шовку, а також одержано в результаті синтезу. Ця амінокислота часто зустрічається у складі білків рослин і тварин, а також знаходиться у вільному стані. Крім а-аланіну в організмі виявлено також (і-аланін. Однак до складу білків останній не входить. b-Аланін бере участь в утворенні структури пептидів, зокрема дипептидів карнозину та ансерину, які містяться у м'язовій тканині більшості хребетних тварин, та входить до складу вітаміну В3.
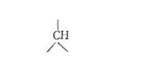
L (+)-Валін (а-аміноізовалеріанова кислота, а-аміно-р-метилмас-
|
ляна кислота):
H2N-CH-COOH
Н3С СН3
Цю амінокислоту виділено з білків підшлункової залози у 1879 р. В організмі тварин і рослин валін входить до складу білків та зустрічається у вільному стані. Значна кількість валіну (4—15 %) міститься у білках — міоглобіні, казеїні.і еластині. В організмі людини і тварин валін не синтезується, і тому для забезпечення нормальних фізіо-
Q5
логічних процесів він повинен постійно надходити з продуктами харчування.
L (— )-Лейцин (а-аміноізокапронова кислота, а-аміно-у-метилвале-ріанова кислота) 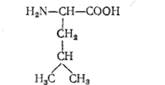
вперше виділено у 1819 р. з сиру. Входить до складу багатьох білків тваринного і рослинного походження. Значна кількість його міститься у пророслому зерні злакових культур. В організмі людини і тварин лейцин не синтезується, тому він повинен постійно надходити з їжею; належить до незамінних амінокислот.
L (-Ь)-Ізолейцин (а-аміно-р-метилвалеріанова кислота):
Ізолейцин відкрито у 1904 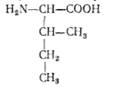 р. і виділено з меляси, а пізніше з фібрину крові. У складі білків міститься в незначних кількостях, належить, як і лейцин, до незамінних амінокислот.
р. і виділено з меляси, а пізніше з фібрину крові. У складі білків міститься в незначних кількостях, належить, як і лейцин, до незамінних амінокислот.
L (— )-Метіонін (а-аміпп-">'-мртіі.птіпмяг-пяня 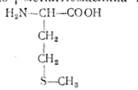 кислота)
кислота)
виділено з казеїну у 1922 р. В організмі відіграє надзвичайно важливу роль як донор метильних груп для забезпечення процесів синтезу холіну, адреналіну; бере участь у процесах утворення цистеїну та інших біологічно активних речовин. В організмі людини і тварин не синтезується. Широко використовується у тваринництві для підвищення продуктивності.
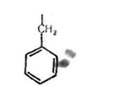
L (—)-Фенілаланін (а-аміно-р-феиілпропіонова кислота):
|
нл-сн-соон
■56
Виділено з білка люпину у 1879 р. В організмі людини і тварин не синтезується. Використовується в процесах синтезу адреналіну і тироксину.
|
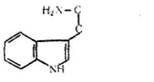
L (—)-Триптофан (а-аміно-р-індолілпропіонова кислота):
н-соон На
Вперше виділено у 1901 р. з продуктів гідролізу казеїну. Міститься в білках рослинного і тваринного походження. В організмах людини і тварин не синтезується і належить до незамінних амінокислот. При декарбоксилюванні триптофану утворюється триптамін, який викликає підвищення кров'яного тиску.
L (— )-Пролін (піролідин-2-карбонова кислота):
Г 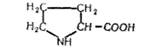
Вперше виділено з казеїну у 1901 р. В організмах людини і тварин синтезується з глутамінової кислоти або орнітину. Пролін міститься майже в усіх білках. Особливо велика кількість його є в колагені, казеїні та інших білках.
Амінокислоти з незарядженими полярними радикалами
Гліцин, або глікокол (а-амінооцтова кислота),
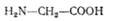
вперше було виділено з желатини у 1820 р. У організмах людини і тварин утворюється з інших амінокислот. Використовується для синтезу глутатіону і гіпурової кислоти, парних жовчних кислот і пуринових основ та інших сполук.
L (— )-Серин (а-аміно-[і-оксипропіонова кислота)
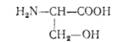
виділено з фіброїну шовку у 1856 р. Синтезується в організмах людини і тварин, є складовою частиною багатьох білків. Серин входить до складу активних центрів таких ферментів, як трипсин, холінестераза; бере участь у синтезі окремих амінокислот та ін.
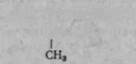
|
L (—)-Треонін (а-аміно-Р-оксимасляна кислота)
H2N-CH-COOH
І СН-ОН
одержано у 1935 р. з фіброїну шовку і казеїну. Входить до складу багатьох рослинних і тваринних білків. Значна кількість треоніну міститься в таких білках, як пепсин, фібрин та ін. Треонін має два асиметричні атоми вуглецю — один у а-положенні, а другий у р-поло-женні. Тому для нього характерні чотири ізомерні форми. В організмі людини і тварин треонін не синтезується.
L (—)-Цистеїн (а-аміно-р-тіолпропіопова 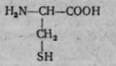 кислота):
кислота):
Цистеїн виділено у 1890 р. з білків покривних тканин тварин. Характерною особливістю цієї амінокислоти є те, що її сульфгідрильна група легко окислюється. При цьому дві молекули цистеїну взаємодіють між собою й утворюють діамінодикарбонову кислоту — цистин ф-|5-дитіо-а-а-діамінопропіонову кислоту):
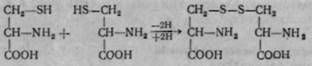
При відновленні цистину відбувається розщеплення його на дві молекули цистеїну. Отже, ці амінокислоти відіграють важливу роль в окислювально-відновних процесах організму.
У значних кількостях цистеїн входить до складу багатьох білків, зокрема білків волосся, нігтів, пір'я та ін.
|
£(+)- Аспарагін
H2N-CH-COOH
CONH2
входить до складу багатьох рослинних і тваринних білків. Особливо багато аспарагіну нагромаджується в паростках бобових рослин. £(-|-)-Глутамін: 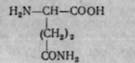
Аспарагін і глутамін відіграють важливу роль у процесах обміну в організмі, особливо в процесах зв'язування аміаку і транспорту його до місця синтезу сечовини.
|
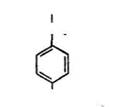
L (—)-Тирозин (а-аміно-р-параоксифенілпропіонова кислота)
H2N-CH-COOH СН,
Он
виділено з казеїну у 1846 р. Входить до складу різних білків, особливо велика кількість його є в інсуліні великої рогатої худоби (до 12,5 %) і пепсині (до 8,5 %). У організмі людини і тварин тирозин утворюється при окисленні фенілаланіну і використовується в процесах синтезу гормонів — тироксину, адреналіну і норадреналіну тощо.
Амінокислоти з негативно зарядженими полярними радикалами
L (+)-Аспарагінова кислота (а-аміноянтарна кислота)
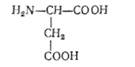
вперше виділена у 1868 р. з рослинних білків. Особливо високий вміст її було виявлено в соку спаржі (звідси і походить її назва). Аспарагінова кислота синтезується в організмах людини і тварин, входить до складу багатьох білків рослинного і тваринного походження. Вона використовується в процесах синтезу азотистих основ нуклеїнових кислот і сечовини, знешкодження аміаку, переамінування амінокислот та ін.
L (-|-)-Глутамінова кислота (а-аміноглутарова кислота)
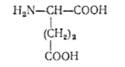
Глутамінову кислоту вперше було виділено у 1866 р. з гідролізату клейковини пшеничного зерна. Вона знаходиться як у складі білків, так і у вільному стані. Зокрема, високим вмістом глутамінової кислоти характеризуються альбуміни і глобуліни крові, колаген та інші
білки. Глутамінова кислота, як і аспарагінова, бере участь у багатьох обмінних процесах організму — в дезамінуванні, переамінуван-ні, декарбоксилюванпі амінокислот. З неї утворюється важливий медіатор нервової системи — у-аміномасляна кислота та інші важливі спо- • луки, зокрема глутамін. Натрієва сіль глутамінової кислоти широко використовується в харчовій промисловості для поліпшення смакових якостей харчових продуктів.
Амінокислоти з позитивно зарядженими полярними радикалами
L (+)-Лізин (а, е-діамінокапронова кислота)
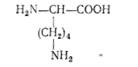
виділено у 1889 р. з казеїну. Входить до складу всіх білків; в організмах людини і тварин не синтезується і належать до незамінних амінокислот. Багато лізину міститься в білках ядер — протамінах і гіс-топах.
Зараз лізин добувають у результаті хімічного синтезу, його використовують для підвищення продуктивності сільськогосподарських тварин.
L (+)-Аргінін (а-аміно-а-гуанідинвалеоіанова кислота)
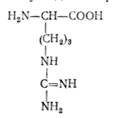
виділено у 1886 р. з паростків люпину. Високий вміст аргініну (до 84 % загальної маси амінокислот) виявлено в спермі риб. Аргінін відіграє досить важливу роль в обміні речовин, зокрема в процесах утворення сечовини, креатину та інших речовин. Аргінін постійно синтезується в організмі людини і тварин.
L (—)-Пстидин (а-аміно-р-імідазолпропіонова кислота)
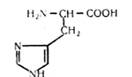
 виділено у 1896 p. з сперми осетра і казеїну. У значних кількостях гістидин міститься в тканинах печінки, нирок та в гемоглобіні крові. З гістидину при його декарбоксилюванні утворюється важливий біогенний амін — гістамін, який сприяє розширенню кровоносних судин та секреції соляної кислоти в шлунку.
виділено у 1896 p. з сперми осетра і казеїну. У значних кількостях гістидин міститься в тканинах печінки, нирок та в гемоглобіні крові. З гістидину при його декарбоксилюванні утворюється важливий біогенний амін — гістамін, який сприяє розширенню кровоносних судин та секреції соляної кислоти в шлунку.
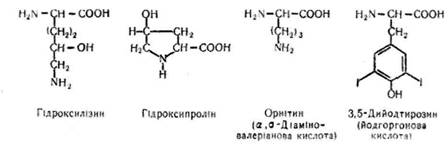
Дослідження амінокислотного складу свідчать про те, що деякі амінокислоти входять до складу лише окремих білків. Це такі амінокислоти, як гідроксилізин, гідроксипролін, 3,5-дийодтирозин, оксилі-зин, орнітин та ін.:
|
Гідроксилізин і гідроксипролін входять до складу колагену і желатини. У складі білка тиреоглобуліну виявлено амінокислоту 3,5-днйод-тирозин, а в білках окремих субклітинних структур — похідні лізину та аргініну.
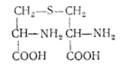
До амінокислот, які рідко зустрічаються у складі білків, відноситься також лантіонін, виділений з гідролізатів шерсті і деяких антибіотиків. Він належить до діамінодикарбонових кислот, тобто містить дві аміно- і дві карбоксильні групи:
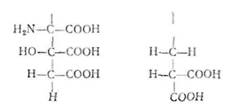
Немає сумніву в тому, що з часом буде відкрито ще ряд амінокислот. Зокрема, з білків нуклеопротеїдних комплексів різних органів — тимусу, селезінки, а також з рибосом клітин тварин — виділено дві амінокислоти — амінолимопну і ^-карбоксіаспарагінову:
|
Н Н
н2\-с-соон
Ці амінокислоти містять по три карбоксильні групи і мають високий негативний заряд. Роль цих амінокислот у метаболічних процесах організму поки що не встановлено.
Основні способи добування амінокислот
Дослідження амінокислотного складу білків різних органів і тканин рослин і тварин свідчать про те, що вільних амінокислот у природі дуже мало. Добувають амінокислоти гідролізом білків, а також хімічним та мікробіологічним синтезом. Нині розрізняють три види гідролізу білків — кислотний, лужний і ферментативний. У лабораторних і заводських умовах найчастіше використовують кислотний гідроліз, внаслідок чого утворюється суміш амінокислот, які входили до складу білка. Окремі амінокислоти з гідролізату виділяють різними методами: осадженням, розділенням на спеціальних смолах, а також методами електрофорезу і хроматографії. Проте гідролізом можна добути не всі "амінокислоти, а в основному ті, які входять до складу білків у значних кількостях. Цим способом виділяють гліцин з желатину, глутамі-нову кислоту з казеїну та клейковину із злаків, тирозин з фіброїну шовку, цистин і цистеїн з шерсті, гістидин з білків крові тощо. Однак відносно висока собівартість і дефіцитність вихідної сировини, а також багатоступенева хімічна обробка її (пов'язана з виділенням амінокислот і їх очисткою) не дає поки що можливості широко використовувати цей спосіб у промисловості. Разом з цим кислотний гідроліз білків часто супроводжується руйнуванням деяких амінокислот — триптофану, треоніну, серину, цистеїну (за даних умов окислюється до цистину). Певні недоліки характерні і для ферментативного гідролізу білків. Зокрема, гідроліз може бути неповним і фермент при цьому може розкладатися, утворюючи відповідні амінокислоти.






