
 Типичный вид температурной кривой правильно поставленного калориметрического опыта при измерении экзотермического эффекта показан на рис. 2. Расчет величины изменение температуры в ходе химической реакции DT с учетом теплообмена по закону Ньютона производится графическим методом.
Типичный вид температурной кривой правильно поставленного калориметрического опыта при измерении экзотермического эффекта показан на рис. 2. Расчет величины изменение температуры в ходе химической реакции DT с учетом теплообмена по закону Ньютона производится графическим методом.
На миллиметровой бумаге построить зависимость температуры (°С) от времени (с). На оси абсцисс откладывается время в масштабе 1 с = 1 мм, на оси ординат – температуру в масштабе 1°С = 5 см (рис. 2). После того как на график нанесены все экспериментальные точки, получается кривая ABCD. Участок AB называется начальным периодом, BC - главным, CD - конечным. Чтобы определить DT, не искаженное тепловым обменом, происходящим в течение времени главного периода, продолжают линии AB и CD до пересечения с вертикальной прямой EF. Для этого точки m и n, соответствующие начальной и конечной температурам главного периода, наносят на ось ординат. Через середину отрезка mn проводят линию KP. Пересечение этой линии с кривой BC дает точку g, определяющую положение прямой EF. Отрезок EF будет равен DT.
Характер линии BC зависит от условий протекания теплового процесса (например, от смешивания), наклон кривой AB и CD зависит от характера теплообмена с окружающей средой.
Таблица 2
| Раствор | DT1 | DT2 | DT3 | 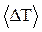
| K, кДж/град | Q, кДж | Θ | e |
| HCl + NaOH | -57,36 | |||||||
| CH3COOH + NaOH | ||||||||
| HCl + NH4OH |
Расчет систематической погрешности
Систематическая погрешность проведенных измерений возрастания температуры раствора в ходе реакции при доверительной вероятности 0.95 определяется по формуле:
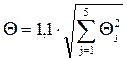
где Θj систематическая погрешность всех использованных средств измерения:
· погрешность термометра Q1 = 0,1%;
· погрешность пипетки Q2 = Q3 = 2%;
· концентрации стандартных растворов кислоты и основания Q4 = Q5 = 0,1%.
Расчет погрешности в определении теплового эффекта реакции
Погрешность в определении теплового эффекта исследуемой реакции определяется как погрешность косвенных измерений из выражения

Погрешность в определении теплового эффекта калибровочной реакции, известного с большой точностью может быть близкой к нулю. Погрешности в определении возрастания температуры раствора в ходе реакции нейтрализации e (DТ0) и e (DТ1,2), как показывает практика, определяется систематической погрешностью Q. Таким образом, погрешность в определении теплового эффекта может быть рассчитана по формуле

Содержание и оформление отчета
Отчет о проведенной работе должен включать:
1. Постановку цели работы;
2. Краткие теоретические основы метода калориметрии;
3. Описание экспериментальной установки;
4. Результаты измерений температуры в ходе проведения калибровочной и исследуемой реакций в виде таблиц;
5. Расчет погрешности измерений;
6. Выводы.
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ
1) Как описывается первый закон термодинамики при протекании изопроцессов различного типа?
2) Как связан закон Гесса с первым законом термодинамики?
3) Какие следствия закона Гесса Вы знаете?
4) Что называется теплотой образования соединения?
5) В чем заключается метод калориметрии?
6) Какие типы калориметров Вы знаете?
7) Для чего необходимо проводить калибровку калориметрической установки при адиабатическом способе измерения?
8) Какие причины обуславливают погрешность измерения в данной работе?






