Лабораторна робота № 21
СПОСТЕРЕЖЕННЯ СПЕКТРІВ ЗА ДОПОМОГОЮ СПЕКТРОСКОПА
ТА ВИЗНАЧЕННЯ ПОСТІЙНОЇ РІДБЕРГА
Мета роботи: Вивчення спектральних закономірностей, вивчення
спектроскопа.
Прилади і матеріали: 1.Спектроскоп двотрубний;
2. Газонаповнені трубки з гелієм і воднем;
3. Ртутно-кварцева лампа;
4. Штатив з тримачем, в який вставлені газонаповнені трубки;
5..Індукційна котушка (Румкорфа);
6. Набір кольорових стекол;
7. Випростувач;
8. Настільна лампа.
Література: 1. Кортнев А.В. і ін. Практикум по физике. – 1963. – робота № 81, 82.
2. Яворський Б.М., Детлаф А.А. Курс фізики.Т.3. – 1971. – § 13.3, 13.4.
Теоретична частина
Видиме світло являє собою електромагнітні хвилі, довжина яких перебуває в межах приблизно 0,4-0,75 мікрона. Довжина хвилі червоного світла – 0,7 мк, а довжина хвилі фіолетового світла – 0,4 мк. У вакуумі світло незалежно від довжини хвилі поширюється із швидкістю 3·108; але при переході до іншого прозорого середовища швидкість світла змінюється – зменшується залежно від довжини хвилі і середовища.
 Найбільше зменшується швидкість фіолетового променя, а найменше – червоного. Цим пояснюється те, що фіолетовий промінь переходячи з вакууму в інше прозоре середовище, заломлюється більше, ніж промінь червоний, тобто має більший абсолютний показник заломлення. Білий промінь складений, а тому, коли він проходить через тригранну призму (рис. 1), то не тільки заломлюється до її основи, а й розкладається на кольорові промені.
Найбільше зменшується швидкість фіолетового променя, а найменше – червоного. Цим пояснюється те, що фіолетовий промінь переходячи з вакууму в інше прозоре середовище, заломлюється більше, ніж промінь червоний, тобто має більший абсолютний показник заломлення. Білий промінь складений, а тому, коли він проходить через тригранну призму (рис. 1), то не тільки заломлюється до її основи, а й розкладається на кольорові промені.
Основних кольорів (за Ньютоном)
є сім: 1 – Червоний, 2 – Оранжевий, 3 – Жовтий, 4 – Зелений, 5 – Голубий, 6 – Синій, 7 – Фіолетовий.
Отже, будь-який складний промінь за допомогою тригранної призми можна розкласти на його складові частини. Відомо також, що розжарені тверді і рідкі тіла дають спектр випромінювання суцільний – суцільну кольорову смугу, яка складається з різних кольорів, що поступово переходять одинв другий. Розжарені пари і гази елементів дають лінійчасті спектри, що складаються з окремих кольорових ліній. Лінійчасті спектри – характеристичні. Кожному елементу в стані розжареної пари або газу відповідає певне число кольорових ліній. Наприклад, натрій дає тільки одну жовту лінію (фактично, це дублет – дві близькі лінії, але їх можна побачити окремо тільки в доброму спектроскопі), водень (Н) – має чотири яскраво виявлені лінії: одну в червоній частині спектра, другу – в зеленій, третю – в синій, четверту – в фіолетовій.
Таким чином, розглядаючи лінійчасті спектри, можна визначити хімічну природу пароподібної або газоподібної речовини, що перебуває в розжареному стані.
Якщо розжарене тверде тіло, або рідке, що дає суцільний спектр оточене парою або газом, який має більш низьку температуру, то в цьому випадку промені, пройшовши через тригранну призму, дадуть спектр вбирання, тобто суцільний спектр, перерізаний різкими темними лініями вбирання. Її темні лінії будуть у тих спектра, де наведений вище газ, або пара, перебуваючи в розжареному стані, дають властиві їм кольорові лінії. Досліджуючи спектр вбирання можна, користуючись спеціальними таблицями, визначити, якому елементу належать ті або інші темні лінії. Таким чином, аналіз лінійчастих спектрів випромінювання і спектрів вбирання дає можливість встановити хімічну природу речовини.
Вивчення лінійчастих спектрів встановило певні закономірності цих спектрів, які зв’язані з внутрішньою будовою атомів. А саме встановлено, що спектральні лінії можна об’єднати у серії. Теорія дає, що для водню хвильові числа спектральних ліній (тобто величини, обернені до довжини хвилі 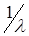 ) можна визначити з формули:
) можна визначити з формули:
 , (1)
, (1)
де  – швидкість світла;
– швидкість світла;
 – постійна Рідберга;
– постійна Рідберга;
 і
і  – цілі числа, при цьому
– цілі числа, при цьому  певне число, а
певне число, а  – ряд чисел, починаючи з числа, на одиницю більшого від
– ряд чисел, починаючи з числа, на одиницю більшого від  .
.
Число  визначає серію (ряд ліній, що відповідають певному
визначає серію (ряд ліній, що відповідають певному  при різних
при різних  ). Наприклад, при
). Наприклад, при  = 2 одержуються лінії видимої частини спектра – серія Бальмера.
= 2 одержуються лінії видимої частини спектра – серія Бальмера.
Кожна спектральна ліня виникає при переході електронів з одного стаціонарного стану в інший. При цьому зміна енергії електрона дорівнює енергії випромінюваного кванта.
За теорією Бора енергія електрона зв’язана певним числом з його характеристиками. Тому і постійна Рідберга з ними зв’язана.
Наведемо формулу без виводу:
 , (2)
, (2)
де  – маса електрона;
– маса електрона;  – заряд електрона;
– заряд електрона;  – постійна Планка;
– постійна Планка;
 = 8,85·10 -12 ф/м.
= 8,85·10 -12 ф/м.
Для одержання і вивчення спектрів користуються приладами, які називаються спектроскопами.






