Свойства белков следуют из их строения
Амфотерность
Заряд белка зависит от соотношения количества кислых и основных аминокислот. Поэтому, аналогично аминокислотам, белки заряжаются положительно при уменьшении рН, и отрицательно при его увеличении. Если рН раствора соответствует изоэлектрической точке белка, то заряд белка равен 0.
Влияние рН на заряд белка
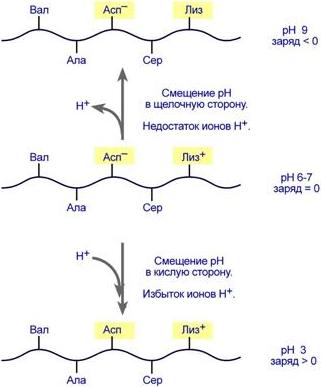
Изменение заряда белковой цепи при изменении pH
Растворимость
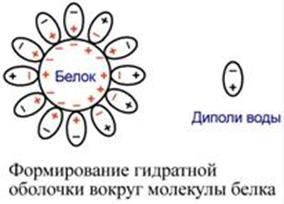
Растворимость объясняется:
· наличием заряда и взаимоотталкиванием заряженных молекул белка,
· наличием гидратной оболочки – чем больше полярных и/или заряженных аминокислот в белке, тем больше гидратная оболочка.
Классификация по функции
В соответствии с биологическими функциями выделяют:
· структурные белки (коллаген, кератин),
· ферментативные (пепсин, амилаза),
· транспортные (трансферрин, альбумин, гемоглобин),
· пищевые (белки яйца, злаков),
· сократительные и двигательные (актин, миозин, тубулин),
· защитные (иммуноглобулины, тромбин, фибриноген),
· регуляторные (соматотропный гормон, адренокортикотропный гормон, инсулин).
Классификация по строению

Простые белки немногочисленны
Структура простых белков представлена только полипептидной цепью (альбумин, инсулин). Однако необходимо понимать, что многие простые белки (например, альбумин) не существуют в "чистом" виде, они всегда связаны с какими-либо небелковыми веществами. Их относят к простым белкам только по той причине, что связи с небелковой группой слабые.
Альбумины
Альбумины – это группа схожих белков плазмы крови с молекулярной массой около 40 кДа, содержат много глутаминовой кислоты и поэтому имеют кислые свойства и высокий отрицательный заряд при физиологических рН.
Легко адсорбируют полярные и неполярные молекулы, являются, белком-транспортером в крови для многих веществ, в первую очередь для билирубина и длинноцепочечных жирных кислот.
Глобулины
Группа разнообразных белков плазмы крови с молекулярной массой до 100 кДа, слабокислые или нейтральные.
При электрофорезе глобулины сыворотки крови разделяются, как минимум, на 4 фракции – α1-глобулины, α2-глобулины, β-глобулины и γ-глобулины.
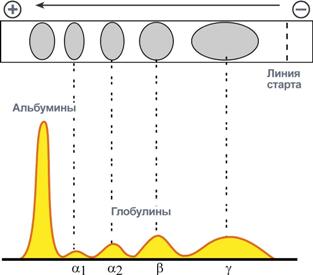
Картина электрофореза белков сыворотки крови
Гистоны - внутриядерные белки массой около 24 кДа
 Участок суперспирали ДНК
Участок суперспирали ДНК
|
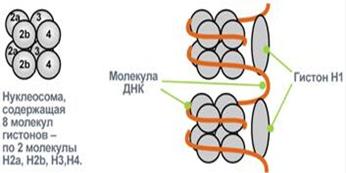
Взаимодействие гистонов и ДНК
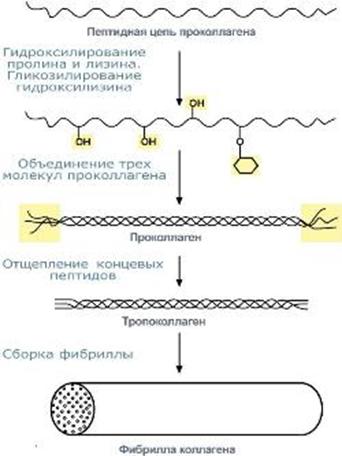 Коллаген
Коллаген
Синтез коллагена
Фибриллярный белок с уникальной структурой. Составляет основу межклеточного вещества соединительной ткани сухожилий, кости, хряща, кожи, но имеется, конечно, и в других тканях.
Обычно содержит моносахаридные (галактоза) и дисахаридные (галактоза-глюкоза) остатки, соединенные с ОН-группами некоторых остатков гидроксилизина.
Полипептидная цепь коллагена включает 1000 аминокислот и состоит из повторяющегося триплета [ Гли-А-В ], где А и В – любые, кроме глицина, аминокислоты. В основном это аланин, его доля составляет 11%, доля пролина и гидроксипролина – 21%. Таким образом, на другие аминокислоты приходится всего 33%. Структура пролина и гидроксипролина не позволяет образовать α-спиральную структуру, из-за этого образуется левозакрученная спираль, где на один виток приходится 3 аминокислотных остатка.
При синтезе коллагена первостепенное значение имеет гидроксилирование лизина и пролина, включенных в состав первичной цепи, осуществляемое при участии аскорбиновой кислоты.
Эластин
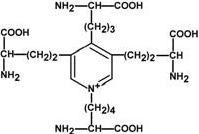
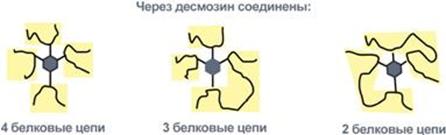
Строение десмозина
По строению в общих чертах эластин схож с коллагеном. Находится в связках, эластичном слое сосудов. Структурной единицей является тропоэластин с молекулярной массой 72 кДа и длиной 800 аминокислотных остатков. В нем гораздо больше лизина, валина, аланина и меньше гидроксипролина. Отсутствие пролина обуславливает наличие спиральных эластичных участков.
Характерной особенностью эластина является наличие своеобразной структуры – десмозина, который своими 4-мя группами объединяет белковые цепи в системы, способные растягиваться во всех направлениях.
α-Аминогруппы и α-карбоксильные группы десмозина включаются в образование пептидных связей одного или нескольких белков.