2.1. ОСНОВЫ МОЛЕКУЛЯРНО – КИНЕТИЧЕСКОЙ ТЕОРИИ
Молекулярная физика основывается на положении о том, что любое вещество состоит из частиц, которые находятся в беспорядочном движении и взаимодействуют друг с другом.
Идеальный газ – газ, в котором взаимодействием молекул можно пренебречь.
Основное уравнение МКТ идеального газа  ;
; 
Концентрация молекул вещества – число частиц в единице объема

Число частиц 
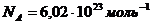 – число Авогадро (число молекул в 1моле вещества).
– число Авогадро (число молекул в 1моле вещества).
Количество вещества – число молей вещества 
Моль – количество вещества, содержащее столько же молекул, сколько атомов содержится в 0,012 кг углерода.
Абсолютная масса – масса одной частицы 
Относительная молекулярная масса

Молярная масса - масса одного моля вещества
 ;
; 
Температура – характеристика интенсивности теплового движения молекул изолированной системы при тепловом равновесии.
Температура – мера средней кинетической энергии поступательного движения молекул:
 ,
,
где k – постоянная Больцмана, k = 1,38·10-23  .
.
Средняя квадратичная скорость движения молекул:

Уравнение связи температуры по шкале Цельсия и абсолютной шкале
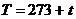 0С
0С
Закон Авогадро – в равных объёмах газов при одинаковых температурах и давлениях содержится одинаковое число молекул:
р= nkT
Уравнение состояния идеального газа:
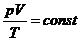 ;
; 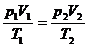 (для двух состояний газа).
(для двух состояний газа).
Уравнение Клапейрона – Менделеева  ,
,
где R – универсальная газовая постоянная
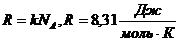 .
.
Закон Бойля – Мариотта (изотермический процесс) – при постоянной температуре и неизменной массе давление газа обратно пропорционально занимаемому газом объему:
 .
.
Закон Гей-Люссака (изобарный процесс) – при постоянном давлении и неизменной массе объем газа прямо пропорционален температуре:
 .
.
Закон Шарля (изохорный процесс) – Давление данной массы при постоянном объеме прямо пропорционально температуре:
 .
.
Закон Дальтона – давление смеси газов равно сумме парциальных давлений каждого из газов:
 .
.
Контрольные вопросы
1. Баллоны электроламп заполняют криптоном при низком давлении. Почему?
2. Каков физический смысл температуры?
3. При переходе определённой массы газа из одного состояния в другое давление уменьшается, а температура увеличивается. Как меняется его объём?
4. При каких условиях свойства реальных газов существенно отличаются от свойств идеального газа?
5. Почему газы способны неограниченно расширяться?
6. Как объяснить закон Бойля-Мариотта на основании МКТ?
7. Какие молекулы в атмосфере движутся быстрее: молекулы кислорода или молекулы азота?
8. Имеет ли смысл вопрос: «Какое давление оказывает на стенку сосуда одна молекула?
Примеры решения задач
Задача 1. Сколько молекул воздуха будет находиться в 1см3 сосуда при 10оС, если воздух в сосуде откачан до давления 1,33мкПа?
 |  |
Дано:
V=1см3
t=10оС
р=1,33мкПа
 N –?
N –?
СИ:
10-6м3
Т=283К
1,33·10-6Па
Решение:
Число молекул в 1см3 воздуха можно найти, зная постоянную Авогадро NА и число n молей, содержащихся в 1см3 воздуха, по формуле:
N = νN А
Число молей вещества  . Отношение же
. Отношение же 
Можно найти из уравнения Клапейрона – Менделеева:
 .
.
Таким образом, искомое число молекул:


Задача 2. Имеются два сосуда с газом: один вместимостью 3л, другой 4л. В первом сосуде газ находится под давлением 202кПа, а во втором 101кПа. Под каким давлением будет находиться газ, если эти сосуды соединить между собой? Считать, что температура в сосудах одинакова и постоянна.
 Дано:
Дано:
V1=3л
V2=4л
р1=202кПа
р2=101кПа
 р –?
р –?
СИ:
3·10-3м3
4·10-3м3
2,02·105Па
1,01·105Па

Решение:
По закону Дальтона,
р=р3+р4. (1)
Так как процесс изотермический, то парциальное давление газа в каждом сосуде можно найти по закону Бойля – Мариотта: p 1 V 1 = p 3 V, p 2 V 2 = p 4 V,
где V = V 1 + V 2.
Тогда парциальное давление газа в каждом из сосудов после их соединения
 (2)
(2)
Подставляем выражения (2) в (1):


Задача 3. Определить среднюю квадратичную скорость молекул газа, плотность которого при давлении 50кПа составляет 4,1·10-2кг/м3.
Дано:
р=50кПа
ρ=4,1·10-2кг/м3
 |
 –?
–?

СИ:
5·104Па

Решение:
По основному уравнению молекулярно-кинетической теории для давления имеем
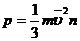 .
.
Произведение m 0 n = ρ – это плотность газа. Тогда


Задача 4. В закрытом сосуде вместимостью 1л содержится 12кг кислорода. Найти давление кислорода при 15оС.
 |  |
Дано:
V1=1л
m=12кг
t1=15оС
 р1–?
р1–?
СИ:
10-3м3
Т1=288К
Решение:
Сравним состояние данной массы кислорода (p1, V1, T1) c его состоянием при нормальных условиях (р0, V0, T0). По объединённому закону газового состояния,

Поскольку 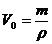 , где
, где  – плотность кислорода при нормальных условиях, то
– плотность кислорода при нормальных условиях, то  , откуда
, откуда 

Задача 5. Во сколько раз при подъёме пузырька воздуха в озере с глубины 30м до поверхности увеличивается его объём?
 Дано:
Дано:
h=30м
 |

Решение:
Обозначим через V1 и p1 объём и давление воздуха в пузырьке, когда он находится на дне, а через V2 и p2 – на поверхности.
По условию процесс изотермический, поэтому
p 1 V 1 = p 2 V 2,
при этом
p 1 = p 2 + ρgh.
Тогда
 .
.
Полагая, что p2=p0≈105Па, получаем:

Упражнения
1. Сколько молекул воды содержится в капле массой 0,2г?
Ответ: 6,7·1021.
2. Какой объём занимают 100моль ртути? Плотность ртути 13,6·103 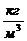 .
.
Ответ: 1,5л.
3. Рассчитать давление азота в баллоне, если средняя квадратичная скорость его молекул  , а плотность 1,35
, а плотность 1,35 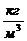 .
.
Ответ: 1,3·105.
4. Определить среднюю квадратичную скорость молекул кислорода при температуре 20оС.
Ответ: 470  .
.
5. Пузырёк воздуха поднимается со дна реки на её поверхность, увеличиваясь в объёме от 1 до 3 мм3. Температура воды на дне 7оС, а на поверхности 27оС. Какое давление испытывал пузырёк на дне, если на поверхности давление 100кПа?
Ответ: 2,8·105Па.
6. На поверхности Венеры температура 750К и давление 9120кПа. Найти плотность атмосферы у поверхности планеты, считая, что она состоит из углекислого газа.
Ответ: 64,4 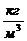 .
.
7. Сколько молекул воздуха будет находиться в 1см3 сосуда при 10оС, если воздух в сосуде откачан до давления 1,33мкПа?
Ответ: 3,4·108.
8. Резиновый шар объёмом 3дм3 был в комнате при 27оС. Его вынесли на улицу, где температура – 27оС. На сколько изменится объём газа?
Ответ: 0,54л.
9. Сосуд, содержащий 12л газа под давлением 400кПа, соединён с пустым сосудом ёмкостью 4000см3. Найти конечное значение давления, если температура газа не изменилась.
Ответ: 3·105Па.
10. Найти концентрацию молекул кислорода, если давление 0,2МПа, а средняя квадратичная скорость молекул 700  .
.
Ответ: 2,3·1025м-3.
Самостоятельно
11. Какова среднеквадратичная скорость движения молекул газа, если, имея массу 6кг, они занимает объём 5м2 при давлении 200кПа?
Ответ: 700  .
.
12. Вычислить массу одной молекулы метана СН4.
Ответ: 2,7·10-26кг.
13. Газ при давлении 0,2МПа и температуре 15оС имеет объём 5л. Чему равен объём газа этой массы при нормальных условиях?
Ответ: 9,5л.
14. При увеличении давления в 1,5 раза, объём газа уменьшился на 30мл. Найти первоначальный объём.
Ответ: 90мл.
15. В сосуде объёмом 1м3 под давлением 1·105Па находится газ в количестве 1моль. Какова средняя кинетическая энергия движения молекул газа?
Ответ: 2,5·10-19Дж.
16. * Из баллона со сжатым водородом, вместимостью 10л, вследствие неисправности вентиля, утекает газ. При 7оС манометр показал давление 5МПа. Показание манометра не изменились и при 17оС. Определить, сколько газа утекло.
Ответ: 1,5·10-3кг.
2.2. ОСНОВЫ ТЕРМОДИНАМИКИ
Внутренняя энергия тела – это сумма кинетических и потенциальных энергий всех молекул тела.
Внутренняя энергия идеального газа
 ,
,
т. к. потенциальная энергия взаимодействия молекул идеального газа равна нулю.
Для одноатомного идеального газа формула внутренней энергии:

Изменение внутренней энергии газа:

При изобарном расширении газа, газ совершает работу:

При изобарном сжатии газа работа внешних сил:

Теплообмен (теплопередача) – передача энергии от одного тела другому без совершения работы.
Количество теплоты – энергия, переданная путём теплообмена.
Нагревание (охлаждение):
Q = cm (t 2 - t 1),
где с – удельная теплоёмкость вещества (физическая величина, численно равная количеству теплоты, необходимому для нагревания единицы массы вещества на 1Со).
Q = C (t 2 - t 1),
где С – теплоёмкость тела; С=с m.
Плавление (кристаллизация):
 ,
,
где  - удельная теплота плавления (количество теплоты, необходимое для превращения единицы массы из твёрдого состояния в жидкое при неизменных температуре и давлении).
- удельная теплота плавления (количество теплоты, необходимое для превращения единицы массы из твёрдого состояния в жидкое при неизменных температуре и давлении).
Парообразование (конденсация):
Q = rm,
где r – удельная теплота парообразования (количество теплоты, необходимое для превращения единицы массы из жидкого состояния в парообразное при неизменных температуре и давлении).
Сгорание топлива:
Q = qm,
где q – удельная теплота сгорания (физическая величина, численно равная количеству теплоты, выделяющемуся при полном сгорании единицы массы топлива).
Уравнение теплового баланса для замкнутой системы, состоящей из нескольких тел, имеющих различные температуры:
Q 1 + Q 2 +…+ Qn =0
Q>0 – тело получает некоторое количество теплоты,
Q<0 – тело отдаёт некоторое количество теплоты.
Первый закон термодинамики: изменение внутренней энергии газа происходит за счёт совершения работы и передачи теплоты:
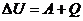
Изобарный процесс:

Изохорный процесс:

Изотермический процесс:

Адиабатный процесс:

Тепловая машина – устройство, в котором внутренняя энергия рабочего вещества превращается в механическую работу
 ,
,
где Q1 – количество теплоты, отданное нагревателем,
Q2 – количество теплоты, переданное холодильнику.
Коэффициент полезного действия (КПД) теплового двигателя:
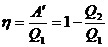
КПД идеальной тепловой машины:
 ,
,
где Т1 – температура нагревателя, Т2 – температура холодильника.
Контрольные вопросы
1. Почему в пустынях температура поднимается очень высоко днём, а ночью опускается ниже нуля?
2. Как изменится КПД тепловой машины, если температура нагревателя будет повышаться, а температура холодильника – понижаться?
3. Почему в дизеле не требуется зажигание горючей смеси с помощью электрической искры.
4. Почему инструмент при заточке нагревается?
5. В каких случаях изменение внутренней энергии отрицательно?
6. Почему при накачивании велосипедной шины насос заметно нагревается?
7. Почему нельзя говорить, что система обладает запасом определённого количества теплоты?
Примеры решения задач
Задача 1. Алюминиевый сосуд массой 0,5кг содержит 0,118кг воды при температуре 20оС. Кусок железа массой 0,2кг, нагретый до 75оС, опускают в сосуд. Определить конечную температуру.
Дано: Решение:
 m1=0,5кг В теплообмене участвуют три тела: алюминий, вода, железо.
m1=0,5кг В теплообмене участвуют три тела: алюминий, вода, железо.
m2=0,118кг Количество теплоты  , полученное алюминиевым
, полученное алюминиевым
t1=20oC сосудом и количество теплоты  , полученное во
, полученное во
m3=0,2кг дой, в сумме равны количеству теплоты  , то есть
, то есть
t3=75oC по уравнению теплового баланса Q1+Q2+Q3=0

 -?
-? 
Решая это уравнение относительно  , получим
, получим

Производим подстановку численных значений:

Задача 2. Газ, занимавший объём 20л при нормальных условиях был изобарно нагрет до 80оС. Определить работу расширения газа.

 Дано: СИ: Решение:
Дано: СИ: Решение:
V1=20л  Работа расширения газа при изобарном процессе
Работа расширения газа при изобарном процессе
T1=0o Т1=273К определяется формулой 
T2=80oC Т2=353К Из уравнения состояния газа следует:



 Из уравнения Клапейрона – Менделеева
Из уравнения Клапейрона – Менделеева
 , находим число молей газа:
, находим число молей газа:
 , отсюда
, отсюда  .
.
Произведём вычисления: 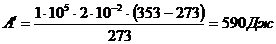 .
.
Задача 3. Температура нагревателя идеальной тепловой машины 500К, температура холодильника 400К. Определить КПД цикла Карно и полезную мощность машины, если нагреватель передаёт ей 1675Дж теплоты в секунду.
 Дано: Решение:
Дано: Решение:
Т1=500К КПД идеальной тепловой машины определяется
Т2=400К  ;
; 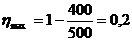 .
.
Q1=1675Дж В полезную работу превращается  .
.
 t=1с Полезная мощность машины
t=1с Полезная мощность машины 
 Подставляем уравнение работы, получим
Подставляем уравнение работы, получим
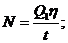
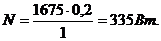
Задача 4. При выстреле вертикально вверх свинцовая пуля достигла высоты 1200м. При падении, ударившись о землю, она нагрелась. Считая, что 50% всей энергии удара пошла на нагревание пули, рассчитать, на сколько повысилась её температура.
 Дано: Решение:
Дано: Решение:

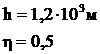 Используем соотношение
Используем соотношение  , где
, где  - измене-
- измене-
 ние внутренней энергии пули при её нагревании.
ние внутренней энергии пули при её нагревании.
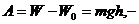 работа по изменению потенциальной энергии пули,
работа по изменению потенциальной энергии пули,
тогда  , откуда
, откуда
 ;
;
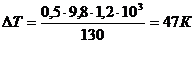
Задача 5. Давление азота, находящегося в сосуде ёмкостью 3 литра, после нагревания возросло на 2,2МПа. Определить количество теплоты, сообщённое газу.


 Дано: СИ: Решение:
Дано: СИ: Решение:




 V=3л Процесс протекает при неизменном объёме, исполь -зуем уравнение Клапейрона – Менделеева для двух состояний газа:
V=3л Процесс протекает при неизменном объёме, исполь -зуем уравнение Клапейрона – Менделеева для двух состояний газа:
При вычитании одного уравнения из другого, получим
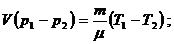 отсюда
отсюда  ;
; 
Количество теплоты, сообщённое газу
 ; сделав подстановку, получим
; сделав подстановку, получим
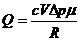
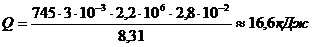 .
.
Упражнения
1. В латунный калориметр, массой 150 г, содержащий 200 г воды при 15оС, опустили железную гирю, массой 260 г при температуре 100оС. Найти установившуюся общую температуру.
Ответ: 25оС.
2. До какой температуры нагреется 0,8 кг воды, находящейся в медном калориметре массой 0,7 кг и имеющей температуру 12оС, если ввести в калориметр 0,05 кг пара при 100оС?
Ответ: 46оС.
3. Сколько керосина необходимо сжечь, чтобы 50 л воды нагреть от 20оС до кипения? КПД нагревателя 35%.
Ответ: 1,1кг.
4. Вода падает с высоты 15 м и 30% совершенной ею работы идёт на нагревание самой воды. На сколько градусов нагреется вода?
Ответ: 0,01оС.
5. Свинцовая пуля, летящая со скоростью 200 м/с, попадает в земляной вал. На сколько повысится температура пули, если на её нагревание пошло 78% кинетической энергии?
Ответ: 120К.
6. Температура нагревателя 520оС, а холодильника – 20оС. Какую работу совершила машина, получив от нагревателя  Дж?
Дж?
Ответ:  Дж.
Дж.
7. В вертикальном цилиндре под поршнем находится кислород массой 2 кг. Для повышения температуры на 5оС ему передано 9,16 кДж теплоты. Найти работу газа при изобарном расширении.
Ответ: 2670 Дж.
8. Температура нагревателя идеального теплового двигателя 127оС, а холодильника 7оС. Количество теплоты, получаемое двигателем ежесекундно от нагревателя, равно 50 кДж. Какое количество теплоты отдаётся холодильником за 1 секунду?
Ответ: 35кДж.
Самостоятельно
9. В цилиндре под тяжёлым поршнем находится СО2 массой 200 г. Газ нагревается на 88 К. Какую работу он при этом совершает?
Ответ: 3,3 кДж.
10. В калориметр с теплоёмкостью 63 Дж/оК было налито 250 г масла при 12оС. После опускания в масло медного тела массой 500 г при 100оС общая температура установилась 33оС. Какова удельная теплоёмкость масла?
Ответ: 2,2кДж/кг оС.
11. Колба, теплоёмкостью которой можно пренебречь, содержит 600г воды при температуре 80оС. Какое количество льда при температуре -15оС нужно добавить в воду, чтобы окончательная температура смеси была равна 50оС?
Ответ: 0,13кг.
12. Сколько стали, взятой при 20оС, можно расплавить в печи с КПД 50%, сжигая 2 т каменного угля?
Ответ: 40 т.
13. На сколько повысилась температура стальной детали массой 2 кг, после 5 ударов молота массой 0,35 т, при падении молота с высоты 2 м? На нагревание детали идёт 50% энергии молота.
Ответ: 18,7оС.
14. Самолёт летел со скоростью 720 км/ч и пролетел 1800 км. Мощность его моторов 1177,2 кВт, их КПД 30%. Сколько авиационного бензина израсходовано?
Ответ: 706,3 кг.
15. Определить работу расширения 20 л газа при изобарном нагревании от 300К до393К, если давление газа 80 кПа.
Ответ: 496 Дж.
16. Для изобарного нагревания газа в количестве 800 моль на 500 К ему сообщили количество теплоты 9,4 МДж. Определить работу газа.
Ответ: 3,3 МДж.
17. В идеальной тепловой машине за счёт каждого килоджоуля энергии, получаемой от нагревателя, совершается работа 300 Дж. Определить КПД машины и температуру нагревателя, если температура холодильника 280 К.
Ответ: 30%; 400 К.
18 *. Идеальный одноатомный газ, находящийся в количестве 2моль при 0оС, сначала изохорно перевели в состояние, в котором давление в 2 раза больше первоначального, а затем, изобарно – в состояние, в котором объём в 2 раза больше первоначального. Найти изменение внутренней энергии.
Ответ: 20,4 кДж.






