Лекционное занятие №2
Тема: Основные понятия и законы химии
Вопросы для самоконтроля:
1Выберите определения относительной атомной массы:
а) наименьшая масса вещества, которая определяет ее свойства б) масса одного моля атомов вещества в граммах;
в) масса одной молекулы вещества в граммах, г) от ношения массы атома элемента к 1 / 12 массы атома углерода.
2Выберите определения химической формулы:
а) условная запись состава вещества с помощью символов химических элементов и индексов;
б) обозначения вещества с помощью названий элементов в) химический символ простого вещества;
г) обозначение вещества с помощью символов и названий элементов
3 Среди перечисленных явлений выберите химические:
а) ржавления железа, б) образование инея в) горение спирта г) плавления сахара д) гниение древесины
4 Установите соответствие между формулой вещества и молярной массой.
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Формула вещества: Молярная масса, г / моль:
1)Н3РО4; а) 90;
2) Fe(OH)2; б) 200;
3) СаВг2; в) 65;
4) NaBrO2. г) 98;
д) 135.
Лекционное занятие № 3
Тема: Периодический закон и Периодическая система химических элементов Д.И. Менделеева и строение атома.
Вопросы для самоконтроля:
1 Периодический закон открыт:
а) Ломоносовым; б) Менделеевым; в) Лавуазье.
2 Какие элементарные частицы входят в состав атомного ядра:
а) протоны и нейтроны; б) нейтроны и электроны; в) только протоны; г) только нейтроны.
3Что такое изотопы:
а) атомы с разным зарядом ядра;
б) вещества, имеющие одинаковый состав, но разную массу;
в) атомы, имеющие одинаковое число протонов в ядре, на разное число нейтронов;
г) атомы одного и того же элемента, имеющие разную массу.
4. Укажите порядковый номер элемента, атом которого имеет на внешнем энергетическом уровне 1 электрон:
а) N81 б) N37 в)N36.
5. Электронная формула ls22s22p63s23p4 соответствует атому:
а. кислорода б. серы в. азота г. фосфора
6 Одинаковое количество энергетических уровней имеют атомы элементов с порядковыми номерами: а) 6 и 14 б) 6 и 7. Ответ подтвердите составлением электронных схем и электронных формул.
_____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Лекционное занятие № 4
Тема: Строение вещества
Вопросы для самоконтроля: 1 В узлах ионной кристаллической решетки находятся: а) атомы, б) ионы, в) молекулы.
2 Химическая связь в молекуле SiH4:
а). ковалентная полярная б) ковалентная неполярная в)ионная г) металлическая
3 Пользуясь Периодической системой элементов, укажите, какой из перечисленных элементов имеет наибольшую электроотрицательность:
а) азот; б) мышьяк; в) селен; г)кислород
4 Выберите ряд, в котором перечисленные соединения с ионным типом связи:
а) Р205, НСI, Si02, С02; б) КСI, СаВг2,N а20, К2S;
в) N2, СI2, Н2, 02; г) НВг, РН3,, Н2S.
5 Эмульсией является:
А. Молоко. В. Пена. Б. Тушь. Г. Туман.
6. Эмульсия – это:
А жидкость + твердое вещество Б жидкость + жидкость
В жидкость + газ Г газ + твердое вещество
7. Суспензия – это:
А жидкость + твердое вещество Б жидкость + жидкость
В жидкость + газ Г газ + твердое вещество
Лекционное занятие № 5
Тема: Вода. Растворы.
Вопросы для самоконтроля:
1) К насыщенным относятся растворы, в которых:
а) Вещество растворяется дополнительно при данной температуре;
б) При данной температуре вещество больше не растворяется;
в) Растворенное вещество при охлаждении раствора выпадает в осадок;
г) При повышении температуры растворяется больше вещества.
2) Если в раствор добавить воду, то массовая доля вещества в растворе:
а) Уменьшится;
б) Увеличится;
в) Не изменится;
г) Сначала увеличится, затем уменьшится.
3) Массовая доля вещества в растворе равна:
а) Отношению массы раствора к его объему;
б) Разнице между массами растворенного вещества и раствора;
в) Отношению объема раствора к массе растворенного вещества;
г) Отношению массы растворенного вещества к массе раствора.
4) К раствору массой 250г с массовой долей вещества 0,2 добавили воду массой 50г. Массовая доля вещества в образовавшемся растворе равна:
а)0,01; в)0,2;
б)0,17; г)0,3.
РЕШЕНИЕ:
__________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Лекционное занятие № 6
Тема: Электролитическая диссоциация.
Вопросы для самоконтроля:
1. К электролитам относится:
а) сахар б) оксид меди (II) в) оксид углерода (IV) г) соляная кислота
2. Формула слабого электролита:
а) CuCl2 б) HCl в) H2SO4 г) H2S
3. Вещества, которые при диссоциации образуют в качестве катионов ионы водорода, являются
а) кислотами б) солями в) щелочами г) оксидами
4. Вещество, которое в растворе полностью распадается на ионы.
а) аммиак б) вода в) серная кислота г) гидроксид цинка
5. Все ионы являются анионами в ряду:
а) Cl ̄, SO4 2¯, NO3 ̄ в) Н+, Na + , Ca 2+
б) Сl¯, H+, K+ г) CO3 2¯,Ca 2+ , NO3 ̄
6 Составьте уравнения реакции ионного обмена между веществами:
а) СаСО3 + 2HCl 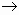 CaCl2 + H2O + CO2
CaCl2 + H2O + CO2 
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Б) H2SO4 + Ba(OH)2 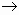 BaSO4
BaSO4  + 2H2O
+ 2H2O
______________________________________________________________________________________________________________________________________________________________________________
В)1) NaOH + HCl 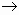 NaCl + H2O
NaCl + H2O
_______________________________________________________________________________________
_________________________________________________________________________________
Лекционное занятие № 7






