Вариант № 4
1. Определите, во сколько раз увеличится скорость реакции, если температура возрастет от 10оС до 50оС. Температурный коэффициент равен 3.
Ответ: скорость реакции увеличится в 81 раз.
2. Обоснуйте, при изменении каких факторов равновесие можно сместить в сторону образования продуктов реакции:
2SO2(г) + О2(г) ↔2SО3(г); ΔHо>0.
3. Напишите выражение закона действующих масс для скорости прямых реакций и химического равновесия и рассчитайте Кравн при превращении 20% исходных веществ:
а) NO(г) + NO2(г) + O2(г) ↔2N2O5(т)
б) CO(г) + Cl2(г) ↔СОCl2(г)
в) Cl2(г) + H2(г) ↔ 2HCl(г)
Вариант № 5
1. Определите, во сколько раз увеличится скорость реакции, если температура возрастет от 10оС до 50оС. Температурный коэффициент равен 4.
Ответ: скорость реакции увеличится в 256 раз.
2. Обоснуйте, при изменении каких факторов равновесие можно сместить в сторону образования продуктов в реакции и рассчитайте Кравн при превращении 40% исходных веществ:
MgO(к) + CO2(г) ↔MgCO3(к); ΔHо<0.
3. Напишите выражение закона действующих масс для скорости прямых реакций и химического равновесия:
а) 2CO(г) ↔CO2(г) + C(к)
б) 2NO(г) + Cl2(г) ↔2NOCl (г)
в) 2SO2(г) + О2(г) ↔2SО3(г)
Вариант № 6
1. Определите, на сколько градусов необходимо увеличить температуру, чтобы скорость реакции увеличилась в 64 раз. Температурный коэффициент равен 2.
Ответ: температуру необходимо увеличить на 60оС.
2. Обоснуйте, при изменении каких факторов равновесие можно сместить в сторону образования продуктов реакции:
СS2(г) + 2H2S(г) ↔ CH4(г) + 4S(т); DHо <0
3. Напишите выражение закона действующих масс для скорости прямых реакций и химического равновесия и рассчитайте Кравн при превращении 30% исходных веществ:
а) CO2(г) + C(к) ↔2CO(г)
б) 2Н2(г) + O2(г) ↔2Н2O(г)
в) 3H2(г) + N2(г) ↔ 2NH3(г)
Вариант № 7
1. Рассчитайте, температурный коэффициент химической реакции, если при увеличении температуры на 40оС скорость реакции увеличилась в 81 раз.
Ответ: температурный коэффициент равен 3.
2. Обоснуйте, при изменении каких факторов равновесие можно сместить в сторону образования исходных веществ в системе: NH3(г) + HCl(ж) ↔ NH4Cl(ж); DHо>0
3. Напишите выражение закона действующих масс для скорости прямых реакций и химического равновесия и рассчитайте Кравн при превращении 20% исходных веществ:
а) 2NO(г) + SO2(г) ↔ N2O(г) + SO3(г)
б) Br2(г) + H2(г) ↔2HBr(г)
в) С(тв) + 2Н2(г) ↔СН4(г)
Вариант № 8
1. Определите, во сколько раз увеличится скорость реакции, если температура возрастет от 10оС до 30оС. Температурный коэффициент равен 4.
Ответ: скорость реакции увеличится в 16 раз.
2. Обоснуйте, при изменении каких факторов равновесие можно сместить в сторону образования продуктов реакции:
2NO(г) + SO2(г) ↔N2O(г) + SO3(г); DHо<0
3. Напишите выражение закона действующих масс для скорости прямых реакций и химического равновесия и рассчитайте Кравн при превращении 50% исходных веществ:
а) NH3(г) + HCl(ж) ↔NH4Cl(ж)
б) Fe3O4(к) + 4Н2(г) ↔3Fe(к) + 4Н2О(г)
в) 2NO(г) + O2(г) ↔2NO2(г)
Вариант № 9
1. Определите, во сколько раз увеличится скорость реакции, если температура возрастет от 20оС до 50оС. Температурный коэффициент равен 2.
Ответ: скорость реакции увеличится в 8 раз.
2. Обоснуйте, при изменении каких факторов равновесие можно сместить в сторону образования продуктов в реакции:
2SO2(г) + O2(г) ↔ 2SO3(г); ΔHо<0.
3. Напишите выражение закона действующих масс для скорости прямых реакций и химического равновесия и рассчитайте Кравн при превращении 30% исходных веществ:
а) 2NO(г) + O2(г) ↔2NO2(г)
б) СS2(г) + 2H2S(г) ↔CH4(г) + 4S(т)
в) 2NH3(г) ↔N2(г) + 3H2(г)
Вариант № 10
1. Определите, во сколько раз увеличится скорость реакции, если температура возрастет от 10оС до 50оС. Температурный коэффициент равен 3.
Ответ: скорость реакции увеличится в 81 раз.
2. Обоснуйте, при изменении каких факторов равновесие можно сместить в сторону образования продуктов в реакции:
MgO(к) + CO2(г) ↔MgCO3(к); ΔHо<0.
3. Напишите выражение закона действующих масс для скорости прямых реакций и химического равновесия и рассчитайте Кравн при превращении 40% исходных веществ:
а) 2NO(г) + SO2(г) ↔N2O(г) + SO3(г)
б) Br2(г) + H2(г) ↔2HBr(г)
в) С(тв) + 2Н2(г) ↔СН4(г)
Образец выполнения письменных заданий:
1. Определите, на сколько градусов была повышена температура некоторой реакции, если известно, что скорость реакции увеличилась в 16 раз, а температурный коэффициент равен 2.
Решение:
В уравнение Вант-Гоффа
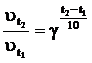
подставим известные значения и рассчитаем изменение температуры:

Ответ: температура увеличится на 40oС.
2. Обоснуйте, при изменении каких факторов равновесие можно сместить в сторону образования продуктов в реакции:
С(т) + Н2О(г) ↔Н2(г) + СО(г); DНо>0
Ответ:
В соответствии с принципом Ле Шателье равновесие можно сместить в сторону образования продуктов реакции при:
1) повышении температуры, т.к. прямая реакция является эндотермической (DНо>0);
2) понижении давления, т.к. в результате прямой реакции число газообразных частиц возрастает;
3) повышении концентрации исходного вещества Н2О или понижении концентрации одного из продуктов реакции Н2 или СО.
3. Напишите выражение закона действующих масс для скорости прямой реакции и химического равновесия:
CuO(к) + H2(г) ↔Cu(к) + H2O(г)
Ответ:
Для скорости реакции – V = k∙C(H2)
Для химического равновесия – 
Тема 4.
Растворы, способы выражения состава растворов.
Приготовление растворов с заданным содержанием растворенного вещества.
Вопросы для самостоятельной внеаудиторной подготовки к занятию:
1. Общие понятия: раствор, растворитель, растворенное вещество.
2. Растворимость. Назовите факторы, от которых зависит растворимость веществ.
3. Процесс растворения веществ. Из каких стадий состоит процесс растворения? Что называется тепловым эффектом растворения?
4. Что называется насыщенным, ненасыщенным и пересыщенным растворами? Каковы условия их получения? Может ли быть насыщенный раствор разбавленным, а концентрированный – ненасыщенным? Приведите примеры.
5. Назовите известные вам способы выражения количественного состава растворов.
Изучив эти вопросы, выполните письменно следующие задания:
Вариант № 1
1. К раствору массой 250 г с w(соли) = 10% добавили эту же соль массой 15 г. Рассчитайте массовую долю соли в полученном растворе.
Ответ: 15,09 %.
2. Смешали раствор массой 200 г с w(щелочи) = 1% с раствором массой 50 г с w(щелочи) = 4%. Вычислите массовую долю щелочи в полученном растворе.
Ответ: 1,6%.
3. Рассчитайте объем воды, который необходимо добавить к раствору объемом 500 мл с w(NaOH) = 40% (r = 1,43 г/мл) для приготовления раствора с w(NaOH) = 10%.
Ответ: 2,15 л.
Вариант № 2
1. К раствору массой 300 г с w(ZnSO4) = 5% добавили сульфат цинка массой 20 г. Рассчитайте массовую долю ZnSO4 в полученном растворе.
Ответ: 10,94%.
2. Смешали раствор массой 150 г с w(КОН) = 5% с раствором массой 200 г с w(КОН) = 10%. Вычислите массовую долю щелочи в полученном растворе.
Ответ: 7,86%.
3. Рассчитайте объем воды, который необходимо добавить к раствору объемом 0,5 л с массовой долей серной кислоты 20% (r = 1,143 г/мл) для приготовления раствора с w(H2SO4) = 12%.
Ответ: 381 мл.
Вариант № 3
1. К раствору массой 450 г с w(NaCl) = 3% добавили эту же соль массой 25 г. Рассчитайте массовую долю NaCl в полученном растворе.
Ответ: 8,10%.
2. Смешали раствор массой 300 г с массовой долей растворенного вещества 2% с раствором массой 140 г с массовой долей растворенного вещества 6%. Вычислите массовую долю этого вещества в полученном растворе.
Ответ: 3,27%.
3. Рассчитайте объем воды, который необходимо добавить к раствору объемом 250 мл с w(HNO3) = 30% (r = 1,205 г/мл) для приготовления раствора с w(HNO3) = 25%.
Ответ: 60,25 мл.
Вариант № 4
1. К раствору массой 150 г с w(КОН) = 10% добавили 5 г гидроксида калия. Рассчитайте массовую долю КОН в полученном растворе.
Ответ: 12,9%.
2. Смешали раствор массой 60 г с массовой долей растворенного вещества 2% с раствором массой 150 г с массовой долей растворенного вещества 5%. Вычислите массовую долю этого вещества в полученном растворе.
Ответ: 4,14%.
3. Какую массу воды нужно добавить к раствору массой 125г с w(NaCl) = 8%, чтобы получить раствор этой соли с массовой долей 5%?
Ответ: 75 г.
Вариант № 5
1. Смешали раствор массой 300 г с w(NaCl) = 20% с раствором массой 500 г с w(NaCl) = 40%. Вычислите массовую долю хлорида натрия в полученном растворе.
Ответ: 32,5%.
2. Рассчитайте массу воды, которую надо добавить к раствору массой 20 г с w(Н2SO4) = 70% для получения раствора с w(Н2SO4) = 3%.
Ответ: 446,67 г.
3. Какой объем раствора с w(НCl) = 5% (r = 1,023 г/мл) можно получить из раствора объемом 103,9 мл с w(НCl) = 30%
(r = 1,149 г/мл)?
Ответ: 700,18 мл.
Вариант № 6
1. Какую массу воды нужно добавить к раствору серной кислоты массой 40 г с w(H2SO4) = 20%, чтобы получить раствор с w(H2SO4) = 8%?
Ответ: 60 г.
2. Какой объем раствора серной кислоты с w(H2SO4) = 90% (r = 1,82 г/мл) нужно взять для приготовления раствора объемом 50 мл с w(H2SO4) = 50% (r = 1,40 г/мл)?
Ответ: 21,37 мл.
3. В растворе массой 500 г с w(CuSO4) = 4% растворили 25 г медного купороса (CuSO4∙5H2O). Рассчитайте массовую долю сульфата меди(II) в полученном растворе.
Ответ: 6,86%.
Вариант № 7
1. Какая масса Na2SO3 потребуется для приготовления раствора объемом 5 л с w(Na2SO3) = 8% (r = 1,075 г/мл)?
Ответ: 430 г.
2. Какую массу кристаллогидрата FeSO4∙7H2O и какой объем воды надо взять для приготовления раствора массой 500 г с массовой долей сульфата железа(II) 5%?
Ответ: 45,73 г; 454,27 мл.
3. Смешали раствор массой 120 г с w(КОН) = 9% с раствором массой 380 г с w(КОН) = 12%. Вычислите массовую долю гидроксида калия в полученном растворе.
Ответ: 11,28%.
Вариант № 8
1. Рассчитайте массу железного купороса FeSO4∙7H2O, которую необходимо растворить в воде объемом 1 л (ρ = 1 г/мл), чтобы получить раствор с массовой долей FeSO4 20%?
Ответ: 576,37г.
2. Какую массу иодида кальция следует добавить к раствору объемом 500 мл с w(CaI2) = 12% (ρ = 1,107 г/мл) для получения раствора с w(CaI2) = 30%?
Ответ: 142,33 г.
3. Какую массу соли следует растворить в 100 г воды для получения раствора c массовой долей этой соли 15%?
Ответ: 17,65 г.
Вариант № 9
1. К раствору массой 250 г с w(соли) = 10% добавили эту же соль массой 15 г. Рассчитайте массовую долю соли в полученном растворе.
Ответ: 15,09 %.
2. Какой объем раствора серной кислоты с w(H2SO4) = 90% (r = 1,82 г/мл) нужно взять для приготовления раствора объемом 50 мл с w(H2SO4) = 50% (r = 1,40 г/мл)?
Ответ: 21,37 мл.
3. Рассчитайте массу железного купороса FeSO4∙7H2O, которую необходимо растворить в воде объемом 1 л (ρ = 1 г/мл), чтобы получить раствор с массовой долей FeSO4 20%?
Ответ: 576,37 г.
Вариант № 10
1. Смешали раствор массой 300 г с массовой долей растворенного вещества 2% с раствором массой 140 г с массовой долей растворенного вещества 6%. Вычислите массовую долю этого вещества в полученном растворе. Ответ: 3,27%.
2. К раствору массой 300 г с w(ZnSO4) = 5% добавили сульфат цинка массой 20 г. Рассчитайте массовую долю ZnSO4 в полученном растворе.
Ответ: 10,94%.
3. В растворе массой 500 г с w(CuSO4) = 4% растворили 25 г медного купороса (CuSO4∙5H2O). Рассчитайте массовую долю сульфата меди(II) в полученном растворе.
Ответ: 6,86%.
Образец выполнения письменных заданий:
1. Какой объем раствора с w(HNO3) = 86% (r = 1,48 г/мл) нужно взять для приготовления раствора объемом 100 мл с w(HNO3) = 32% (r = 1,20 г/мл)?
Решение:
1) Рассчитаем массу раствора с массовой долей HNO3 32%:

2) Найдем массу HNO3 в 32%-ном растворе:
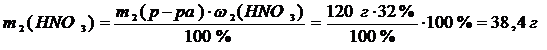
3) Рассчитаем массу раствора с массовой долей HNO3 86%:


4) Найдем объем раствора с массовой долей HNO3 86%:

Ответ: 30,17 мл.
Тема 5.
Электролитическая диссоциация. Слабые и сильные электролиты. Водородный показатель.
Вопросы для самостоятельной внеаудиторной подготовки к занятию:
1. Что называется электролитической диссоциацией? Электролиты и неэлектролиты. Приведите примеры. К каким классам неорганических соединений относятся электролиты? Назовите основные положения теории электролитической диссоциации С. Аррениуса.
2. Как влияет природа химической связи на диссоциацию веществ в растворах? Поясните механизм процесса электролитической диссоциации, приведите примеры и схемы диссоциации в воде электролитов с ионным типом связи и ковалентной полярной связью. Что такое сольваты (гидраты)?
3. Что такое степень диссоциации? Какие электролиты называются сильными и слабыми? Приведите примеры.
4. Зависимость степени диссоциации от:
- от природы электролита и растворителя; роль диэлектрической проницаемости растворителя в процессе диссоциации;
- концентрации электролита и изменения концентрации одно- именных ионов;
- температуры; термодинамический анализ процесса диссоциации.
5. Константа электролитической диссоциации. От каких факторов она зависит? Закон разбавления Оствальда для слабых бинарных электролитов.
6. Дайте определения кислоте, основанию и соли (средней, кислой, основной, двойной) согласно теории электролитической диссоциации.
7. Ионное произведение воды. Водородный показатель – (рН); гидроксидный показатель – рОН. Сумма рН и рОН. Значения концентрации С(Н+) и рН в различных средах.
Изучив эти вопросы, выполните письменно следующие задания:
Вариант № 1
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HClO4, Ca(OH)2, Al2(SO4)3, H3PO4, NaHSO3, MgOHCl, KАl(SO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
2. Составьте молекулярные, полные и сокращенные ионно-молекулярные уравнения для следующих реакций:
1) FеСl3 + NаОН ®
2) Nа2СО3 + НСl ®
3) АgNО3 + Nа3PO4 ®
3. Рассчитайте рН раствора угольной кислоты с концентрацией 0,003 моль/л.
4. Найдите активную концентрацию ионов магния в растворе сульфата магния с концентрацией 0,05 моль/л.
Вариант № 2
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HCl, Fe(OH)2, ZnSO4, H2SО3, (FeOH)2SO4, Ca(HSO4)2, (NH4)2Fe(SO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
2. Составьте молекулярные, полные и сокращенные ионно-молекулярные уравнения для следующих реакций:
1) AlCl3 + NаОН ®
2) NаCl + AgNO3 ®
3) HBr + Na2СО3 ®
3. Рассчитайте рН раствора угольной кислоты с концентрацией 0,007 моль/л.
4. Найдите активную концентрацию ионов магния в растворе нитрата магния с концентрацией 0,05 моль/л.
Вариант № 3
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HClO, КOH, Nа2SO4, H2СО3, FeOHSO4, Mg(HSO4)2, КFe(SO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
2. Составьте молекулярные, полные и сокращенные ионно-молекулярные уравнения для следующих реакций:
1) FeSO4 + NаОН ®
2) Ва(NO3)2 + К2SO4 ®
3) НСl + К2СО3 ®
3. Рассчитайте рН раствора уксусной кислоты с концентрацией 0,002 моль/л.
4. Найдите активную концентрацию ионов магния в растворе хлорида магния с концентрацией 0,07 моль/л.
Вариант № 4
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HClO3, Ba(OH)2, CuSO4, H2S, AlOHSO4, Ca(H2PO4)2, NH4Fe(SO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
2. Составьте молекулярные, полные и сокращенные ионно-молекулярные уравнения для следующих реакций:
1) ВаCl2 + Nа2SO4 ®
2) СаСl2 + К2СО3 ®
3) Sr(ОН)2 + НNО3 ®
3. Рассчитайте рН раствора сернистой кислоты с концентрацией 0,008 моль/л.
4. Найдите активную концентрацию ионов натрия в растворе сульфата натрия с концентрацией 0,05 моль/л.
Вариант № 5
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HNO3, NaOH, Fe2(SO4)3, H3AsO4, NaHCO3, CaOHCl, NH4Fe(SO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
2. Составьте молекулярные, полные и сокращенные ионно-молекулярные уравнения для следующих реакций:
1) Н3PO4 + КОН ®
2) Nа2SiО3 + НСl ®
3) АgNО3 + KСl ®
3. Рассчитайте рН раствора синильной кислоты с концентрацией 0,002 моль/л.
4. Найдите активную концентрацию хлорид ионов в растворе хлорида магния с концентрацией 0,045 моль/л.
Вариант № 6
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HClO3, Sr(OH)2, Na2SO4, H2S, (CaOH)2SO4, Mg(HSO4)2, (NH4)2Fe(SO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
2. Составьте молекулярные, полные и сокращенные ионно-молекулярные уравнения для следующих реакций:
1) FeCl2 + NаОН ®
2) K3PO4 + AgNO3 ®
3) HСl + К2SiО3 ®
3. Укажите кислотно–основные сопряжённые пары в уравнениях протолитических реакций:
Вариант № 7
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HClO2, Ba(OH)2, Nа2SiO3, H2SО3, AlOHSO4, Ca(HSO4)2, КAl(SO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
2. Составьте молекулярные, полные и сокращенные ионно-молекулярные уравнения для следующих реакций:
1) CuSO4 + NаОН ®
2) ВаСl2 + К2SO4 ®
3) Н2SO4 + К2СО3 ®
3. Рассчитайте рН раствора уксусной кислоты с концентрацией 0,006 моль/л.
4. Найдите активную концентрацию нитрат ионов в растворе нитрата алюминия с концентрацией 0,08 моль/л.
Вариант № 8
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HClO, Ca(OH)2, ZnSO4, H2SiO3, CrOHSO4, Mg(H2PO4)2, NH4Fe(SO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
2. Составьте молекулярные, полные и сокращенные ионно-молекулярные уравнения для следующих реакций:
1) FeCl3 + NаОН ®
2) Са(NO3)2 + К2СО3 ®
3) Ba(ОН)2 + НNО3 ®
3. Рассчитайте рН раствора метановой кислоты с концентрацией 0,002 моль/л.
4. Найдите активную концентрацию ионов алюминия в растворе сульфата алюминия с концентрацией 0,04 моль/л.
Вариант № 9
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HClO4, Ca(OH)2, Al2(SO4)3, H3PO4, NaHSO3, MgOHCl, KАl(SO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
2. Составьте молекулярные, полные и сокращенные ионно-молекулярные уравнения для следующих реакций:
1) FeSO4 + NаОН ®
2) Ва(NO3)2 + К2SO4 ®
3) НСl + К2СО3 ®
3. Рассчитайте рН раствора сернистой кислоты с концентрацией 0,002 моль/л.
4. Найдите активную концентрацию нитрат ионов в растворе нитрата бария с концентрацией 0,07 моль/л.
Вариант № 1 0
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HClO2, Ba(OH)2, Nа2SiO3, H2SО3, AlOHSO4, Ca(HSO4)2, КAl(SO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
2. Составьте молекулярные, полные и сокращенные ионно-молекулярные уравнения для следующих реакций:
1) Н3PO4 + КОН ®
2) Nа2SiО3 + НСl ®
3) АgNО3 + KСl ®
3. Рассчитайте рН раствора синильной кислоты с концентрацией 0,007 моль/л.
4. Найдите активную концентрацию ионов хрома в растворе сульфата хрома с концентрацией 0,04 моль/л.
Образец выполнения письменных заданий:
1. Какие электролиты диссоциируют необратимо, а какие - обратимо? Покажите это на примерах следующих электролитов: HNO3, HNO2, LiOH, Mg(HSO4)2. Назовите все образующиеся ионы по номенклатуре ИЮПАК.
Ответ: HNO3 ® H+ + NO 
ион водорода нитрат-ион
HNO2 ↔ H+ + NO 
ион водорода нитрит-ион
LiOH ® Li+ + OH─
ион лития гидроксид-ион
Mg(HSO4)2 ® Mg2+ + 2HSO 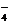
ион магния гидросульфат-ион
2. Составьте молекулярное, полное и сокращенное ионно-молекулярные уравнения для следующей реакции:
Fe(OH)2 + H2SO4®
Ответ: Fe(OH)2 + H2SO4 ® FeSO4 + 2H2O
Fe(OH)2 + 2H+ + SO ® Fe2+ + 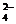
SO + 2H2O
Fe(OH)2 + 2H+ ® Fe2+ + 2H2O
Тема 6.
Равновесные процессы в растворах электролитов.
Теории кислот и оснований. Произведение растворимости.
Гидролиз солей. Буферные растворы.
Вопросы для самостоятельной внеаудиторной подготовки к занятию:
1. Какие достоинства и недостатки имеет теория кислот и оснований С. Аррениуса?
2. Дайте определения кислоте и основанию с позиций протолитической теории. Что называется кислотно–основной сопряжённой парой?
3. Какие достоинства и недостатки имеет протолитическая теория кислот и оснований?






