соли в зависимости от состава делят на три типа:
1. простые соли: построены из одного вида положительных и одного вида отрицательных ионов (K2SO4, NaCl, KCl).
2. Двойные (смешанные соли): соединения, построенные из двух и более типов солей. Они устойчивы в кристаллическом состоянии, но при растворении в воде они распадаются на ионы, причем каждая соль растворяется независимо. Например, KCl·MgCl2·6H2O при растворении распадается на ионы К+, Mg2+, Cl-
3. Комплексные соли: построены из двух или более типов солей. И в кристалле и в водном растворе проявляют свойства, отличные от каждой составляющей соли.
Fe(CN)2 + 4KCN → K4[Fe(CN)6];
HgJ2 + 2KJ → K2[HgJ4].
Молекулярные соединения, сочетания компонентов которых приводит к образованию сложных ионов, способных к свободному существованию как в кристалле, так и в растворе называются комплексными соединениями или просто комплексами (координационные соединения).
Свойства и строение комплексных соединений (к.с.) объясняет координационная теория, предложенная в 1895 г. швейцарским химиком Альфредом Вернером.
 Строение комплексных соединений:
Строение комплексных соединений:
Согласно координационной теории, в молекуле любого к.с. один из ионов, обычно положительно заряженный, занимает центральное место и называется комплексообразователем (к.о.) или центральным ионом. Вокруг него в непосредственной близости расположено или, как говорят, координировано некоторое число противоположно заряженных ионов или электронейтральных молекул, называемых лигандами (или аддентами), образующих внутреннюю сферу соединения. Остальные ионы, не разместившиеся во внутренней сфере, находятся на более далеком расстоянии от центрального атома или иона, составляя внешнюю сферу. Внутренняя сфера комплекса сохраняет стабильность при растворении. Ее границы обозначают квадратными скобками. Ионы, находящиеся во внешней сфере в растворах легко отщепляются.
Координационное число (к.ч.) – количество образуемых комплексообразователем σ-связей, чаще всего оно равно числу лигандов, если они монодентатные, т.е. образуют по одной σ-связи с комплексообразователем и занимают одно место в координационной сфере.
Между к.о. и лигандами σ-связи возникают по обменному или донорно-акцепторному механизму
В роли к.о. может выступать любой элемент ПС. Но наибольшую склонность к комплексообразованию проявляют:
1) d-элементы как в виде катионов, так и в свободном виде:


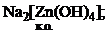


2) р-элементы в высокой степени окисления:



3) значительно реже – щелочные и щелочноземельные металлы. В водных растворах ионы этих металлов находятся в виде аквакомплексов: 






