4.1.1 Создание конструкции in vitro
Так как не было уверенности, какой терминатор выбрать, решено создать две конструкции: одна будет нести в себе терминатор TL (далее конструкция рCu-asFur-TL), а другая терминаторы T1 и T2 последовательно (далее конструкция РCu-asFur-T12). Для объединения промотора и гена asRNA, а также внесения терминатора, мы выбрали метод overlap ПЦР (!!!!!!!!!!). С плазмиды pSK9 амплифицировали участок, содержащий промотор PрetJ (далее рCu) с помощью праймеров MidCat-r2 и PpetJ/5’asFur (Табл.2). Последний в своей 5’области содержал участок, гомологичный последовательности asRNA гена fur (далее asFur). С хромосомы дикого типа амплифицировали последовательность asFur с использованием праймеров 5’asFur/PpetJ-c (содержит на 5’-конце область гомологии с рCu) и 3’asFur-T12(Bgl) (Табл. 2) для рCu-asFur-T12 и 5’asFur/PpetJ-c и 3’asFur-TL(Bgl) (Табл. 2) для рCu-asFur-TL. Праймер MidCat-r2 на 5’-конце содержал сайт рестрикции для EcoRI, а 3’asFur-TL(Bgl) и 3’asFur-T12(Bgl) на своем 5’-конце несли сайт рестрикции для BglII. Результаты первого ПЦР представлены на рис.1. Получены ПЦР-фрагменты pCu (852 п.н.), asFur-T12 (225 п.н.) и asFur-TL (173 п.н.).

Рис.1 Первый этап pfu-ПЦР фрагментов для построения конструкции pPetJ-asFur-T
Лунки 1-2 фрагмент pPetJ с матрицы pSK9 и праймерами MidCatR2 и 5’asFur/pPetJ-c
Лунки 3-4 фрагмент asFur-Т12 с матрицы хромосомы дикого типа и праймерами pPetJ/5’asFur и 3’asFurT12(BglII)
Лунки 5-6 фрагмент asFur-TL с матрицы хромосомы дикого типа и праймерами pPetJ/5’asFur и 3’asFurTL (BglII)
 На втором этапе поставили ПЦР для объединения участков. Для получения pCu-asFur-TL (рис.2а) (965 п.н.) в качестве матрицы использовали продукты pCu и asFur-TL, праймеры MidCat-r2 и 3’asFur-TL(Bgl). Соответственно, для получения pCu-asFur-T12 (рис.2б) (1017 п.н.) матрицей служили pCu и asFur-T12, праймеры MidCat-r2 и 3’asFur-T12. В результате получили продукты предсказанного размера (рис.3)
На втором этапе поставили ПЦР для объединения участков. Для получения pCu-asFur-TL (рис.2а) (965 п.н.) в качестве матрицы использовали продукты pCu и asFur-TL, праймеры MidCat-r2 и 3’asFur-TL(Bgl). Соответственно, для получения pCu-asFur-T12 (рис.2б) (1017 п.н.) матрицей служили pCu и asFur-T12, праймеры MidCat-r2 и 3’asFur-T12. В результате получили продукты предсказанного размера (рис.3)
А

Б
Рис.2

Рис.3 Второй этап pfu-ПЦР-overlap фрагмента pPetJ-asFur-T12 (колонка 1 и 2) и pPetJ-asFur-TL (колонка 3 и 4).
Полученный продукт элюировали из геля с помощью коммерческого набора???????????. Используя набор CloneJet (Thermo Scientific), клонировали очищенный продукт вектор положительной селекции pJet (рис.4).

Трансформированные клетки E. coli и отбирали на среде с ампицилином. Далее из них выделили рекомбинантную плазмиду, обозначенную pJet-asFur-TL (рис. 5.а и б) и pJet-asFur-T12 (рис 5. в и г).



А Б

В Г
Рис.5. Физические карты рекомбинантных плазмид pJet-asFur-TL(А, Б) и pJet-asFur-T12 (В,Г). Слева прямой направление вставки, справа-обратное.
Для проверки ориентации вставки использовали рестриктазы EcoRI и XhoI. В результате, выбранные нами клоны 3 (pPetJ-asFur-T12)и 7 (pPetJ-asFur-TL) имеют обратную ориентацию вставки (рис. 6).
РИСУНОК 6
Конечный этап работы – встраивание конструкции в вектор pSK9, несущий область гомологии к незначащему участку генома Synechocystis sp. Для этого плазмиды pPetJ-asFur-T12 и pPetJ-asFur-TL были выделены и обработы рестриктазами EcoRI и BglII, после чего вырезанный фрагмент очистили и элюировали из геля. Этими же рестриктазами обработали вектор pSK9, очистив на колонке. В результате лигирования был получен конечный вектор для трансформации Synechocystis sp. (рис. 7 а и б).
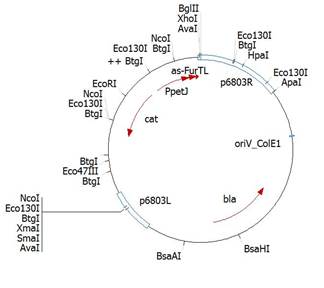

А Б
Рис.7 Физические карты вектора pSK9-pCu- asFur-T12 (А) и pSK9-pCu- asFur-TL (Б). Показана область гомологии с участком хромосомы p6803L и p6803R со встроенным по сайтам EcoRI и BglII фрагментом между ними.
Секвенирование с праймерами Up-PpetJ-s, PpetJ-sr1, PpetJ-sr2, Plat_6803-r, MidCat-r2, asFur-s показало, что последовательность asFur осталась неизменной, но найдена замена основания в предположительно незначащей области промотера, также было обнаружено, что праймер 3’asFur-T12(Bgl) не содержи сайта рестрикции для BglII.
Трансформантов Synechocystis sp. отбирали на среде с хлорамфениколом, так как вектор содержат маркер устойчивости bla.
Сегрегировали на среде с повышенным содержанием меди и хлорамфениколом.
Как правило, функциональный анализ гена подразумевает его инактивацию и изучение фенотипа полученного мутанта. Однако известные попытки инактивации гена fur (sll0567) у цианобактерий Synechocystis 6803 (Kunert et al., 2003) и Anabaena sp. PCC 7120 (Gonzalez et al., 2010) с получением гомозиготных мутантов оказались неудачными, что служит свидетельством жизненно важной функции этого гена. В нашей работе была поставлена задача сконструировать условный мутант, у которого ген fur может быть выключен в определенных условиях. С этой целью использовали следующий подход. Ген fur инактивировали инсерцией Sp-кассеты, после чего в нефункциональную часть генома гетерозиготного мутанта ввели копию гена fur под контролем промотора гена petJ (P petJ), экспрессия которого полностью подавляется микромолярной концентрацией меди в среде (Zhang et al., 1992; Tous et al., 2001; Peter et al., 2009). Таким образом, за счет функционирования копии гена fur под контролем P petJ при росте клеток в среде без добавления меди можно ожидать успешной сегрегации гомозиготного мутанта с инактивированным геном fur в его исходном локусе генома. Далее у такого мутанта можно исследовать физиолого-биохимические характеристики и изменения в экспрессии генов предполагаемого fur -регулона в условиях выключения копии гена fur под контролем P petJ – при инкубации клеток в среде с добавлением меди.
4.1. Конструирование мутантных штаммов Synechocystis 6803 с инактивацией гена fur и/или с введением в геном копии fur под контролем зависимого от меди промотора
Конструирование штамма с инактивацией гена fur
На первом этапе работы с помощью ПЦР (праймеры Fur-f и Fur-r; табл. 2) амплифицировали участок хромосомы штамма ДТ Synechocystis 6803, содержащий ген fur. Полученный ПЦР-фрагмент в 1,33 т.п.н. клонировали в векторе pGEM-T и из клеток трансформантов E. coli выделили рекомбинантную плазмиду, обозначенную pGMFUR (рис. 2А); по сайтам Eco RI полилинкера из этой плазмиды вырезался фрагмент ДНК ожидаемого размера – 1,33 т.п.н. (рис. 3А). Для определения ориентации гена fur в плазмиде использовали рестриктазу Nde I; в результате был выявлен фрагмент размером 1,28 т.п.н. (данные не приведены), что свидетельствовало об одном направлении транскрипции гена fur и плазмидного маркера bla (рис. 2А). С целью инактивации гена fur в составе рекомбинантной плазмиды часть его вырезали (делеция) по сайтам Van 91I и Cla I и после затупления концов ДНК с помощью фрагмента ДНКПI Кленова оставшуюся часть плазмиды лигировали со Sp-кассетой. Таким способом была сконструирована плазмида pGMFUR-Sp, в которой ген aadA кассеты транскрибируется в направлении, противоположном направлению транскрипции гена fur (Рис. 2Б). Ориентация Sp-кассеты была установлена с помощью обработки плазмиды pGMFUR-Sp рестриктазой Sph I, в результате которой выявили фрагмент ДНК размером 2,43 т.п.н. (рис. 3Б).

Рис. 2. Физические карты рекомбинантных плазмид pGMFUR (А) и pGMFUR-Sp (Б). Плазмида pGMFUR-Sp является производной плазмиды pGMFUR, в которой часть гена fur между сайтами Van 91I и Cla I замещена Sp-кассетой, содержащей ген ааdА.

Рис. 3. Рестрикционный анализ рекомбинантных плазмид pGMFUR (А) и pGMFUR-Sp (Б), в каждом случае выделенных из трех трансформантов E. coli (1, 2, 3), отобранных в одном опыте. Использованные рестриктазы: Eco RI (А) и Sph I (Б).
М – маркерные фрагменты ДНК. Стрелками указаны фрагменты плазмид в т.п.н.
На следующем этапе работы штамм ДТ Synechocystis 6803 трансформировали плазмидой pGMFUR-Sp, в результате чего были отобраны устойчивые к спектиномицину трансформанты. Один из полученных трансформантов использовали в качестве несегрегированного мутантного штамма, обозначенного Δfur.
Конструирование мутантных штаммов с введением в геном копии fur под контролем зависимого от меди промотора
Для клонирования гена fur под контролем промотора P petJ использовали сконструированный в нашей лаборатории вектор pVZExCu (рис. 4). Вектор является производным рекомбинантной плазмиды с «платформой p6803» – клонированным фрагментом генома Synechocystis 6803 с протяженным нетранслируемым участком между встречно направленными генами (Los et al., 2003). Фрагмент этого нетранслируемого участка, простирающегося до сайта Bgl II в правом плече платформы (в направлении от сайта Nde I вектора), замещен рекомбинантной конструкцией, которая содержит промотор P petJ и сцепленный с ним маркер устойчивости к Cm, cat. Клонирование генов в векторе pVZExCu осуществляется с использованием сайтов Nde I и Cla I (на карте не указан) или Nde I и Bgl II (рис. 4).
C помощью Pfu -ПЦР с использованием праймеров Fur-Nde-f и Fur-Bgl-r (табл. 2), а также хромосомы штамма ДТ Synechocystis 6803 в качестве матрицы, был амплифицирован фрагмент ДНК размером около 500 п.н., содержащий только кодирующую часть гена fur. Полученный ПЦР-фрагмент был обработан рестриктазами Nde I и Bgl II, сайты рестрикции которых введены в состав соответствующих праймеров, и лигирован с ДНК вектора pVZExCu, обработанного теми же рестриктазами и щелочной фосфатазой CIAP (Fermentas). В результате была сконструирована рекомбинантная плазмида pCuFur, в которой ген fur находится под контролем промотора P petJ (рис. 4). Контрольное секвенирование плазмиды pCuFur с праймерами Fur-Nde-f и Fur-Bgl-r с полным перекрыванием клонированного гена fur в обоих направлениях показало, что кодирующая последовательность гена осталась неизменной (в сравнении с последовательностью из CyanoBase), причем, стартовый кодон ATG и стоп-кодон TAG перекрываются сайтами Nde I и Bgl II, как ожидали.

Рис. 4. Физическая карта участка вектора pVZExCu и рекомбинантной плазмиды на его основе pCuFur, в которой ген fur встроен между сайтами Nde I и Bgl II с замещением соответствующего фрагмента вектора. Неокрашенные прямоугольники обозначают части платформы p6803 из генома цианобактерии Synechocystis 6803 (Los et al., 2003). Показаны промотор P petJ и маркер устойчивости к Cm, cat. Загнутые стрелки указывают положение праймеров для ПЦР-анализа рекомбинанатной области генома, образующейся при встраивании конструкции с геном fur в платформу p6803.
С помощью трансформации мутанта Δfur плазмидой pCuFur были получены трансформанты с селективным маркером устойчивости к Cm, свидетельствующим о встраивании копии гена fur под контролем промотора P petJ в нефункциональный участок генома (платформа p6803; Los et al., 2003). В настоящее время три мутантных клона, обозначенных Δfur/CuFur, поддерживаются на агаризованной среде с двумя антибиотиками, Cm (5 мкг/мл) и Sp (в ходе последовательных пересевов концентрация повышена с 5 до 50 мкг/мл). Проводится дальнейшая сегрегация этих клонов с использованием селективной среды без добавления меди для получения гомозиготного мутанта с инактивированным геном fur в его исходном локусе генома.
Тем же способом получен штамм CuFur, производный ДТ, который содержит интактный ген fur и его копию под контролем промотора P petJ. Этот штамм, поддерживаемый на селективной среде с более высокой концентрацией Cm (20 мкг/мл), сконструирован с целью изучения регуляторной функции гена fur при его сверхэкспрессии. Аналогичный подход был использован ранее для цианобактерии Anabaena sp. PCC 7120. В данном случае ген furA (гомолог fur Synechocystis 6803), находящийся под контролем активируемого медью промотора P petE, был введен в штамм ДТ на конъюгативной плазмиде (Gonzalez et al., 2010). При сверхэкспрессии furA в клетках, инкубируемых в среде с добавлением меди, выявлены существенные изменения в экспрессии ряда генов, включая гены, кодирующие каталазу и супероксидисмутазу, белок D1 фотосистемы II (ген psbA), актины (гены mreBCD) и рецептор сидерофора шизокинина в наружной мембране (ген schT). Более того, установлено, что гены psbA, mreBCD и schT регулируются непосредственно геном furA.






