Лактоза - углевод группы дисахаридов, содержится в молоке и молочных продуктах. Молекула лактозы состоит из остатков молекул глюкозы и галактозы C12H22O11. Лактозу иногда называют молочным сахаром.

С химической точки зрения лактоза относится к классу восстанавливающих углеводов, которые способны отдавать электроны с разрывом собственной кислородной связи. Лактоза отличается свойствами слабой кислоты, поэтому способна реагировать с гидроксидом натрия (едкий натр). Один моль лактозы может нейтрализовать два моля гидроксида натрия. В целом лактоза является химически довольно активным веществом, поскольку в ее структуре имеются спиртовые функциональные группы, а также молекула способна принимать форму альдегида. Связь между молекулой глюкозы и галактозы в соединении лактозы осуществляется посредством кислорода, и называется гликозидной. Участвуя в химических реакциях, лактоза может распадаться на моносахара именно за счет разрыва гликозидной связи. Разрыв данной гликозидной связи может осуществляться под действием специальных ферментов (лактазы), или при помощи гидролиза в растворах сильных кислот. Чаще всего для химического гидролиза лактозы применяют серную и соляную кислоты, причем скорость протекания этого процесса зависит от температуры. Чем выше температура - тем быстрее происходит гидролиз лактозы под действием кислот. При помещении лактозы в растворы щелочей (например, едкого натра) она распадается до кислот с сохранением сахариновой структуры. Это означает, что щелочи приводят к распаду лактозы на два моносахарида, с образованием у каждого из них активной кислотной группы, превращающей соединение в кислоту. Процесс щелочного гидролиза лактозы зависит от температурного режима. Ферментативный гидролиз лактозы осуществляется лактазами или бета-галактозидазой, которые нарабатываются микроорганизмами нормальной микрофлоры кишечника. Кроме гидролиза лактоза подвергается процессу брожения, в результате которого получаются разнообразные кисломолочные продукты и сыры.
Саму лактозу получают из молочной сыворотки в процессе сушки. Лактозу используют при производстве такого препарат как — пенициллин, а так же для многих других медицинских препаратов.
Применяют для приготовления детского питания. Служит отличной заменой женского молока при кормлении младенца. Входят в состав кормовых витаминов. Все процессы изготовления продуктов потребления включают в себя лактозу. Например, при выпечке хлебных изделий лактозу применяют, чтобы получить вкусную красивую коричневую корочку. В кондитерской сфере это вещество придает вкусовые качества конфетам и другим сладостям. Без лактозы не обходиться не одна шоколадка мармелад, сгущенное молоко, и много других продуктов. Компонент лактозы содержится в диабетических продуктах. В мясные продукты добавляют для того чтобы убрать горечь и соленость и таким образом продлевается время хранения мясного продукта. Так же добавляется в алкогольные напитки для смягчения вкусовых качеств.
Содержится лактоза в продуктах в граммах на 100 г продукта:
| Сыворотка сухая | |
| Молоко сухое обезжиренное | |
| Молоко пастеризованное (3,5%-ное) | 4,8 |
| Кефир | |
| Творог обезжиренный | 3,2 |
| Творог (20%-ный) | 2,7 |
| Сметана (10%-ная) | 2,5 |
| Масло сливочное | 0,6 |
| Молоко нежирное | 4,9 |
| Молочный шоколад | 9,5 |
Гликоген - полисахарид, образованный остатками глюкозы, связанными α-1→4 связями (α-1→6 в местах разветвления); основной запасной углевод животных. Гликоген является основной формой хранения глюкозы в животных клетках. Откладывается в виде гранул в цитоплазме во многих типах клеток (главным образом печени и мышц)

Гликоген иногда называется животным крахмалом, так как его структура похожа на амилопектин — компонент растительного крахмала. В отличие от крахмала, гликоген имеет более разветвленную и компактную структуру, не дает синей окраски при окраске йодом.
Гликоген образует энергетический резерв, который может быть быстро мобилизован при необходимости восполнить внезапный недостаток глюкозы. Гликогеновый запас, однако, не столь ёмок в калориях на грамм, как запас триглицеридов (жиров). Только гликоген, запасённый в клетках печени (гепатоциты) может быть переработан в глюкозу для питания всего организма. Содержание гликогена в печени при увеличении его синтеза может составить 5-6% от массы печени. Общая масса гликогена в печени может достигать 100—120 грамм у взрослых. В мышцах гликоген перерабатывается в глюкозу исключительно для локального потребления и накапливается в гораздо меньших концентрациях (не более 1 % от общей массы мышц), в то же время его общий мышечный запас может превышать запас, накопленный в гепатоцитах. Небольшое количество гликогена обнаружено в почках, и ещё меньшее — в определённых видах клеток мозга (глиальных) и белых кровяных клетках.
Гликоген синтезируется в период пищеварения (через 1-2 ч после приёма углеводной пищи). Следует отметить, что синтез гликогена из глюкозы как и любой анаболический процесс, является эндергоническим, т.е. требующим затрат энергии.
Глюкоза, поступающая в клетку, фосфорилируется при участии АТФ (реакция 1). Затем глюкозо-6-фосфат в ходе обратимой реакции превращается в глюкозо-1 -фосфат (реакция 2) под действием фермента фосфоглюкомутазы. Глюкозо-1-фосфат по термодинамическому состоянию мог бы служить субстратом для синтеза гликогена. Но в силу обратимости реакции глюкозо-6-фосфат ↔ глюкозо-1-фосфат синтез гликогена из глюкозо-1-фосфата и его распад оказались бы также обратимыми и поэтому неконтролируемыми. Чтобы синтез гликогена был термодинамически необратимым, необходима дополнительная стадия образования уридинди-фосфатглюкозы из УТФ и глюкозо-1-фосфата (реакция 3). Фермент, катализирующий эту реакцию, назван по обратной реакции: УДФ-глюкопирофосфорилаза. Однако в клетке обратная реакция не протекает, потому что образовавшийся в ходе прямой реакции пирофосфат очень быстро расщепляется пирофосфатазой на 2 молекулы фосфата. Реакция образования УДФ-глюкозы обусловливает необратимость всей серии реакций, протекающих при синтезе гликогена. Этим же объясняется невозможность протекания распада

Синтез гликогена. 1 - глюкокиназа или гексокиназа; 2 - фосфоглюкомутаза; 3 - УДФ-глюкрпирофосфорилаза; 4 - гликогенсинтаза (глюкозилтрансфераза); 5 - фермент "ветвления" (амило-1,4 → 1,6-глюкозилтрансфераза), светлые и заштрихованные кружки - глюкозные остатки, закрашенные кружки - глюкозные остатки в точке ветвления.
К продуктам богатым гликогеном относятся: печень,рыба,мясо.
Гиалуроновая кислота - несульфированный гликозаминогликан, входящий в состав соединительной, эпителиальной и нервной тканей. Является одним из основных компонентов внеклеточного матрикса, содержится во многих биологических жидкостях (слюне, синовиальной жидкости и др.). Принимает значительное участие в пролиферации и миграции клеток. Продуцируется некоторыми бактериями (напр. Streptococcus). В теле человека весом 70 кг в среднем содержится около 15 граммов гиалуроновой кислоты, треть из которой преобразуется (расщепляется или синтезируется) каждый день.
В организме гиалуроновая кислота присутствует в форме соли, гиалуроната, и обнаружена в высоких концентрациях в некоторых мягких соединительных тканях, в составе кожи, пуповины, синовиальной жидкости, и стекловидного тела. Значительное количество гиалуроновой кислоты найдено также в легких, почках, головном мозге, и мышечных тканях. При промышленном производстве гиалуроновая кислота обычно экстрагируется из гребня петуха и человеческой пуповины, или же производится в больших количествах путем бактериальной ферментации. Клеточный синтез гиалуроновой кислоты является очень своеобразным и тщательно контролируемым процессом. Большинство гликозаминогликанов синтезируется в аппарате Гольджи. Гиалуроновая кислота, однако, синтезируется на цитоплазматической мембране и сразу же транспортируется наружу в межклеточный матрикс. Этот процесс осуществляется группой белков, называемых ГК-синтазами, которые расположены в клеточной мембране.
Структура гиалуроновой кислоты обеспечивает уникальные физико-химические и биологические свойства, которые находятся в зависимости от молекулярного веса. Если экстрагировать гиалуроновую кислоту из тканей, она полидисперсна по размеру, со средним молекулярным весом в несколько миллионов. В физиологическом растворе, гиалуроновая кислота формирует ригидные спирали случайного размера, длина периметра в них около 2.5 мкм на каждую цепь массой 1*106, содержащую порядка 2650 дисахаридных повторов. Вторичные водородные связи формируются вдоль оси гиалуроновой кислоты, обеспечивая стабильность и формируя гидрофобные участки, благодаря чему гиалуроновая кислота организуется в упорядоченные структуры. Раствор гиалуроновой кислоты обладает высокой вязкоэластичностью, другими словами, при увеличении скорости сдвига цепи гиалуроновой кислоты выстраиваются по направлению движения, что приводит к снижению вязкости раствора. Этот эффект снижения вязкости можно наблюдать при выдавливании гиалуроновой кислоты из шприца. Гиалуроновая кислота – высоко-гидрофильный полимер. Каждая единица гиалуроновой кислоты содержит карбоксильную группу, благодаря чему при физиологическом pH возрастает полианионный характер ГК. В присутствии воды молекулы ГК могут увеличиваться в объеме в 1000 раз и формировать слабоупакованный гидратированный матрикс. Благодаря этому свойству, гиалуроновая кислота выполняет несколько функций во внеклеточном матриксе: она действует как заполнитель объема, смазочный материал, и осмотический буфер. Сеть из гидратированных полимеров гиалуроновой кислоты может действовать как сито, ограничивая движение патогенов, белков плазмы и протеаз. Кроме того, полионная структура ГК способна захватывать свободные радикалы, обладая вследствие этого антиоксидантными свойствами и принимая участие в регуляции воспалительного процесса.
Гиалурановая кислота содержится в таких продуктах как, соевые продукты, красные натуральные вина, плоды, источники животного происхождения. Гиалурановую кислоту можно обнаружить в гребнях петухов и кур, а также в отваре из куриных лап. Особенно богаты этим веществом наваристые мясные бульоны, приготовленные с использованием в качестве сырья не только мяса, но и костей, кожи и сухожилий. Традиционный бульон из курицы или холодец из индейки, свинины – богаты гиалуроновой кислотой и рекомендуются в пищу в качестве источника этого вещества. Именно животная пища является основным поставщиком гиалуроната.
Хондроитинсульфаты- полимерные сульфатированные гликозаминогликаны. Являются специфическими компонентами хряща. Вырабатываются хрящевой тканью суставов, входят в состав синовиальной жидкости. Необходимым строительным компонентом хондроитинсульфата, является глюкозамин, при недостатке глюкозамина в составе синовиальной жидкости образуется недостаток хондроитинсульфата, что ухудшает качество синовиальной жидкости и может вызвать хруст в суставах. Известно несколько типов хондроитинсульфатов. Наиболее изучены 4 представителя, которые принято обозначать буквами латинского алфавита: хондроитинсульфат А(хондроитин-4-сульфат),B(дерматансульфат),C(хондроитин-6-сульфат),D(кератансульфат).
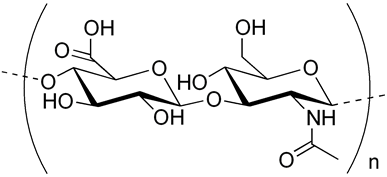
Макромолекулы хондроитинсульфата А (хондроитин-4-сульфата) состоят из чередующихся звеньев остатковβ-D-глюкуроновой кислотыи4-сульфат-N-ацетил-β-D-галактозамина, соединенныхβ-(1→3)-гликозидными связями. Дисахаридные остатки соединеныβ-(1→4)-гликозидными связями
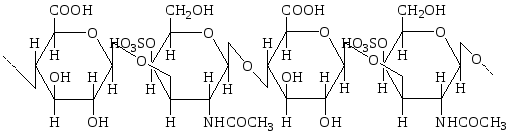
Хондроитинсульфат С (хондроитин-6-сульфат) и хондроитинсульфат А (хондроитин-4-сульфат) построены по одному принципу. Отличие между ними заключается в локализации сульфатной группы. Дисахаридный фрагмент хондроитин-6-сульфата включает звенья остатковβ-D-глюкуроновой кислотыи6-сульфат-N-ацетил-β-D-галактозамина, соединенныхβ-(1→3)-гликозидными связями.Дисахаридные фрагменты связаныβ-(1→4)-гликозидными связями.
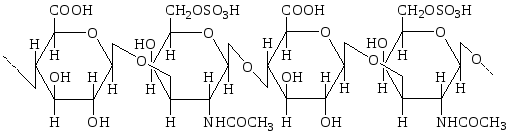
Хондроитинсульфат В (дерматансульфат) построен из чередующихся остатковα-L-идуроновой кислотыи4-сульфат-N-ацетил-β-D-галактозамина, соединенныхβ-(1→3)-гликозидными связями. Дисахаридные фрагменты связаныβ-(1→4)-гликозидными связями.

В отличие от остальных гликозаминогликанов макромолекулы хондроитинсульфата D (кератансульфата) не содержат звенья остатков глюкуроновой и идуроновой кислот. Дисахаридная единица состоит из звеньев остатковβ-D-галактопиранозыиN-ацетил-D-глюкозамин-6-сульфата, соединенных β-(1→4)-гликозидными связями. Дисахаридные фрагменты соединены β-(1→3)-гликозидными связями

Один из наиболее богатых источников хондроитинсульфатов – хрящ носовой перегородки(20-40%). Поскольку ткань хряща наряду с хондроитинсульфатами содержит большое количество коллагена, при получении полисахаридов из биомассы необходимо отделить белковую часть. Наилучший метод выделения – экстракция хлоридом калия. В полученный экстракт добавляют ацетатный буфер для осаждения коллагена. Затем уделяют примеси адсорбцией на каолине. Полученный фильтрат подвергают диализу от низкомолекулярных соединений. К диализованному раствору вновь добавляют ацетатный буфер и пропускают через колонку с коалином. (Для очистки хондроитинсульфатов от низкомолекулярных примесей можно использовать также препаративный электрофорез.) Фильтрат упаривают в вакууме и осаждают хондроитинсульфат концентрированным раствором этилового спирта.
Хондроитинсульфаты содержатся в коже, сухожилиях, костном мозге и хрящах животных и в еще большей степени в рыбе (особенно лосось, семга, колючая акула или катран, скаты, осетровые).
Гепари́н — кислый серосодержащий гликозаминогликан; впервые выделен из печени. В клинической практике известен как прямой антикоагулянт, то есть как вещество, препятствующее свёртыванию крови. Применяется для профилактики и терапии тромбоэмболических заболеваний, при операциях на сердце и кровеносных сосудах, для поддержания жидкого состояния крови в аппаратах искусственного кровообращения и гемодиализа, а также для предотвращения свертывания крови при лабораторных исследованиях. Синтезируется в тучных клетках, скопления которых находятся в органах животных, особенно в печени, лёгких, стенках сосудов.

Гепарин относится к семейству гликозаминогликанов; его молекула представлена несколькими полисахаридными цепями, связанными с общим белковым ядром. Белковое ядро же включает в свой состав в основном остатки двух аминокислот: серина и глицина. Приблизительно две трети сериновых остатков как раз и связывается с полисахаридными цепями. В основе последних лежит цепочка из повторяющихся дисахаридов - α-D-глюкозамин и уроновая кислоты, соединенные 1-4 гликозидными связями. Большинство остатков α-D-глюкозамина сульфатировано по амино- и гидроксильной группе; небольшая часть аминогрупп может быть ацетилирована. Звенья уроновой кислоты представляют собой остатки L-идуроновой кислоты (~90%) или эпимерные остатки D-глюкуроновой кислоты (~10%). Благодаря наличию значительного количества отрицательно заряженных сульфатных и карбоксильных групп, молекула гепарина представляет собой сильный природный полианион, способный к образованию комплексов со многими белковыми и синтетическими соединениями поликатионной природы, несущими суммарный положительный заряд.
Длина полисахаридных цепей эндогенного гепарина может быть разной, а, значит, и молекулярная масса его тоже колеблется в широких пределах - от 3000 до 40000 дальтон. Средняя молекулярная масса «коммерческих» гепаринов, используемых в качестве лекарственных препаратов, колеблется в более узких пределах - от 12000 до 16000 дальтон. В последнее время была получена группа низкомолекулярных гепаринов, обладающая дополнительными свойствами.
Субстратами для биосинтеза гепарина являются глюкоза и неорганический фосфат. Присоединение сульфатных групп осуществляется после полимеризации, но некоторые ученые) предполагают, что сульфатирование происходит на более ранних этапах, то есть ещё на уровне низкомолекулярных предшественников. Среди ферментов участвующих в биосинтезе гепарина выделяют различные гликозилтрансферазы, сульфотрансферазы, эпимеразы, многие из которых выделены в чистом виде.
Основным продуктом, содержащим большое количество гепарина является печень.
Почти вся информация взята из Википедии.






