Алмасу реакциясы тән комплекстік иондар
Ag(CN22-: K_t=1.0*〖10〗^(-21)
Fe(CN63-: K_t=1.0*〖10〗^(-31)
Атомдардың металлдық қасиеттері артады:
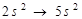
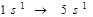
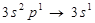
Атомдардың бейметалдық қасиеттері артады:
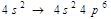
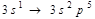
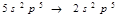
Амфотерлі қасиет көрсететін гидроксидтер:
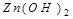 және
және 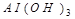
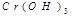 және
және 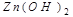
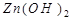 және
және 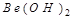
Азот қышқылының 10%-тік ерітіндісін дайындау үшін тығыздығы 1,4 г/см3 200 мл 68%–тік қышқыл ерітіндісіне қосуға қажетті су көлемі:
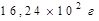
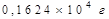
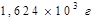
Алюминий нитраты ерітіндісі үшін:
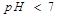
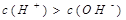
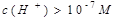
Анионы бір мезгілде электролиттік диссоциация және гидролиздену үрдістеріне ұшырайтын тұз:
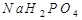
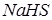
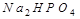
Азот ТТР-да тотықтырғыш та, тотықсыздандырғыш та ролін атқаратын қосылыс:
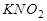
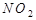
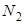
Ас тұзы ерітіндісінің электролизінде бөлінетін заттар:
H2
Cl2
NaOH
Атомдық орбитальдардың қаптасуынан түзілетін сигма байланыс:
В) р(х) –р(х)
Анотта судың тотығуы мүмкін болатын тұздың ерітіндісі:
Д) K2SO4
G) Na2CO3
Атомдардың электртерістігі (ЭТ) мәндеріне байланысты күшті полярлы байланысқан заттар:
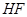 ; эo(н)=2,1; эo(f)=4,0
; эo(н)=2,1; эo(f)=4,0
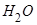 ; эo(н)=2,1; эo(о)=3,5
; эo(н)=2,1; эo(о)=3,5
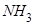 ; эo(н)=2,1; эo(n)=3,0
; эo(н)=2,1; эo(n)=3,0
Анодта су молекулалары тотығуы мүмкін тұздар ерітінділері:
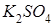
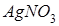
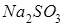
Анодта су молекулалары тотығуы мүмкін тұз ерітіндісі:
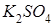
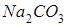
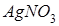
Бөлшектердің тотығу дәрежелері өзрегеді реакцияларда:
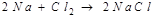
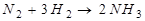
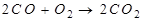
Бертолет тұзының (формуласын белгіле) 245 г алу үшін жұмсалған гидроксид пен хлордың зат мөлшері:
он екі моль сілті
алты моль хлор
калий хлораты
Бейтарап атом оң зарядталған ионға айналады:
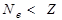
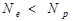
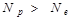
Бейтарап атом теріс зарядталған ионға айналады:
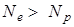
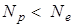
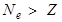
Бейметал атомдарының электрондық құрылысының ерекшеліктері:
соңғы электрон р-деңгейшені толтырады
электртерістігі екіден жоғары
атомдардың сыртқы электрондарының саны төрттен көп
Бірінші А және жетінші А топтар элементтері атомдарының арасындағы байланыс:
иондық
ковалентті күшті полюсті
коваленттік үлеспен иондық
Бериллий хлориді молекуласының геомертиялық пішіні жэне валенттік бұрышы, гибридтену типі:

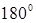
сызықтық
Байланыс табиғаты сутектік зат:
фторсутек қышқылы
су
амин қышқылы
Бейтарап орта үшін:
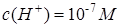
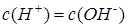
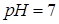
Гидроксидтері, суда еритін тұздарын сілтімен әрекеттестіріп, алмасу реакциясы нәтижесінде алынатын металдар:
Cu, Zn
Mg, Zn
Ni, Mg
Гидроксо- тұз түзіледі реакция барысында:
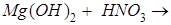
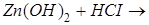
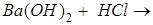
Гомегнді реакция
N2+3H2--- 2NH3
2CO+O2---2CO2
HNO3+KOH---KNO3+H2O
Гетерогенді реакция:
А) FeO+C<->Fe+CO
C) CaO+CO2-> CaCO3
E)Fe+CuCl2 -> FeCl2 +Cu
Гидролиз реакциясы
С) Na2S + HOH =NaHS+NaOH
D) AlCl3+HOH= AlOHCl2 +HCl
E)NH4Cl+ HOH= NH4OH+HCl
Газдарды еріткенде Гиббс энергясының (G), энтальпияның (Н) энторпияның (S) өзгеру белгісі
А) G<0
Е)S<0
F)H<0
Газ күйіндегі затты еріткенде Гиббс энергиясының 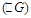 , энтальпияның
, энтальпияның 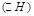 , энтропияның
, энтропияның 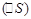 өзгеру белгісі:
өзгеру белгісі:
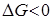
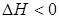
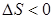
Гидролиз катион бойынша терең жүреді:
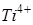
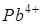
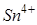
Гидролиз үрдісі:
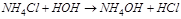
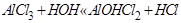
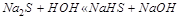
Гидролиз үрдісі күшейеді, егер:
гидролизденетін ионның заряды өссе.
гидролизденетін ионның радиусы кішірейсе.
гидролизденетін ионның жұмсақ қабаты болса.
Гидролиз үрдісі күшейеді, егер:
температура көтерілсе.
катион бойынша гидролизденетін тұзға сілті қосу.
ерітінді концентрациясын сұйылтса.
Гальваникалық элемент (ГЭ) үшін дұрыс жағдай:
анод – ГЭ теріс полюсі
катод –ГЭ оң полюсі
анодта тотығу үрдісі жүреді
Гальваникалық элементте Zn/Zn2+//Fe2+/Fe жүретін ТТР
Fe2+=Fe




