Напишите формулу мицеллы золя сульфата бария, полученного при взаимодействии раствора хлорида бария с небольшим избытком раствора сульфата натрия?
Решение:
В основе получения золя лежит реакция:
BaCl2 + Na2SО4 изб.= 2 NaCl + Ba SО4¯
Условием получения золя является избыток Na2SО4, который является стабилизатором золя.
В растворе будут присутствовать ионы натрия и сульфат-ионы, образующиеся при диссоциации сульфата натрия
Na2SO4 = 2Na+ + SO²⁻
На поверхности агрегатов будут адсорбироваться сульфат-ионы.
Образуетсяя ядро коллоидной частицы:
[(BaSO4)m∙nSO²⁻
Несущее отрицательный заряд ядро притягивает из раствора ионы противоположного знака, называемые противоионами. В нашем случае в роли противоионов выступают катионы натрия.
формула мицеллы полученного золя:
{[(BaSO4)m·nSO²⁻]2(n-x)Na+}2x-2xNa+
К какому электроду будут перемещаться частицы золя полученного при взаимодействии нитрата серебра с избытком хлорида натрия?
Решение. При смешивании растворов AgNO3 и NaCl изб. протекает реакция
 AgNO3+ NaСl (изб.) = AgСl + NaNO3.
AgNO3+ NaСl (изб.) = AgСl + NaNO3.
Ядро коллоидной частицы золя хлорида серебра состоит из агрегата молекул (mAgСl) и зарядообразующих ионов Cl ⁻, которые находятся в растворе в избытке и обеспечивают коллоидным частицам отрицательный заряд. Противоионами являются гидратированные ионы натрия.
Формула мицеллы хлорида серебра имеет вид:
[ m (AgCl) n Cl– (n– x)Na+] x – x Na+
Коллоидная частица имеет отрицательный заряд, значит будет перемещаться к положительно заряженному электроду - катоду.
Напишите формулы мицелл коллоидных растворов для следующих веществ:
а) кремниевый кислоты: агрегат m [Н2SiO3], ионный стабилизатор K2SiO3 ® 2K+ + SiO32–
б) гидрозоля золота: агрегат m [Аu], ионный стабилизатор NaAuO2 ® Na + + AuO2–
в) двуокиси олова: агрегат m [SnO2], ионный стабилизатор K2SnO3 ® 2K+ + SnO32–
Решение:
а) Образование золя кремневой кислоты происходит по реакции
K2SiO3 изб.+ 2HCl = H2SiO3 + 2KCl.
 K2SiO3 2K⁺+ SiO₃²⁻
K2SiO3 2K⁺+ SiO₃²⁻
На электронейтральном агрегате частиц (mH2SiO3) адсорбируются ионы элемента, входящего в состав ядра. Таковыми являются ионы HSiO3‾, которые образуются в результате гидролиза соли K2SiO3:
K2SiO3 + H2O 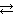 KHSiO3 + KOH или в ионной форме
KHSiO3 + KOH или в ионной форме
SiO32− + H2O 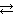 HSiO3‾ + OH‾.
HSiO3‾ + OH‾.
Ионы HSiO3‾, адсорбируясь на поверхности частиц золя кремниевой кислоты, сообщают им отрицательный заряд. Противоионами являются гидратированные ионы водорода H+. Формула мицеллы золя кремневой кислоты:
{[(m H2SiO3) · n HSiO3‾·(n-x)H+∙ y H2O] x − + x H+∙ z H2O}.
б) Образование гидрозоля золота происходит при действии восстановителя на соль золотой кислоты в слабощелочной среде:
2NaAuО2 + 3НСНО + Na2CO3 = 2Аu + ЗНСООNa + NaНСО3 + Н2О.
На агрегате частиц (mAu) адсорбируются ионы элемента, входящего в состав ядра. Таковыми являются ионы AuO2‾,
Формула мицеллы золя:
{m[Au]·nAuO²⁻·(n-x) Na⁺}x⁻·xNa⁺
в) Образование золя двуокиси олова происходит следующим образом:
 K2SnO3 2K⁺ + SnO3²⁻
K2SnO3 2K⁺ + SnO3²⁻
На электронейтральном агрегате частиц (mSnO2) адсорбируются ионы элемента, входящего в состав ядра. Таковыми являются ионы SnO32‾:
K2SnO3 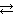 SnO32⁻ + 2K⁺
SnO32⁻ + 2K⁺
Ионы SnO32‾, адсорбируясь на поверхности частиц золя, сообщают им отрицательный заряд. Противоионами являются ионы K+. Формула мицеллы золя двуокиси олова:
{[(m SnO2) n SnO32‾·(2 n-x)K+] 2 − + x K+}.






