Пример 1
Расчет температуры замерзания раствора неэлектролита с известным количественным составом.
Вычислите температуру замерзания водного раствора рибозы с массовой долей 2 %.
Решение. Понижение температуры замерзания раствора по сравнению с чистым растворителем зависит от концентрации кинетически самостоятельных единиц. Предварительно рассчитаем моляльную концентрацию рибозы в растворе по формуле, приведенной в таблице:.
1000 ω 1000·0,02
сm (С5Н10О5) = ———————————— = —————— = 0,136 моль/кг
[1 - ω(С5Н10О5)M(С5Н10О5)] 1 – 0,05·150,1
Для расчета понижения температуры замерзания раствора рибозы воспользуемся выражением:
Δ Т зам = К(Н2О) с m(С5Н10О5)
Подставим в это выражение значения вычисленной моляльной концентрации рибозы и криоскопического коэффициента воды: K(H2O) = 1,86 К×кг/моль
ΔTзам = 1,86 К×кг/моль · 0,136 моль/кг = 0,253 К
Для расчета температуры замерзания раствора tзам используем выражение:
tзам = 0 °С - 0,253 °С = - 0,253 °С
Ответ: раствор замерзает при - 0,253 °С
Пример 2
Расчет осмотического давления раствора неэлектролита.
Установление изотоничности другому раствору
Вычислите осмотическое давление раствора глицерина с массовой долей 1% (плотность 1,0006 г/мл) при температуре 25 °С. Будет ли он изотоничен раствору с осмотическим давлением 500 кПа?
Решение. Осмотическое давление раствора глицерина рассчитывается по закону Вант-Гоффа:
р осм = с (глицерин)RT
Предварительно найдем молярную концентрацию этого раствора, воспользовавшись таблицей справочника:
l000wr
с = ———
М
Подставив это выражение в уравнение, получим:
1000wrRT
р осм = ¾¾¾¾¾
М
1000 мл/л × 0,01 × 1,0006 г/мл × 8,31 Дж/(моль×К) ×298 К
р осм = ¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾ = 268 кПа
92,1 г/моль
Ответ: 268 кПа; Поскольку осмотическое давление раствора глицерина меньше 500 кПа, он будет гипотоничен по отношению ко второму раствору.
Пример 3
Расчет молярной массы неэлектролита по криометрическим и эбулиометрическим данным.
Вычислите массу рибозы, которую следует растворить в 180 г воды, чтобы получить раствор, кипящий при 100,1 °С.
Решение. Найдем 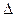 Т кип, исходя из выражения:
Т кип, исходя из выражения:
ΔТкип = tкип(раствор) - tкип(Н2О).
Преобразуем выражение относительно моляльной концентрации рибозы
с m(С5Н10О5) = D Т к/ Э(H2O)
Выразим количество вещества рибозы через моляльную концентрацию, а затем вычислим ее массу.
n(С5Н10О5) = с m(С5Н10О5)m(Н2О) = 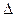 Ткип· m(Н2О) / Э(H2O)
Ткип· m(Н2О) / Э(H2O)
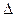 Т кип ·m(Н2О)·M(С5Н10О5)
Т кип ·m(Н2О)·M(С5Н10О5)
m(С5Н10О5) = ¾¾¾¾¾¾¾¾¾¾¾¾
Э(H2O)
Подставим известные величины в выражение массы растворенного вещества, предварительно найдя в справочнике значение эбулиоскопического коэффициента воды:
(100,1-100)К× 0,180 кг ×150,13 г/моль
m(С5Н10О5) = ¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾ = 5,19 г.
0,52 К·кг/моль
Ответ: нужно растворить 5,19 г рибозы.
Пример 4
Расчет ионной силы. Расчет активности ионов
В качестве плазмозамещающего раствора применяется раствор Рингера-Локка, имеющий пропись:
Натрия хлорид 0,9 г
Калия хлорид 0,02 г
Кальция хлорид 0,02 г
Натрия гидрокарбонат 0,02 г
Глюкоза 0,1г
Вода для инъекций до 100 мл.
Вычислите ионную силу этого раствора и активность иона натрия.
Решение. Рассчитаем молярные концентрации электролитов по формуле:
с (Х) = m(Х)/M(Х)V
с (NaCl) = 0,9г/(58,5 г/моль × 0,1л) = 0,154 моль/л
с (KCI) = 0,02г/ (74,5 г/моль ×0,1л) = 0,00268 моль/л
с (СаС12) = 0,02г/(111 г/моль ×0,1л) = 0,00180 моль/л
с (NaHCO3) = 0,02г/ (84г/моль ×0,1л) = 0,00238 моль/л
Глюкоза не является электролитом, поэтому не оказывает влияния на ионную силу раствора. Концентрации ионов калия, кальция и гидрокарбонат-ионов числено совпадают с концентрациями электролитов, в состав которых они входят. Суммарную молярную концентрацию хлорид-ионов найдем по выражению:
с (Cl-) = с (NaCl) + с (КС1) + 2 с (СаС12)
с сумм(Cl-) = 0,154 + 0,00268 + 2 0,00180 = 0,160 моль/л
Для суммарной концентрации иона натрия:
с (Na+) = с (NaCl) + с (NaHCO3)
с сумм(Na+) = 0,154 +0,00238 = 0,157 моль/л
Ионную силу раствора рассчитаем по формуле применительно к данной задаче:
I = 0,5 [ с (Na+) + с (K+) + с (Сa2+)× 22 + с (HCO3-) + с (Сl-)]
I = 0,5 (0,157 + 0,00268 + 0,00180 ×4 + 0,160 + 0,00238) = 0,165 моль/л
По значению ионной силы (табл.) найдем значение коэффициента активности [f(Na+) = 0,72], а затем вычислим активность иона натрия по формуле:
a(Na+) = f(Na+) с (Na+) = 0,72 ×0,156 = 0,112
Ответ: ионная сила равна 0,164 моль/л; активность иона натрия равна 0,112.
Пример 5
. Расчет изотонического коэффициента по данным криоскопических и эбулископических исследований
Раствор, приготовленный растворением 10,11 г нитрата калия в дистиллированной воде массой 246 г, кипит при 100,4 °C. Вычислите изотонический коэффициент нитрата калия в этом растворе.
Решение. Вычислим количество KNO3, находящегося в растворе:
n(KNO3) = m(KNO3) / M(KNO3),
Моляльная концентрация исследуемого раствора равна:
сm = n (KNO3) / m (Н2O)
Преобразовав выражение 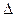 Тк = i Э(S) с (x), вычислим
Тк = i Э(S) с (x), вычислим
i = Δ Т кип / с Э(Н2O)
Конечное выражение имеет вид:
[tзам(раствор) - tзам(растворитель)] M(KNO3) m(H2О)
i = ¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾————————
m(KNO3) Э(H2О)
Подставим в него известные величины:
(100,4 - 100) К ×101,3 г/моль ×0,246 кг
i = ¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾ =1,90
10,11г× 0,52(К×кг)/моль
Ответ: i = 1,90
Пример 6
Расчет изотонического коэффициента по известному осмотическому давлению раствора электролита
Водный раствор хлорида магния с концентрацией 0,1 моль/л имеет при 298 К осмотическое давление 691 кПа. Вычислите изотонический коэффициент хлорида магния в этом растворе.
Решение. Преобразуя выражение р оcм = i с RT, вычислим:
i = р оcм / с RT
Подставим в полученное выражение известные величины:
691 кПа
i = ¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾ = 2,79
0,1 моль/л × 8,31 Дж/(моль·К)×298 К
Ответ: 2,79
Пример 7
Расчет осмолярности (осмоляльности) раствора
Рассчитайте верхнюю и нижнюю границу осмолярности растительных тканей степных растений. Осмотическое давление в них принимает значения от 810 кПа до 4052 кПа. Температуру принять равной 25°С.
Решение. Преобразуя выражение
р осм = i с RT, вычислим:
с осм = i с = р осм / RT
Подставим в полученное выражение известные величины:
810 кПа
с осм = ¾¾¾¾¾¾¾¾¾¾ = 0,327 осмоль/л
8,31 (л ×кПа)/(моль× К) × 298К
Подстановка в аналогичное выражение р осм = 4052 кПа дает результат с осм = 1,64 осмоль/л.
Ответ: осмолярность тканей степных растений находится в диапазоне от 0,327 осмоль/л до 1,64 осмоль/л.
Лабораторная работа.






