ЛФ, ФИУ, ПФ. Занятие № 13
А. Основные положения
Антиген: определение.
Молекула (вещество), распознаваемое иммунной системой в контексте «свой/чужой».
Антиген: принцип строения.
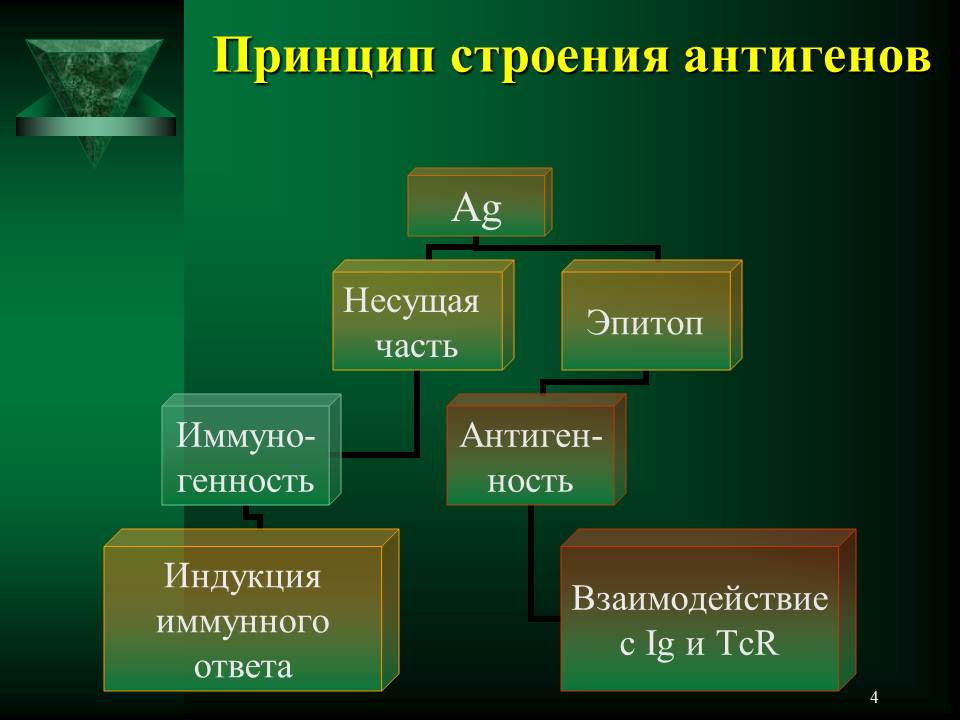
Антиген состоит из несущей части, обуславливающей индукцию антигеном иммунного ответа (т.е. иммуногенность антигена) и эпитопов, обуславливающих взаимодействие антигена с иммуноглобулинами и антигенраспознающими рецепторами лимфоцитов (т.е. антигенность антигена).
Эпитоп и его количественный состав.
Участок молекулы антигена специфического состава и конфигурации, содержит 5-6 аминокислотных (для белков) или липополисахаридных (для липополисахаридов) остатков.
Валентность антигена.
Количество идентичных эпитопов в его составе.
Факторы, определяющие степень иммуногенности антигена.
Степень иммуногенности антигена определяют следующие факторы: физико-химические свойства антигена, динамико поступления антигена в макроорганизм и катаболизм его во внутренней среде макроорганизма, состояние макроорганизма в момент контакта с антигеном, введение антигена в комплексе с адъювантом.
Физико-химические свойства антигена, влияющие на его иммуногенность.
Степень иммуногенности антигена зависит от его чужеродности, химической природы, химического состава, молекулярной массы, пространственной организации, для растворимых антигенов – растворимости.
Динамика поступления и катаболизма антигенов, влияющие на его иммуногенность.
Степень иммуногенности антигена зависит от способа его введения в макроорганизм, количества введённого антигена, дробности его введения, чувствительности антигена к катаболическому разрушению.
Зависимость иммуногенности антигенов от состояния макроорганизма.
Высота иммунного ответа конкретного макроорганизма на конкретный антиген зависит как от генотипа данного макроорганизма, так и от его функционального состояния в момент контакта с данным антигеном.
Адъюванты.
Вещества, неспецифически усиливающие иммуногенность антигена.
Классификации антигенов.
Антигены классифицируются по происхождению (экзогенные и эндогенные), по природе (белковые и небелковые), по структуре (глобулярные и фибриллярные), по необходимости участия в иммунном ответе Т-хелперов (Т-зависимые и Т-независимые), по иммуногенности (иммуногены и гаптены), по степени чужеродности.
Аутоантигены.
Антигены собственного организма, в норме к ним не развивается иммунный ответ (состояние иммунологической толерантности), кроме забарьерных антигенов, иммунный ответ к которым не развивается вследствие недоступности их для контакта с иммунной системой.
Антигенпредставляющие молекулы: общая характеристика.
Это те молекулы на поверхности иммунокомпетентных клеток, в комплексе с которыми лимфоциты распознают чужеродный антиген в контексте «свой/чужой»: молекулы (антигены) МНС – для пептидных антигенов и молекулы (антигены) CD1 – полисахаридных и пептидных антигенов; так как основную роль в индукции иммунного ответа играют пептидные антигены (как наиболее иммуногенные), то основными антигенпредставляющими молекулами являются антигены МНС (антигены главного комплекса гистосовместимости).
Антигены главного комплекса гистосовместимости: общее понятие.
Представляют собой мембранные гликопротеины, представленные двумя классами: MHC-I и MHC-II.
МНС-I.
Экспрессированны на всех ядросодержащих клетках, состоят из двух полипептидных цепей, одна из которых (тяжёлая) «заякоревается» в цитоплазматической мембране антигенпредставляющей клетки, имея цитоплазматический участок, и формирует углубление, куда помещается процессированный антиген, вторая полипептидная цепь (лёгкая), ковалентно связанная с первой, не имеет цитоплазматического участка; используются для представления антигена CD8-лимфоцитам.
MHC-II.
Экспрессированны на профессиональных антигенпредставляющих (для Т-хелперах) клетках (макрофагах, дендритных клетках, В-лимфоцитах) и клетках эндотелия сосудов; представляют собой две одинаковые полипептидные цепи, «заякоренные» в цитоплазматической мембране и имеющие цитоплазматический фрагмент, углубление для процессированного антигена формируется между этих двух цепей; используются для представления антигена CD4-лимфоцитам.
Антигенпредставляющие молекулы CD1.
Мембранные гликопротеины, по структуре схожие с МНС-I, экспрессированны на многих лимфоидных и не лимфоидных клетках.
Суперантигены.
Антигены, вызывающие неспецифическую активацию и пролиферацию Т-лимфоцитов без процессинга в антигенпрезентирующих клетках.
Антигены бактерий: классификации по специфичности и по природе (происхождению).
Антигены бактерий классифицируются по специфичности (групповые – общие у нескольких видов, видовые – общие для одного вида, типовые – общие для одного серовара) и по природе (продукты распада – принадлежащие клеточным структурам бактериальной клетки, продукты жизнедеятельности бактериальной клетки).
Антигены, входящие в состав органелл бактериальной клетки.
В состав клеточных структур бактериальной клетки входят, например, следующие антигены: O-Ag (антиген клеточной стенки), К-Ag и Vi-Ag (антигены капсулы), Н-Ag (антиген жгутиков).
Антигены, продуцируемые микробной клеткой в процессе своего метаболизма.
К ним относятся белковые токсины, ферменты (в том числе – ферменты вирулентности).
Антигенные свойства грибов.
Антигенный состав грибов крайне гетерогенен, грибная клетка содержит многие десятки и даже сотни антигенов.
Основные этапы клеточного иммунного ответа.
Основные этапы клеточного иммунного ответа следующие: взаимодействие с антигеном антигенпрезентирующей клетки, процессинг в ней антигена, презентация процессированного антигена CD4-лимфоциту, активация Т-хелпера первого типа и синтез им активационных цитокинов (прежде всего – ИЛ-2), активация ИЛ-2 соответствующего клона Т-киллера и лейкоцитов воспалительной реакции, эффекторное звено (уничтожение чужеродного антигена Т-киллерами и в ходе иммунного воспаления), в случае элиминации чужеродного антигена – завершающие процессы (супрессия иммунного ответа и появление клеток иммунологической памяти).
Процессинг антигена.
Этим термином обозначаются те изменения, которые происходят с антигеном внутри антигенпрезентирующей клетки: поглощение антигена, его частичная деградация с вычленением эпитопов, соединение каждого вычлененного эпитопа с молекулой МНС (так называемый процессированный антиген).
Презентация антигена.
Этим термином обозначается вывод комплекса [эпитоп + МНС] (так называемого презентированного антигена) на внешнюю мембрану антигенпрезентирующей клетки.
Механизмы действия ЦТЛ (Т-киллеров).
Цитотоксические лимфоциты осуществляют внеклеточную цитотоксичность, синтезируя перфорины, которые, вызывая множественные дефекты наружной мембраны, вызывают лизис клетки-мишени; кроме того, ЦТЛ активируют в клетке-мишени процесс апоптоза.
Реакция агглютинации: основные термины.
Антиген, участвующий в реакции агглютинации, называется агглютиноген, антитело – агглютинин, образующийся в результате реакции агглютинации иммунный комплекс (т.е. комплекс антиген-антитело) – агглютинат.
Условия осуществления реакции агглютинации.
Для осуществления реакции агглютинации необходимо, чтобы антиген, в ней участвующий, был не менее, чем четырёхвалентным, а иммуноглобулин – не менее, чем двухвалентным.
Этапы (стадии) реакции агглютинации.
Реакция агглютинации протекает в два этапа (две стадии): сначала происходит формирования решётки (каркаса), в узлах которой располагаются антигены, а антитела играют роль «прутьев» этой решётки, связывая антигены друг с другом (эта стадия – невидимая), затем решётка выпадает в осадок (реакция становится видимой).
Внешние проявления реакции агглютинации.
Осадок-агглютинат может состоять из мелких частиц (иногда настолько мелких, что их можно увидеть только в микроскоп – в этом случае речь идёт о реакции микроагглютинации), а может формироваться в виде крупных хлопьев, как это бывает, например, при агглютинации жгутиконосных бактерий; в первом случае говорят о мелкодисперсной агглютинации, во втором – о крупнохлопчатой.
Способы постановки реакции агглютинации.
Реакцию агглютинации можно ставить на стекле (пластинчатая реакция агглютинации) – такая реакция чаще используется для идентификации антигена; реакция агглютинации, которую ставят в пробирке, носит название объёмной, или развернутой, агглютинации – она используется для обнаружения антител и определения их количество (титра).
Принципы осуществления реакции агглютинации.
Если агглютиноген непосредственно связывается с агглютинином, то такая реакция называется прямой реакцией агглютинации; но в ряде случаев образующийся при этом агглютинат не виден – чтобы его визуализировать, ставят непрямую реакцию агглютинации: или агглютинин или агглютиноген ассоциируют с частицами, склеивание которых сопровождается видимым эффектом (в качестве таких частиц используют эритроциты – реакция непрямой гемагглютинации, частицы латекса – латекс-агглютинация, клетки стафилококка – коагглютинация).
Внешние проявления РНГА.
Реакцию непрямой гемагглютинации ставят в иммунологических планшетах: в положительном случае эритроциты связываются друг с другом посредством формирования иммунного комплекса и оседают пластами, формирую рыхлый осадок с неровными краями по всему дну лунки (осадок в виде «розетки»); если иммунный комплекс не образуется, эритроциты оседают монетными столбиками, формируя в середине дна лунки компактный осадок с ровными краями (осадок в виде «пуговки»).
Б. Лекционный курс

























































В. Теоретический материал
35. Антигены
35.1. Основные свойства антигенов
35.2. Принцип строения молекулы антигена
35.3. Факторы, определяющие степень иммуногенности антигена
35.4. Классификации антигенов
35.5. Суперантигены
35.6. Аутоантигены
35.7. Антигены бактерий
35.8. Антигенные свойства грибов
36. Антигенпредставлющие молекулы
36.1. МНС
36.2. CD1
37. Клеточный иммунный ответ
37.1. Основные этапы клеточного иммунного ответа (перечисление)
37.2. Процессинг антигена
37.3. Презентация процессированного антигена
37.4. Активация Т-хелпера первого типа
37.5. Действие активационных цитокинов
37.6. Эффекторное звено клеточного иммунного ответа
37.7. Завершающие процессы эффективного клеточного иммунного ответа
АНТИГЕНЫ
35.1. Основные свойства антигенов
Антигеном называется молекула (вещество), распознаваемое иммунной системой в контексте свой/чужой. Ниже буду рассмотрены механизмы этого распознавания. Так как иммунная система относится подобным образом ко всем веществам, антигеном может быть любое вещество. Встречающееся в литературе определение антигена как «молекула или вещество, способное вызывать иммунный ответ и реагировать с его продуктами», на первый взгляд, более понятно, но – как будет показано ниже – менее корректно, так как существуют антигены (называемые гаптенами), которые не способны сами по себе вызывать иммунный ответ. Тем не менее, вторая часть этого определения «… реагировать с его продуктами» указывает на неотъемлемое свойство любого антигена. Вообще, основных свойств у антигенов два: антигенность и иммуногенность.
А. Под антигенностью понимают способность антигена специфически реагировать с антителами или клетками, которые продуцируются на его введение в организм (человека или животного). Это свойство, как только что было указано, неотъемлемое, т.е. если антиген не обладает свойством антигенности, то он, строго говоря, не может быть рассматриваем как антиген.
Б. Под иммуногенностью понимают способность антигенов индуцировать специфический иммунный ответ, в результате чего продуцируются антитела или активируются иммунные лимфоциты. Это свойство, в отличие от антигенности, не присуще всем без исключения антигенам.
1. Антигены, обладающие свойством иммуногенности, называются иммуногенами.
2. Антигены, не обладающие свойством иммуногенности, называются гаптенами.
3. Существуют вещества, неспецифически усиливающие иммуногенность антигенов. Такие вещества называются адъювантами.
а. Механизм такого действия адъювантов, в частности, заключается в создании «депо антигена» (т.е адъювант связывает антиген, и эта связь постепенно разрушается, обеспечивая постепенное высвобождение антигена). В результате обеспечивается длительная антигенная стимуляция. Другими словами, антиген реагирует с иммунной системой не всей дозой сразу, а дробно – небольшими дозами. Такой способ введения антигена способствует развитию более сильного иммунного ответа.
б. Кроме этого, к эффектам действия адъювантов относятся стимуляция ими фагоцитоза и их митогенное действие на иммунокомпетентные клетки.
в. В качестве примеров адъювантов можно привести:
– адъювант Фрейнда (смесь вазелиновых масел с инактивированными микобактериями в полном адъюванте Фрейнда или без последних в неполном адъюванте Фрейнда);
– гидроокись алюминия (алюминиевые квасцы);
– мурамил-дипептиды и мурамил-трипептиды (синтетические аналоги компонентов бактериальных клеток).
35.2. Принцип строения молекулы антигена
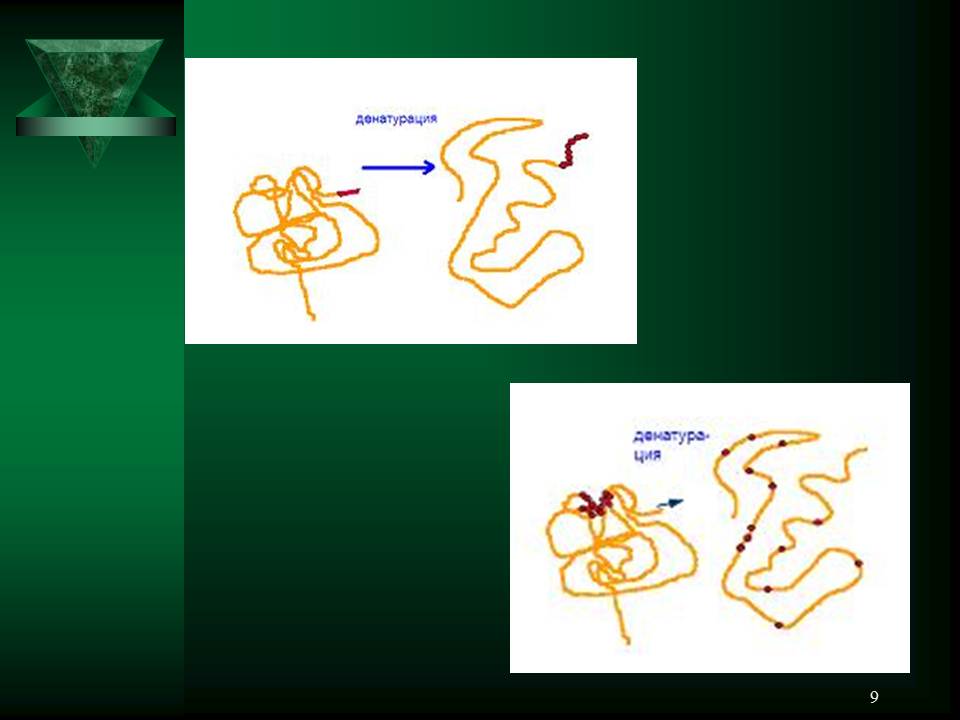
Все антигены, несмотря на их огромное разнообразие, имеют общий принцип строения (Рис. 35.2-1). Основная часть молекулы антигена – несущая часть – определяет его иммуногенность. Антигенность же обуславливает участок молекулы антигена специфического состава и конфигурации (Рис. 35.2-2), называемый эпитопом (в качестве синонимов используются также термины «антигенная детерминанта», «детерминантная группа антигена»).

| 
|
| Рис. 35.2-1. Принцип строения антигена | Рис. 35.2-2. Схематическое расположение эпитопов на поверхности несущей части антигена |
А. Количество идентичных эпитопов, содержащихся молекулой антигена, определяет его валентность. Например, на рис. 35.2.-2 антиген двухвалентен по всем пяти эпитопам.
Б. Эпитоп формируется, как правило, 5-6 аминокислотными остатками (у белков) или 5-6 липополисахаридными остатками (у липополисахаридов).
В. В зависимости от расположения в молекуле антигена (например, белка) эпитопы классифицируются на три группы.
1. Линейные (секвенциальные) эпитопы формируются первичной аминокислотной последовательностью белковой молекулы. Такие эпитопы взаимодействуют как с Т-, так и с В-лимфоцитами.
2. Поверхностные (конформационные) эпитопы образуются в результате вторичной, третичной или четвертичной конформации молекулы белка. Такие эпитопы реагируют с В-лимфоцитами.
3. Глубинные (скрытые) эпитопы проявляются при разрушении биополимера. Такие эпитопы реагируют с Т-лимфоцитами.
35.3. Факторы, определяющие степень иммуногенности антигена
Степень иммуногенности антигена определяется многочисленными факторами, которые условно можно классифицировать (кроме уже упомянутого выше введения антигена в комплексе в адъювантом) на три группы.
А. Физико-химические свойства антигена.
1. Чем выше чужеродность антигена для макроорганизма, тем выше его иммуногенность. Впрочем это правило не абсолютно и здесь уместно будет упомянуть о двух исключениях из него.
а. Перекрестно реагирующие антигены микроба могут спровоцировать иммунный ответ на собственные антигены макроорганизма, в норме лишенные иммуногенности.
б. Уход микробов с помощью антигенной мимикрии от распознавания иммунной системой может значительно снизить иммуногенность их антигенов.
2. Иммуногенность зависит от биохимической природы антигена. Наибольшая иммуногенность присуща белкам.
3. Влияет на иммуногенность и химический состав антигена. Иммуногенность белков усиливают:
– ароматические аминокислоты,
– левовращающие изомеры,
– разнообразие аминокислотного состава.
4. Чем выше молекулярная масса антигена, тем, как правило, выше и его иммуногенность.
5. Структура антигена так же влияет на его иммуногенность – у агрегированных она выше, чем у растворимых.
6. У растворимых антигенов их растворимость прямо пропорциональна иммуногенности.
Б. Динамика поступления антигена в макроорганизм и катаболизм его во внутренней среде макроорганизма.
1. Влияние способа введения на иммуногенность может быть разной у разных антигенов, но, в целом, наибольшая иммуногенность проявляется при парентеральном введении антигена.
2. Чем больше количество введенного антигена, тем выше его иммуногенность. Правда, до определенного предела, превышение которого может свести иммуногенность данного антигена до нуля (разовьется состояние, которое называется иммунологическая толерантность большой дозы; о нем будет сказано ниже).
3. Важной значение имеет дробность введения антигена. Так, неоднократное введение малых доз вызывает более сильный иммунный ответ, чем однократное введение большой дозы.
4. И, наконец, чем выше чувствительность антигена к катаболическому разрушению, тем выше его иммуногенность.
В. Состояние макроорганизма в момент контакта с антигеном.
1. Особенности реагирования макроорганизма на конкретный антиген, в том числе и высота иммунного ответа на него, зависит от генотипа этого макроорганизма.
2. Влияет на силу иммунного ответа на антиген и функциональное состояние макроорганизма.
35.4. Классификации антигенов
Классифицируют антигены в зависимости от их происхождения, химической природы, пространственной структуры, необходимости участия в иммунном ответе на них Т-лимфоцитов, по иммуногенности и по степени чужеродности для макроорганизма.
А. По своему происхождению антигены подразделяются на две группы.
1. Экзогенные антигены поступают в макроорганизм извне.
2. Эндогенные антигены принадлежат собственным тканям макроорганизма или образуются внутри его.
Б. По химической природе антигены также подразделяются на две группы.
1. Антигены белкового происхождения, как было упомянуто, вызывают наиболее сильный иммунный ответ.
2. Все остальные антигены входят в группу небелковых антигенов.
В. На две группы антигены классифицируются и по пространственной структуре своей молекулы.
1. Группу глобулярных антигенов составляют те из них, чья молекула имеет шарообразную структуру.
2. Те антигены, чьи молекулы имеют нитевидную структуру, составляют группу фибриллярных антигенов.
Г. По необходимости участия в иммунном ответе Т-лимфоцитов (точнее, Т-хелперов) антигены подразделяются тоже на две группы.
1. Подавляющее большинство антигенов относится к Т-зависимым. Это значит, что в иммунном ответе на эти антигены обязательно задействованы Т-хелперы.
2. В иммунном ответе на Т-независимые антигены Т-хелперы не участвуют. К таким антигенам относятся, например, бактериальные антигены простого строения, состоящие из монотонно повторяющихся последовательностей, с многочисленными однотипными эпитопами.
Д. По иммуногенности (точнее, по наличию этого свойства) антигены классифицируются, как уже было изложено в разделе 35.1 на иммуногены и гаптены.
Е. По степени чужеродности (прежде всего, в трансплантологии) антигены классифицируются на четыре группы.
1. Ксеногенные антигены – общие для организмов различных видов и родов. Такие антигены называются также ксеноантигенами, гетерологичными антигенами, «антигенами Форсмана».
2. Аллогенные антигены – общие для организмов одного вида. Такие антигены называются еще групповыми.
3. Изоантигены – общие для генетически идентичных организмов (например, однояйцовых близнецов). Такие антигены называются еще индивидуальными.
4. Органо- и тканеспецифические антигены – изоантигены, характерные для определенных анатомо-морфологических образований данного макроорганизма.
35.5. Суперантигены
Отдельную группу составляют суперантигены.
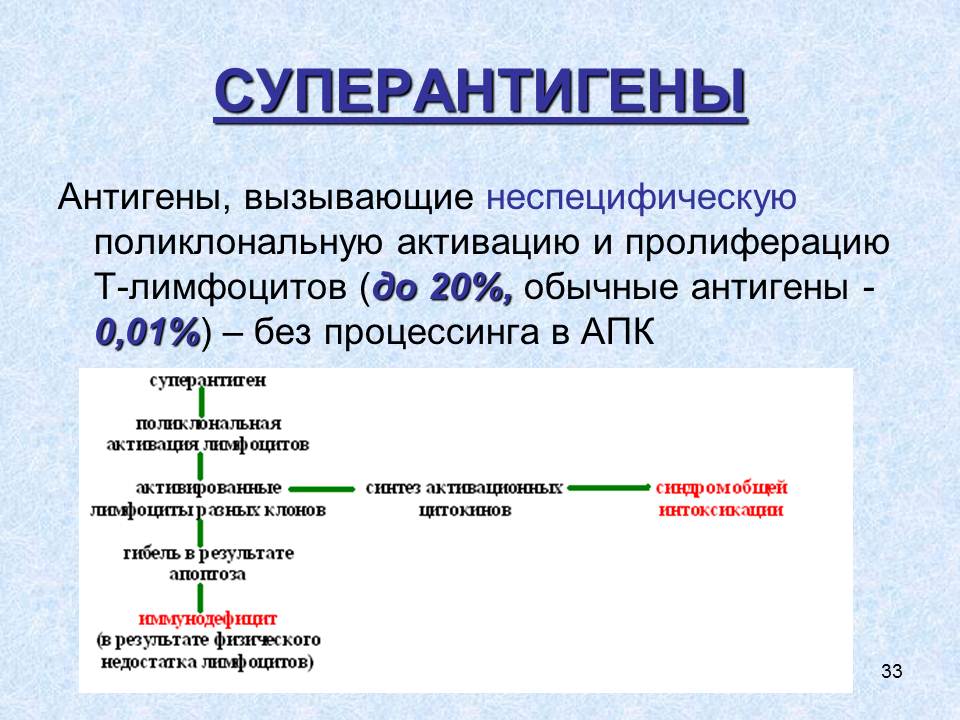
А. Так называются антигены, вызывающие неспецифическую поликлональную активацию и пролиферацию Т-лимфоцитов. Если обычный антиген вызывает активацию и полиферацию лишь «своего» и близких к нему клонов Т-лимфоцитов (примерно 0,01% общего пула этих клеток), то суперантигены активируют до 20% Т-лимфоцитов макроорганизма, причем – без процессинга в антигенпрезентирующих клетках.
Б. Механизм такого действия суперантигенов иллюстрируется рисунком 35.5-1.

| |
| Рис. 35.5-1. Взаимодействие Т-лимфоцита с антигенпрезентирующей клеткой. | |
| Слева: взаимодействие с участием обычного, процессированного, антигена, происходящее лишь в том случае, когда последний совпадает по специфичности с соответствующими рецепторами антигенпрезентирующей клетки и Т-лимфоцита. | Справа: взаимодействие с участием суперантигена, неспецифически связующего рецепторы обеих клеток. |
1. В результате активированные многочисленные клоны Т-лимфоцитов продуцируют огромное количество активационных цитокинов, что может привести к развитию синдрома общей интоксикации.
2. С другой стороны, активированные Т-лимфоцитов имеют ограниченный срок жизни и быстро погибают, что может привести к развитию иммунодефицита вследствие физического недостатка этих клеток.
В. Суперантигены чаще всего – микробного происхождения.
1. К суперантигенам бактериального происхождения относятся, например (наряду с другими антигенами бактериальной клетки):
– энтеротоксины стафилококков,
– токсин синдрома токсического шока некоторых кокков.
2. Суперантигены могут входить и в состав вирусов. Среди прочих вирусов ими обладают, например:
– вирус иммунодефицита человека,
– вирус бешенства,
– ротавирусы.
35.6. Аутоантигены
Аутоантигенами, или аутогенными антигенами, называются антигены собственного макрорганизма.
А. В норме к аутоантигенами иммунный ответ не развивается.
Б. Неиммуногенность аутоантигенов обусловлена двумя основными причинами:
– отсутствием иммунокомпетентных клеток с соответствующими антиген-распознающими рецепторами (явление естественной иммунологической толерантности, о котором будет сказано в разделе 42),
– недоступность аутоантигенов ряда органов и тканей для контакта с иммунной системой (так называемые забарьерные антигены).
35.7. Антигены бактерий
Бактериальная клетка имеет большое количество антигенов, которые можно классифицировать по их специфичности и по их природе.
А. По специфичности бактериальные антигены классифицируются на три группы.
1. К групповым антигенам относятся антигены, общие для нескольких видов бактерий.
2. Видовые антигены общие для всех особей данного вида.
3. Антигены, по которым различаются различные серовары (серотипы) одного вида, называются типовыми.
Б. По своей природе антигены бактериальной клетки можно классифицировать на две большие группы.
1. К первой группе относятся антигены, входящие в состав различных органелл бактериальной клетки. Так как в чистом виде такие антигены можно получить лишь в результате лизиса клетки, их можно определить как продукты распада бактериальной клетки.
а. Основной антиген клеточной стенки бактерий носит название О-антигена.
1. У грамположительных бактерий его специфичность определяют тейхоевые кислоты.
2. У грамотрицательных бактерий его специфичность определяет липополисахарид наружной мембраны (точнее, боковые полисахаридные цепочки его молекулы).
б. Ряд антигенов входят в состав капсулы, в том числе микрокапсулы. В ряде случаев к этой группе могут относится поверхностные антигены клеточной стенки.
1. Основной капсульный антиген носит название К-антигена.
2. У некоторых бактерий имеются особые капсульные антигены, так называемые Vi-антигены, наличие которых может коррелировать с уровнем вирулентности.
в. Антиген жгутиков (а именно – белок флагеллин) называется Н-антигеном.
г. В состав бактериальной клетки входят и другие антигены (рибосомальные и т.п.)
2. Ко второй группе относятся антигены, продуцируемые бактериальной клеткой в процессе метаболизма (т.е. продукты ее жизнедеятельности).
а. К этой группе бактериальных антигенов относятся белковые токсины.
б. Ферменты, продуцируемые бактериальной клеткой (прежде всего – экзоферменты) также являются бактериальными антигенами.
в. Особую группу антигенов бактериальной клетки составляют протективные антигены. Это нетоксичные для макроорганизма белки, продуцируемые некоторыми бактериями на специальных питательных средах, являющиеся сильными иммуногенами. Термин «протективный антиген» используется также для обозначения такого микробного антигена, иммунный ответ против которого предотвращает заболевание, вызываемое данным микроорганизмом. Наиболее эффективные вакцины готовятся на основе именно протективных антигенов.
35.8. Антигенные свойства грибов
Антигенный состав грибов отличается крайней гетерогенностью. Так, например, у основного возбудителя кандидоза – Candida albicans – насчитывается 78 различных антигенов.
А. Часть антигенов грибов входит в состав их клеточной стенки.
Б. Часть – содержится в цитоплазме микотической клетки.
АНТИГЕНПРЕДСТАВЛЯЮЩИЕ МОЛЕКУЛЫ
36.1. МНС
Молекулы МНС (от английских слов major histocompatibility complex – главный комплекс гистосовместимости) является основными антигенпредставляющими молекулами. Именно они представляют для Т-лимфоцитов пептидные антигены, которые играют ведущую роль в индукции иммунного ответа. При этом Т-лимфоциты распознают именно комплекс [антиген + молекула МНС]. У человека они были первоначально открыты на лейкоцитах, поэтому получили название молекул (или антигенов) HLA (human leucocyte antigen). В «чистом виде» МНС на поверхности антигенпредставляющих клеток (АПК) не экспрессируются – если не с чужим, то они комплексируются с аутоантигеном. Молекулы МНС являются мембранными гликопротеинами и представлены двумя классами.
А. Молекулы МНС первого класса обычно обозначаются как МНС-I.
1. МНС-I экспрессируются на всех ядросодержащих клетках (т.е. их нет лишь на эритроцитах). В наибольшем количестве они присутствуют на лимфоцитах и лейкоцитах.
2. МНС первого класса связываются с антигенами цитозоля и внутриядерного содержимого АПК.
а. Поэтому МНС-I презентируют (представляют) Т-лимфоцитам прежде всего вирусные антигены.
б. Кроме этого МНС-I презентируют (представляют) Т-лимфоцитам антигены бактерий, способных к внутриклеточному паразитированию.
3. МНС первого класса выполняют две основные функции
а. Во первых, МНС-I представляют антиген CD8-лимфоцитам.
б. Кроме антигенпредставляющей функции, МНС-I играют важную роль в регуляции активности NK-клеток.
1. МНС-I тормозят цитотоксическую активность NK-клеток, поэтому если они присутствуют на клетке в достаточном количестве, то такую клетку естественные киллеры «не трогают».
2. На опухолевых клетках и клетках, пораженных вирусами, экспрессия МНС-I резко снижается. И NK-клетки их убивают.
4. Строение молекулы МНС-I иллюстрирует Рис. 36.1-1.

Рис. 36.1-1. Строение молекулы МНС-I.
а. Как и все молекулы иммуноглобулинового суперсемейства (см. раздел 31) МНС-I состоит из двух полипептидных цепей.
1. Тяжелая полипептидная цепь обозначается как α-цепь, она проникает сквозь цитоплазматическую мембрану АПК, «заякореваясь» в ее цитоплазме.
2. Легкая цепь, обозначаемая как β2-микроголоблин, имеет значительно меньший размер и не имеет цитоплазматического участка.
б. Тяжелая цепь формирует углубление (клефт) в которое помещается 8-10 аминокислотных остатков презентируемого антигена.
Б. Молекулы МНС второго класса обычно обозначаются как МНС-II.
1. МНС-II экспрессированы, в отличие от МНС первого класса, лишь на некоторых клетках.
а. Во первых, они экспрессируются на профессиональных антигенпредставляющих клетках, а именно:
– на макрофагах/моноцитах,
– дендритных клетках,
– В-лимфоцитах.
б. Во-вторых, МНС-II экспрессируются на клетках эндотелия сосудов.
2. МНС второго класса связываются с антигенами мембранных структур клетки (т.е. той зоны клетки, которая непосредственно сообщается с внешней средой).
а. Поэтому МНС-II презентируют (представляют) Т-лимфоцитам антигены возбудителей внеклеточных инфекций.
б. Кроме этого МНС-II презентируют (представляют) Т-лимфоцитам антигены возбудителей так называемых везикулярных инфекций, которые находятся в клетке внутри везикул, а не непосредственно в цитоплазме (например, хламидий).
3. МНС второго класса представляют антиген CD4-лимфоцитам.
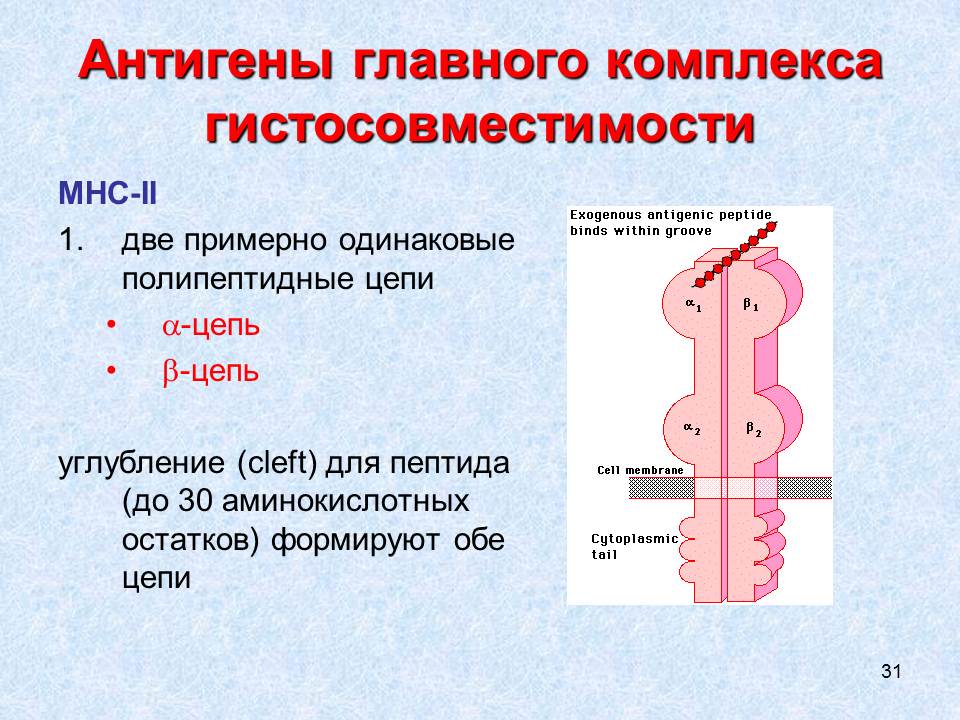
4. Строение молекулы МНС-II иллюстрирует Рис. 36.1-2.

Рис. 36.1-2. Строение молекулы МНС-II.
а. Как и все молекулы иммуноглобулинового суперсемейства (см. раздел 31) МНС-II состоит из двух полипептидных цепей. В отличие от молекул МНС-I, эти цепи – α- и β- – примерно одинаковые и обе проникают сквозь цитоплазматическую мембрану АПК, «заякореваясь» в ее цитоплазме.
б. Углубление (клефт), в которое (также в отличие от МНС-I) помещается до 30 аминокислотных остатков, формируется не одной, а обеими цепями.
36.1. CD1
Молекулы CD1 представляют для Т-лимфоцитов липидные и полисахаридные антигены. И в этом случае Т-лимфоциты также распознают именно комплекс [антиген + молекула CD1].
А. Представляют собой мембранные гликопротеины, схожие по структуре с MHC-I.
1. У человека молекулы CD1 представлены пятью изоформами.
2. Углубление (клефт) в молекуле CD1 уже и глубже, чем у MHC-I и имеет большое химическое сродство к гидрофобным лигандам.
Б. Полный список клеток, на которых экспрессируются молекулы CD1 еще не определен. Эти антигенпредставляющие молекулы обнаружены, например, на:
– дендритных клетках,
– клетках Лангерганса,
– кортикальных тимоцитах,
– В-лимфоцитах,
– других нелимфоидных клетках.
КЛЕТОЧНЫЙ ИММУННЫЙ ОТВЕТ
37.1. Основные этапы клеточного иммунного ответа
При клеточном иммунном ответе деструкцию и элиминацию причинного антигена осуществляют цитотоксические лимфоциты (ЦТЛ) и активированные иммунной системой («нанятые» ею) лейкоциты воспалительной реакции. Основные этапы клеточного иммунного ответа следующие (в кратком виде они приведены на рис. 37.1-1):
– взаимодействие с антигеном антигенпрезентирующей клетки (АПК), чаще – дендритной клетки или макрофага,
– процессинг антигена в АПК,
– презентация процессированного антигена антигенпрезентирующей клеткой Т-хелперу (CD4-клетке),
– активация Т-хелперов первого типа и синтез ими активационных цитокинов (ИЛ-2 и др.),
– действие активационных цитокинов, проявляющаяся в активации и пролиферации соответствующего клона Т-киллера, а также в активации («нанимании») лейкоцитов воспалительной реакции,
– эффекторное звено клеточного иммунного ответа – уничтожение клеток, несущих комплекс [чужеродный пептид + МНС-I] ЦТЛ (Т-киллерами), а также развитие иммунного воспаления, осуществляемое «нанятыми» лейкоцитами,
– завершающие процессы (в случае успешной деструкции и элиминации причинного антигена, т.е. эффективного иммунного ответа) – супрессия иммунного ответа вследствие гибели активированных клеток, а также ингибиции их активности, и появление клеток иммунологической памяти (долгоживущих и не до конца дифференцированных Т-лимфоцитов).

Рис. 37.1-1. Общая схема клеточного иммунного ответа
37.2. Процессинг антигена
Этим термином обозначаются те изменения, которые происходят с антигеном внутри антигенпрезентирующей клетки (Рис 37.2-1).

Рис. 37.2-1. Процессинг и презентация антигена
А. Процессинг начинается с поглощения антигена антигенпрезентирующей клеткой.
Б. Затем происходит частичная деградация антигена с вычленением эпитопов.
В. После этого в цитоплазме АПК каждый вычлененный эпитоп соединяется с молекулой МНС и образуется «процессированный антиген» – так называется комплекс [эпитоп + МНС].
37.3. Презентация процессированного антигена
Вывод комплекса [эпитоп + МНС] на поверхностную мембрану антигенпрезентирующей клетки называется презентацией антигена, а сам этот комплекс обозначается как презентированный антиген (Рис. 37.3-1).
А. Комплекс [эпитоп + МНС-II] презентируется Т-хелперам (CD4-лимфоцитам).
Б. Комплекс [эпитоп + МНС-I] презентируется Т-киллерам (CD8-лимфоцитам).

Рис. 37.3-1. Взаимодействие рецепторных и корецепторных молекул при презентации АПК процессированного антигена Т-киллеру (слева) и Т-хелперу (справа).
37.4. Активация Т-хелпера первого типа
Дивергенция иммунного ответа, т.е. выбор пути его преимущественного осуществления –клеточного или гуморального, осуществляется посредством выбора соответствующего типа Т-хелпера, активируемого антигенпрезентирующей клеткой. Точнее, выбора того пути активации, который будет избран для неактивного Т-хелпера (так называемого «нулевого Т-хелпера» – Th0). В случае клеточного иммунного ответа нулевой Т-хелпер активируется и дифференцируется в Т-хелпер первого типа (Th1), а в случае гуморального иммунного ответа – в Т-хелпер второго типа (Th2). При этом алгоритм активации Т-хелперов обоего типа практически идентичен, разница заключается лишь в конкретном наборе цитокинов, продуцируемых активированным Т-хелпером и, соответственно, в тех дальнейших событиях, которые этими цитокинами обуславливаются. Поэтому разбираемый ниже процесс активации Т-хелпера первого типа можно рассматривать и как алгоритм активации Т-хелпера второго типа, о котором пойдет речь в разделе 38.
А. Процесс активации Т-хелпера начинается с получения им информационных сигналов от антигенпрезентирующей клетки.
1. Первый информационный сигнал обусловлен контактом при полном соответствии TcR Т-хелпера с презентированным антигеном на поверхности АПК.
2. Второй и последующие информационные сигналы обусловлены корецепторными взаимодействиями Т-хелпера с АПК (включая действие на Т-хелпер синтезируемого макрофагом интерлейкина-1).
Б. Эти информационные сигналы инициируют внутри Т-хелпера определенные биохимические реакции.
В. Продукты этих биохимических реакций активируют транскрипцию определенных генов.
Г. Белки, синтез которых детерминируется этими генами, обуславливают пролиферацию клона Т-хелпера (происходит так называемая экспансия клона).
Д. Практически параллельно начинаются процессы додиференцировки Т-хелперов.
1. Во-первых, синтезируются определенные цитокины.
а. Для активации Т-киллеров (цитотоксических лимфоцитов).
б. Для активации иммунного воспаления (т.е. для «нанимания» осуществляющих его лейкоцитов).
2. Во-вторых, на Т-хелперах данного клона появляются (экспрессируются) специфические мембранные молекулы.
а. Рецепторы для активационных цитокинов, благодаря которым Т-хелперы резко усиливают свою чувствительность к «сигналам активации».
б. Других молекул межклеточного взаимодействия.
37.5. Действие активационных цитокинов
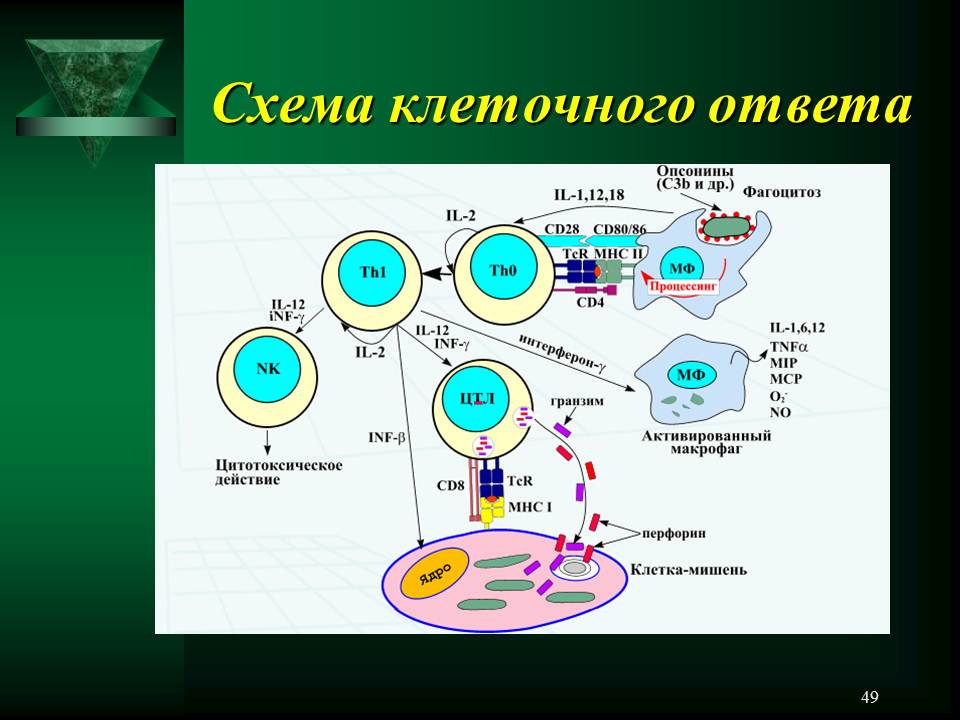
Активационные цитокины синтезируются всеми клетками, участвующими в иммунном ответе. При клеточном иммунном ответе это АПК, Т-хелперы, цитотоксические лимфоциты, лейкоциты воспалительной реакции. В таком «перекрестном» действии иммунокомпетентных клеток и их партнеров проявляется, в числе прочего, кооперативный механизм действия иммунной системы (Рис. 37.5-1).

Рис. 37.5-1. Схема взаимодействия клеток в ходе клеточного иммунного ответа
(по Воробьеву А.А., 2002 г.)
А. Эти цитокины вызывают активацию Т-киллеров, принимающих участие в эффекторном звене клеточного иммунного ответа.
Б. Кроме этого, активационные цитокины стимулируют развитие в зоне нахождения причинного антигена воспалительной реакции, которая, наряду с действием Т-киллеров, и олицетворяет собой результат клеточного иммунного ответа.
37.6. Эффекторное звено клеточного иммунного ответа
Как уже указывалось, эффекторным звеном клеточного иммунного ответа является иммунное воспаление вкупе с цитотоксической активностью Т-киллеров.
А. Воспалительная реакция является нормальной защитной реакцией макроорганизма на проникновение в него микроба, поэтому само по себе воспаление является признаком наличия инфекционного процесса (хотя в редких случаях и может развиться так называемое асептическое воспаление). Термин «иммунное воспаление», которым обозначается одна из двух основных сторон эффекторного звена клеточного иммунного ответа, означает, что воспалительная реакция организована именно иммунной системой в помощь активированным в ходе иммунного ответа цитотоксическим лимфоцитам. Закономерности развития воспалительной реакции разбираются в курсе патологической физиологии.
Б. Что же касается механизмов уничтожения клеток, несущих чужеродный антиген (клеток-мишеней), Т-киллерами (цитотоксическими лимфоцитами), то они сводятся к двум основным процессам.
1. Это, во-первых, внеклеточная цитотоксичность, осуществляемой перфоринами.
а. Перфорин представляет собой особый протеин. В гранулах цитотоксических лимфоцитах он находится в виде растворимого белка-предшественника.
б. Будучи секретирован Т-киллером, перфорин в течение нескольких секунд полимеризуется в мембране клетки-мишени (липофильные участки наружу, гидрофобные – внутрь клетки) с образованием поры диаметром 16 нм. В результате клетка-мишень разрушается в результате осмотического лизиса (Рис. 37.6-1).

Рис. 37.6-1. Осмотический лизис клетки-мишени как результат воздействия на нее перфоринов, синтезированных цитотоксическими лимфоцитами
2. Во-вторых, запуск в клетках-мишенях процесса апоптоза (генетически запрограммированной гибели клеток без образования токсических продуктов распада). Цитотоксические лимфоциты включают апоптоз в клетке-мишени двумя путями.
а. Через мембранную пору, сформированную перфорином, внутрь клетки-мишени проникают секретируемые цитотоксическим лимфоцитом гранзимы (сериновые протеазы), которые активируют в клетке-мишени каспазы (особые ферменты – цистеиновые протеазы), которые в свою очередь активируют эндонуклеазы, осуществляющие фрагментацию ДНК (кариорексис) (Рис. 37.6-2), вслед за чем происходит выпочковывание апоптозных телец (фрагментов, окруженных мембраной) и распад на них клетки без формирования воспалительной реакции (т.е. продукты распада клетки не являются токсичными для макроорганизма) (Рис. 37.6-3).

Рис. 37.6-2. Дефрагментация ДНК при апоптозе

Рис. 37.6-3. Процесс апоптоза
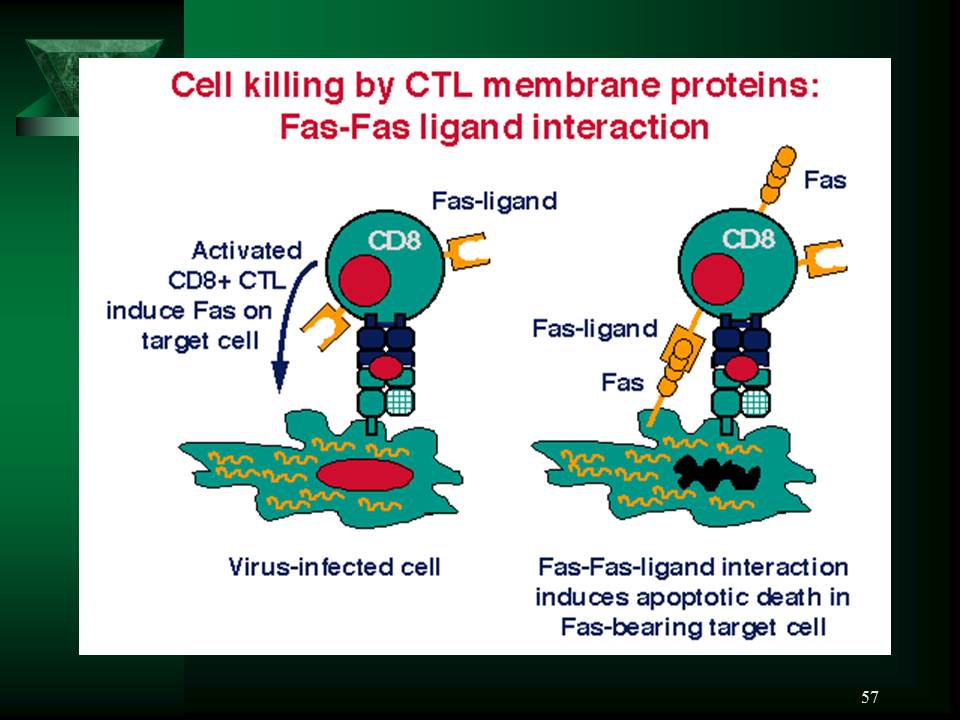
б. Взаимодействие комплекса [TCR + CD3] с MHC-I на поверхности клетки-мишени приводит к включению в геноме ЦТЛ механизма транскрипции гена, детерминирующего синтез Fas-лиганда, который затем экспрессируется на поверхности ЦТЛ. На поверхности клетки-мишени находится рецептор для Fas-лиганда – Fas-белок. Специфическое связывание Fas-белка с Fas-лигандом активизирует Fas-белок, который, в свою очередь запускает процесс активации каспаз (Рис. 37.6-4).

Рис. 37.6-4. Запуск Т-киллером апоптоза клетки-мишени вследствие экспрессии на нем Fas-лиганда и специфического взаимодействия последнего с Fas-рецептором (Fas-белком) на поверхности клетки-мишени
в. На организацию сигнала к апоптозу для клетки-мишени цитотоксическому лимфоциту требуется не более 5 минут, после чего он физически переходит к другой клетке-мишени. Т.е. ЦТЛ является серийным киллером (Рис. 37.6-5).

Рис. 37.6-5. Серийный убийца – цитотоксический лимфоцит (Т-киллер)
(на рисунке видно, что на поверхности клетки-мишени – например, клетки, инфицированной вирусом – меняется «репертуар» рецепторных молекул, что и делает возможным прикрепление к ней Т-киллера с последующим запуском описанных выше путей внеклеточной цитотоксичности последнего)
г. После завершения апоптоза происходит своеобразная «уборка» образовавшихся продуктов распада клетки, в которой участвуют макрофаги и дендритные клетки.
1. Макрофаги фагоцитируют апоптозные тельца.
2. Дендритные клетки играют двоякую роль.
а. С одной стороны, они поглощают апоптозные тельца макрофагоцитозом.
б. С другой стороны, дендритные клетки способны индуцировать иммунный ответ на компоненты апоптозных телец.
37.7. Завершающие процессы эффективного клеточного иммунного ответа
Эффективный иммунный ответ приводит к элиминации (т.е. уничтожению) причинного антигена. С этого момента организм начинает «гасить» иммунологическую реакцию, чтобы не допустить перенапряжения иммунной системы, в частности – дефицита лимфоцитов (так как продолжительность жизни активированных лимфоцитов не велика). События развиваются в двух направлениях.
А. Организовывается супрессия (т.е. подавление) иммунного ответа. Этот процесс осуществляет, в частности, специальная субпопуляция цитотоксических лимфоцитов – Т-супрессоры.
1. Происходит гибель активированных клеток. Механизмы этой гибели аналогичны тем, которые разбирались в разделе 37.6.Б, поскольку на этот раз активированные в ходе иммунного ответа клетки сами являются мишенью действия ЦТЛ.
2. Наряду с этим, путем синтеза соответствующих цитокинов, происходит ингибиция активности активированных в ходе иммунного ответа клеток.
Б. Одновременно появляются клетки иммунологической памяти. Это долгоживущие и не до конца дифференцированные Т-лимфоциты, которые при повторном контакте с причинным антигеном обуславливают развития вторичного иммунного ответа. В отличие от первичного (т.е. в ответ на первый контакт с причинным антигеном), вторичный иммунный ответ развивается значительно быстрее, так как начинается не с одного клона недифференцированных клеток, а со сравнительно многочисленного пула клеток, уже прошедших первые стадии дифференцировки.
13Г. Тестовые вопросы по теме занятия
Несущая часть антигена обуславливает:
-индукцию иммунного ответа
-иммунногенность антигена
взаимодействие антигена с иммуноглобулинами и антигенраспознающими рецепторами лимфоцитов
антигенность антигена
Эпитопы в составе антигена обуславливают:
индукцию иммунного ответа
иммунногенность антигена
-взаимодействие антигена с иммуноглобулинами и антигенраспознающими рецепторами лимфоцитов
-антигенность антигена
Охарактеризуйте молекулы (антигены) МНС:
-антигенпредставляющие молекулы
-используются для презентации пептидных антигенов
используются для презентации полисахаридных антигенов
используются для презентации липидных антигенов
-основные антигенпредставляющие молекулы
Охарактеризуйте молекулы (антигены) CD1:
-антигенпредставляющие молекулы
используются для презентации пептидных антигенов
-используются для презентации полисахаридных антигенов
-используются для презентации липидных антигенов
основные антигенпредставляющие молекулы
Основную роль в индукции иммунного ответа играют:
-пептидные антигены
полисахаридные антигены
липидные антигены
Наибольшей иммуногенностью обладают:
-пептидные антигены
полисахаридные антигены
липидные антигены
Охарактеризуйте антигены (молекулы) МНС-I:
-мембранные гликопротеины
-состоят из двух полипептидных цепей
-используются для представления антигена CD8-лимфоцитам
используются для представления антигена CD4-лимфоцитам
Охарактеризуйте антигены (молекулы) МНС-II:
-мембранные гликопротеины
-состоят из двух полипептидных цепей
используются для представления антигена CD8-лимфоцитам
-используются для представления антигена CD4-лимфоцитам
Охарактеризуйте антигены (молекулы) CD1:
-мембранные гликопротеины
-состоят из двух полипептидных цепей
-по структуре схожи с МНС-I
по структуре схожи с МНС-II
Охарактеризуйте антигены (молекулы) МНС-I:
-одна из цепей «заякоревается» в цитоплазматической мембране, имея цитоплазматический участок, и формирует углубление, куда помещается процессированный антиген, вторая полипептидная цепь (лёгкая), ковалентно связанная с первой, не имеет цитоплазматического участка
представляют собой две одинаковые полипептидные цепи, «заякоренные» в цитоплазматической мембране и имеющие цитоплазматический фрагмент, углубление для процессированного антигена формируется между этих двух цепей
Охарактеризуйте антигены (молекулы) МНС-II:
одна из цепей «заякоревается» в цитоплазматической мембране, имея цитоплазматический участок, и формирует углубление, куда помещается процессированный антиген, вторая полипептидная цепь (лёгкая), ковалентно связанная с первой, не имеет цитоплазматического участка
-представляют собой две одинаковые полипептидные цепи, «заякоренные» в цитоплазматической мембране и имеющие цитоплазматический фрагмент, углубление для процессированного антигена формируется между этих двух цепей
Антигены (молекулы) MHC-I:
-экспрессированны на всех ядросодержащих клетках
экспрессированны на макрофагах, дендритных клетках, в-лимфоцитах и клетках эндотелия сосудов
экспрессированны на многих лимфоидных и не лимфоидных клетках
Антигены (молекулы) MHC-II:
экспрессированны на всех ядросодержащих клетках
-экспрессированны на макрофагах, дендритных клетках, в-лимфоцитах и клетках эндотелия сосудов
экспрессированны на многих лимфоидных и не лимфоидных клетках
Антигены (молекулы) CD1:
экспрессированны на всех ядросодержащих клетках
экспрессированны на макрофагах, дендритных клетках, в-лимфоцитах и клетках эндотелия сосудов
-экспрессированны на многих лимфоидных и не лимфоидных клетках
Антиген бактериальной клеточной стенки:
-O-Ag
К-Ag
Vi-Ag
Н-Ag
Антигены бактериальной капсулы:
O-Ag
-К-Ag
-Vi-Ag
Н-Ag
Антиген бактериальных жгутиков:
O-Ag
К-Ag
Vi-Ag
-Н-Ag
Начальный этап клеточного иммунного ответа:
-взаимодействие с антигеном антигенпрезентирующей клетки
процессинг антигена
презентация антигена
активация Т-хелпера первого типа и синтез им активационных цитокинов
активация Т-хелпера второго типа и синтез им активационных цитокинов
активация соответствующего клона Т-киллера и лейкоцитов воспалительной реакции
уничтожение чужеродного антигена Т-киллерами и в ходе иммунного воспаления
супрессия иммунного ответа и появление клеток иммунологической памяти
После взаимодействия с антигеном антигенпрезентирующей клетки в ходе клеточного иммунного ответа происходит:
-процессинг антигена
презентация антигена
активация Т-хелпера первого типа и синтез им активационных цитокинов
активация Т-хелпера второго типа и синтез им активационных цитокинов
активация соответствующего клона Т-киллера и лейкоцитов воспалительной реакции
уничтожение чужеродного антигена Т-киллерами и в ходе иммунного воспаления
супрессия иммунного ответа и появление клеток иммунологической памяти
После процессинга антигена в ходе клеточного иммунного ответа происходит:
взаимодействие с антигеном антигенпрезентирующей клетки
-презентация антигена
активация Т-хелпера первого типа и синтез им активационных цитокинов
активация Т-хелпера второго типа и синтез им активационных цитокинов
активация соответствующего клона Т-киллера и лейкоцитов воспалительной реакции
уничтожение чужеродного антигена Т-киллерами и в ходе иммунного воспаления
супрессия иммунного ответа и появление клеток иммунологической памяти
После презентации антигена в ходе клеточного иммунного ответа происходит:
взаимодействие с антигеном антигенпрезентирующей клетки
процессинг антигена
-активация Т-хелпера первого типа и синтез им активационных цитокинов
активация Т-хелпера второго типа и синтез им активационных цитокинов
активация соответствующего клона Т-киллера и лейкоцитов воспалительной реакции
уничтожение чужеродного антигена Т-киллерами и в ходе иммунного воспаления
супрессия иммунного ответа и появление клеток иммунологической памяти
После активации Т-хелпера первого типа и синтеза им активационных цитокинов в ходе клеточного иммунного ответа происходит:
взаимодействие с антигеном антигенпрезентирующей клетки
процессинг антигена
презентация антигена
активация Т-хелпера второго типа и синтез им активационных цитокинов
-активация соответствующего клона Т-киллера и лейкоцитов воспалительной реакции
уничтожение чужеродного антигена Т-киллерами и в ходе иммунного воспаления
супрессия иммунного ответа и появление клеток иммунологической памяти
После активации соответствующего клона Т-киллера и лейкоцитов воспалительной реакции в ходе клеточного иммунного ответа происходит:
взаимодействие с антигеном антигенпрезентирующей клетки
процессинг антигена
презентация антигена
активация Т-хелпера первого типа и синтез им активационных цитокинов
активация Т-хелпера второго типа и синтез им активационных цитокинов
-уничтожение чужеродного антигена Т-киллерами и в ходе иммунного воспаления
супрессия иммунного ответа и появление клеток иммунологической памяти
Завершающий этап клеточного иммунного ответа в случае элиминации чужеродного антигена:
взаимодействие с антигеном антигенпрезентирующей клетки
процессинг антигена
презентация антигена
активация Т-хелпера первого типа и синтез им активационных цитокинов
активация Т-хелпера второго типа и синтез им активационных цитокинов
активация соответствующего клона Т-киллера и лейкоцитов воспалительной реакции
-супрессия иммунного ответа и появление клеток иммунологической памяти
Процессинг антигена:
-поглощение антигена антигенпрезентирующей клеткой, его частичная деградация с вычленением эпитопов, соединение каждого вычлененного эпитопа с молекулой МНС
вывод комплекса [эпитоп + МНС] на внешнюю мембрану антигенпрезентирующей клетки
Презентация антигена:
поглощение антигена антигенпрезентирующей клеткой, его частичная деградация с вычленением эпитопов, соединение каждого вычлененного эпитопа с молекулой МНС
-вывод комплекса [эпитоп + МНС] на внешнюю мембрану антигенпрезентирующей клетки
Процессированный антиген:
-соединение эпитопа антигена с молекулой МНС
комплекс [эпитоп + МНС], экспрессированный на внешней мембране антигенпрезентирующей клетки
Презентированный антиген:
соединение эпитопа антигена с молекулой МНС
-комплекс [эпитоп + МНС], экспрессированный на внешней мембране антигенпрезентирующей клетки
Антиген, участвующий в реакции агглютинации:
-агглютиноген
агглютинин
агглютинат
Антитело, участвующее в реакции агглютинации:
агглютиноген
-агглютинин
агглютинат
Иммунный комплекс, образующийся в результате реакции агглютинации:
агглютиноген
агглютинин
-агглютинат
Условия осуществления реакции агглютинации:
-антиген, в ней участвующий, был не менее, чем четырёхвалентным
антиген, в ней участвующий, был не менее, чем двухвалентным
иммуноглобулин, в ней участвующий, был не менее, чем четырёхвалентным
-иммуноглобулин, в ней участвующий, был не менее, чем двухвалентным
Пластинчатая реакция агглютинации:
-чаще используется для идентификации антигена
чаще используется для обнаружения антител и определения их количества (титра)
Объёмная реакция агглютинации:
чаще используется для идентификации антигена
-чаще используется для обнаружения антител и определения их количества (титра)






