Лекция 8. Углеводы. Обмен углеводов.
Строение, свойства и функции основных моно-, олиго- и полисахаридов. Общие пути обмена глюкозы в клетке.
Синтез и распад гликогена. Механизм ветвления гликогена. Ковалентная модификация и аллостерическая регуляция гликогенфосфорилазы и гликогенсинтазы. Механизм синхронизации мышечного сокращения и гликогенолиза. Гликогенозы.
3. Гликолиз: последовательность реакций. Гликолитическая оксидоредукция. Субстратное фосфорилирование.
Ключевые реакции глюконеогенеза. Аллостерическая регуляция ферментов гликолиза и глюконеогенеза. Роль фруктозо-2,6-бисфосфата.
Реакции пентозофосфатного пути превращения глюкозы. Образование восстановительных эквивалентов и рибозы.
Метаболизм фруктозы и галактозы. Регуляция уровня глюкозы в крови. Источники глюкозы крови. Цикл Кори и глюкозо-аланиновый цикл. Почечный порог для глюкозы, глюкозурия. Толерантность к глюкозе.
| Краткое содержание | Конспект | ||
| 1. Строение, свойства и функции основных моно-, олиго- и полисахаридов. Общие пути обмена глюкозы в клетке | |||
Углеводы –это альдегидные или кетонные производные полиатомных (содержащих более одной ОН-группы) спиртов или как соединения, при гидролизе которых образуются эти производные.
Классификация:1) моносахариды (не могут быть гидролизованы до более простых форм) – триозы, тетрозы, пентозы, гексозы и пр.; 2) олигосахариды (при гидролизе дают 2-10 моносахаридов) – дисахариды, трисахариды и пр.; 3) полисахариды (дают при гидролизе более 10 моносахаридов) – целлюлоза, гликоген, крахмал и пр.
Свойства моносахаридов:
1) изомерия (D и L),
2) пиранозные и фуранозные кольцевые структуры,
3) α- и β-аномеры,
4) эпимеры,
5) альдо-кето-изомеризация.
Физиологически важные пентозы
 Дисахариды:
1) сахароза (глюкоза + фруктоза),
2) лактоза (глюкоза + галактоза),
3) мальтоза (глюкоза + глюкоза).
Дисахариды
Дисахариды:
1) сахароза (глюкоза + фруктоза),
2) лактоза (глюкоза + галактоза),
3) мальтоза (глюкоза + глюкоза).
Дисахариды
 Полисахариды:
1) гликоген,
2) крахмал,
3) инулин,
4) декстрины,
5) целлюлоза,
6) хитин,
7) глюкозамингликаны,
8) гликопротеины.
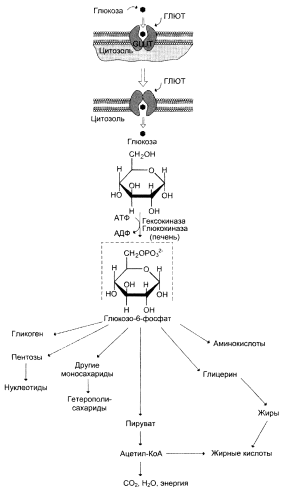
Метаболизм глюкозы в клетке
При нормальном рационе питания концентрация глюкозы в крови поддерживается на уровне 3,3-5,5 ммоль/л (60-100 мг/дл).
Фосфорилирование свободных моносахаридов (используется АТФ) – обязательная реакция на пути их использования. Она приводит к образованию более реакционно-способных соединений и поэтому может рассматриваться как реакция активации. Фосфорилирование глюкозы – практически необратимая реакция, т.к. протекает с использованием значительного количества энергии. В печени глюкоза фосфорилируется с помощью ферментов – глюкокиназы (в период пищеварения) и гексокиназы (в постабсорбтивный период).
Дефосфорилирование глюкозо-6-фосфата
Превращение глюкозо-6-фосфата в глюкозу возможно в печени, почках и клетках эпителия кишечника. В клетках этих органов имеется фермент глюкозо-6-фосфатаза, катализирующий отщепление фосфатной группы гидролитическим путём:
Глюкозо-6-фосфат + Н2О → Глюкоза + Н3РО4
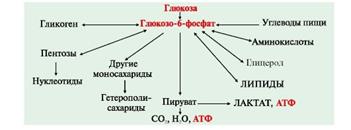
.Общая схема метаболизма углеводов с указанием главных конечных продуктов
У всех млекопитающих глюкоза в клетках превращается в пируват и лактат по метаболическому пути, который называется гликолизом. Для вступления на этот путь необходимо предварительное фосфорилирование. Гликолиз может протекать в отсутствие кислорода (анаэробно), если конечным продуктом является лактат. Ткани, которые потребляют кислород (аэробные условия), способны осуществлять превращение пирувата в ацетил-СоА, который далее может вступать в цикл лимонной кислоты; в этом цикле ацетил-СоА полностью окисляется до СО2 и Н2О; большая часть потенциальной свободной энергии процесса запасается в форме АТР в результате окислительного фосфорилирования. Таким образом, глюкоза служит главным видом топлива для многих тканей, однако она (а также ее метаболиты) участвует и в других процессах.
1. Глюкоза превращается в полимер гликоген, который запасается в ряде тканей, в особенности в скелетных мышцах и в печени.
2. Субстрат пентозофосфатного пути является одним из промежуточных продуктов гликолиза. Этот путь служит источником восстановительных эквивалентов (2Н), используемых в процессах биосинтеза, например в биосинтезе жирных кислот; кроме того, он является источником рибозы, необходимой для синтеза нуклеотидов и нуклеиновых кислот.
3. Триозофосфат, образующийся на одной из стадий гликолиза, является источником глицерола, используемого в синтезе ацилглицеролов (жиров).
4. Пируват и ряд промежуточных соединений цикла лимонной кислоты – это источники углеродных скелетов, используемых в синтезе аминокислот, а ацетил-СоА служит основным строительным блоком в синтезе длинноцепочечных жирных кислот и холестерола – предшественника всех синтезируемых в организме стероидов.
Полисахариды:
1) гликоген,
2) крахмал,
3) инулин,
4) декстрины,
5) целлюлоза,
6) хитин,
7) глюкозамингликаны,
8) гликопротеины.
Метаболизм глюкозы в клетке
При нормальном рационе питания концентрация глюкозы в крови поддерживается на уровне 3,3-5,5 ммоль/л (60-100 мг/дл).
Фосфорилирование свободных моносахаридов (используется АТФ) – обязательная реакция на пути их использования. Она приводит к образованию более реакционно-способных соединений и поэтому может рассматриваться как реакция активации. Фосфорилирование глюкозы – практически необратимая реакция, т.к. протекает с использованием значительного количества энергии. В печени глюкоза фосфорилируется с помощью ферментов – глюкокиназы (в период пищеварения) и гексокиназы (в постабсорбтивный период).
Дефосфорилирование глюкозо-6-фосфата
Превращение глюкозо-6-фосфата в глюкозу возможно в печени, почках и клетках эпителия кишечника. В клетках этих органов имеется фермент глюкозо-6-фосфатаза, катализирующий отщепление фосфатной группы гидролитическим путём:
Глюкозо-6-фосфат + Н2О → Глюкоза + Н3РО4
.Общая схема метаболизма углеводов с указанием главных конечных продуктов
У всех млекопитающих глюкоза в клетках превращается в пируват и лактат по метаболическому пути, который называется гликолизом. Для вступления на этот путь необходимо предварительное фосфорилирование. Гликолиз может протекать в отсутствие кислорода (анаэробно), если конечным продуктом является лактат. Ткани, которые потребляют кислород (аэробные условия), способны осуществлять превращение пирувата в ацетил-СоА, который далее может вступать в цикл лимонной кислоты; в этом цикле ацетил-СоА полностью окисляется до СО2 и Н2О; большая часть потенциальной свободной энергии процесса запасается в форме АТР в результате окислительного фосфорилирования. Таким образом, глюкоза служит главным видом топлива для многих тканей, однако она (а также ее метаболиты) участвует и в других процессах.
1. Глюкоза превращается в полимер гликоген, который запасается в ряде тканей, в особенности в скелетных мышцах и в печени.
2. Субстрат пентозофосфатного пути является одним из промежуточных продуктов гликолиза. Этот путь служит источником восстановительных эквивалентов (2Н), используемых в процессах биосинтеза, например в биосинтезе жирных кислот; кроме того, он является источником рибозы, необходимой для синтеза нуклеотидов и нуклеиновых кислот.
3. Триозофосфат, образующийся на одной из стадий гликолиза, является источником глицерола, используемого в синтезе ацилглицеролов (жиров).
4. Пируват и ряд промежуточных соединений цикла лимонной кислоты – это источники углеродных скелетов, используемых в синтезе аминокислот, а ацетил-СоА служит основным строительным блоком в синтезе длинноцепочечных жирных кислот и холестерола – предшественника всех синтезируемых в организме стероидов.
|  Привести примеры молекул, имеющих указанные свойства и их структурные формулы:
Физиологически важные гексозы
Привести примеры молекул, имеющих указанные свойства и их структурные формулы:
Физиологически важные гексозы
 Напишите структурные формулы указанных дисахаридов:
Перечислите функции указанных полисахаридов:
Напишите структурные формулы указанных дисахаридов:
Перечислите функции указанных полисахаридов:
| ||
| 2. Синтез и распад гликогена. Механизм ветвления гликогена. Ковалентная модификация и аллостерическая регуляция гликогенфосфорилазы и гликогенсинтазы. Механизм синхронизации мышечного сокращения и гликогенолиза. Гликогенозы | |||
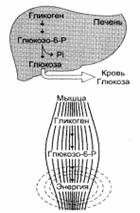
Гликоген– главная форма запасания углеводов у животных и человека. Накапливается гликоген главным образом в печени (до 6% от массы печени) и в скелетных мышцах, где его содержание редко превышает 1%. Запасы гликогена в скелетных мышцах ввиду значительно большей массы последних превышают его запасы в печени. Гликоген присутствует в цитозоле в форме гранул диаметром от 10 до 40 нм.
Функции гликогена в печени и мышцах
 Образование УДФ-глюкозы
Образование УДФ-глюкозы
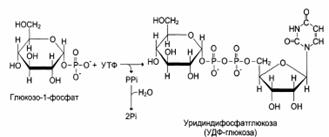 Образованная УДФ-глюкоза далее используется как донор остатка глюкозы при синтезе гликогена. Эту реакцию катализирует фермент гликогенсинтаза (глюкозилтрансфераза).
Поскольку гликоген в клетке никогда не расщепляется полностью, синтез гликогена осуществляется путём удлинения уже имеющейся молекулы полисахарида, называемой «затравкой», или «праймер». К «затравке» последовательно присоединяются молекулы глюкозы. В состав «затравки» может входить белок гликогенин, в котором к ОН-группе одного из тирозиновых остатков присоединена олигосахаридная цепочка, состоящая из 8 остатков глюкозы.
Разветвлённая структура гликогена образуется при участи фермента амило-1,4→1,6-гликозилтрансферазы (фермент ветвления).
Распад гликогена (гликогенолиз)
Стадией, лимитирующей скорость гликогенолиза, является реакция, катализируемая фосфорилазой:
(С6)n + Pi → (С6)n-1 + Глюкозо-1-фосфат
Гликоген Гликоген
Фермент специфично катализирует фосфоролитическое расщепление (фосфоролиз) (1→4)-связей гликогена, продуктом является глюкозо-1-фосфат. Остатки глюкозы отщепляются от дальних концов молекулы гликогена до тех пор, пока на ветвях, идущих от точки ветвления ([1→6]-связи), не останется примерно по 4 остатка глюкозы. Другой фермент (α-[1→4] → α-[1→4]-глюкантрансфераза) переносит трисахаридный фрагмент с одной цепи на другую, экспонируя (1→6)-пункт ветвления. Гидролитическое расщепление (1→6)-связей осуществляет деветвящий (дебранчинг) фермент (амило-[1→6]-глюкозидаза); по-видимому, это второй вид активности глюкантрансферазы. После удаления ветви на цепь гликогена снова действует фосфорилаза. Совместное действие фосфорилазы и других рассмотренных выше ферментов приводит к полному распаду гликогена. Реакция, катализируемая фосфоглюкомутазой, обратима; поэтому из глюкозо-1-фосфата может образовываться глюкозо-6-фосфат.
В печени и почках (но не в мышцах) имеется специфический фермент глюкозо-6-фосфатаза, отщепляющий фосфат от глюкозо-6-фосфата. Образовавшаяся глюкоза диффундирует из клеток в кровь. Это заключительная стадия гликогенолиза в печени, приводящего к повышению содержания глюкозы в крови.
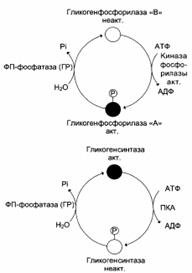
Ковалентная модификация и аллостерическая регуляция гликогенфосфорилазы и гликогенсинтазы
Образованная УДФ-глюкоза далее используется как донор остатка глюкозы при синтезе гликогена. Эту реакцию катализирует фермент гликогенсинтаза (глюкозилтрансфераза).
Поскольку гликоген в клетке никогда не расщепляется полностью, синтез гликогена осуществляется путём удлинения уже имеющейся молекулы полисахарида, называемой «затравкой», или «праймер». К «затравке» последовательно присоединяются молекулы глюкозы. В состав «затравки» может входить белок гликогенин, в котором к ОН-группе одного из тирозиновых остатков присоединена олигосахаридная цепочка, состоящая из 8 остатков глюкозы.
Разветвлённая структура гликогена образуется при участи фермента амило-1,4→1,6-гликозилтрансферазы (фермент ветвления).
Распад гликогена (гликогенолиз)
Стадией, лимитирующей скорость гликогенолиза, является реакция, катализируемая фосфорилазой:
(С6)n + Pi → (С6)n-1 + Глюкозо-1-фосфат
Гликоген Гликоген
Фермент специфично катализирует фосфоролитическое расщепление (фосфоролиз) (1→4)-связей гликогена, продуктом является глюкозо-1-фосфат. Остатки глюкозы отщепляются от дальних концов молекулы гликогена до тех пор, пока на ветвях, идущих от точки ветвления ([1→6]-связи), не останется примерно по 4 остатка глюкозы. Другой фермент (α-[1→4] → α-[1→4]-глюкантрансфераза) переносит трисахаридный фрагмент с одной цепи на другую, экспонируя (1→6)-пункт ветвления. Гидролитическое расщепление (1→6)-связей осуществляет деветвящий (дебранчинг) фермент (амило-[1→6]-глюкозидаза); по-видимому, это второй вид активности глюкантрансферазы. После удаления ветви на цепь гликогена снова действует фосфорилаза. Совместное действие фосфорилазы и других рассмотренных выше ферментов приводит к полному распаду гликогена. Реакция, катализируемая фосфоглюкомутазой, обратима; поэтому из глюкозо-1-фосфата может образовываться глюкозо-6-фосфат.
В печени и почках (но не в мышцах) имеется специфический фермент глюкозо-6-фосфатаза, отщепляющий фосфат от глюкозо-6-фосфата. Образовавшаяся глюкоза диффундирует из клеток в кровь. Это заключительная стадия гликогенолиза в печени, приводящего к повышению содержания глюкозы в крови.
Ковалентная модификация и аллостерическая регуляция гликогенфосфорилазы и гликогенсинтазы
|
Механизм синхронизации мышечного сокращения и гликогенолиза
Регуляция обмена гликогена в мышцах обеспечивает энергетическим материалом как интенсивную работу мышц (бег или борьба), так и энергозатраты в состоянии покоя.
В экстремальных ситуациях в мышечных клетках мобилизация гликогена ускоряется адреналином. Связывание адреналина с β-рецепторами, ассоциированными с аденилатциклазной системой, приводит к образованию цАМФ (cAMP) в клетке, а затем фосфорилированию и активации киназы фосфорилазы и гликогенфосфорилазы.
Образование цАМФ, стимулированное адреналином, служит сигналом к увеличению производства энергии в результате ускорения расщепления гликогена. В ходе распада гликогена образуется глюкозо-6-фосфат, из которого позже происходит синтез АТФ.
В состоянии покоя при низких концентрациях адреналина в крови гликогенфосфорилаза мыщц находится в дефосфорилированном – неактивном состоянии (форма В), но распад гликогена всё-таки происходит. Это объясняется тем, что гликогенфосфорилаза активируется способом, не связанным с её фосфорилированием, т.к. уровень цАМФ в клетке низкий. В данной ситуации происходит аллостерическая активация гликогенфосфорилазы В. Активатором фермента служат АМФ и Н3РО4, образовавшиеся в клетке при распаде АТФ (путь 1).
При умеренных мышечных сокращениях, т.е. в ситуации, не требующей участия в регуляции цАМФ, аллостерическим способом активируется киназа фосфорилазы (путь 2). В данном случае аллостерическими эффекторами служат ионы Са2+, концентрация которых резко возрастает при сокращении мышц в ответ на сигнал от двигательного нерва.
Синтез и распад гликогена
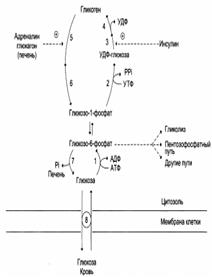
| 1 – гексокиназа или глюкокиназа (печень); 2 – УДФ-глюклпирофосфорилаза; 3 – гликогенсинтаза; 4 – амило-1,4→1,6-гликозилтрансфераза (фермент ветвления); 5 – гликогенфосфорилаза; 6 – «деветвящий» фермент; 7 – глюкозо-6-фосфатаза (печень); 8 – транспортные системы ГЛЮТ. |