ЧАСТЬ II. ОМЫЛЕНИЕ СЛОЖНЫХ ЭФИРОВ В ПРИСУТСТВИИ
ЩЁЛОЧИ
Для выполнения этой части работы, в две мерные колбочки на 100 мл, предварительно вымытые и высушенные, наливают по 50 мл раствора: в первую 0,01н раствор сложного эфира (метил или этилацетата), во вторую 1/60 н раствор едкого натра. Эти колбочки закрывают пробкой и устанавливают в термостате с температурой 250С.
Через 10-15 мин. раствор эфира выливается в раствор щелочи, причем колбочку со щелочью не вынимают из термостата.
Через 10 минут отбирают пробу в количестве 10 мл в коническую колбу, в которую заранее наливают 10 мл воды и помещают в кристаллизатор со льдом. Отобранная проба титруется кислотой с индикатором метиловым оранжевым.
Затем последовательно через промежутки времени 20, 40, 70, 100 минут (от начала реакции) отбирают другие пробы по 10 мл и титруют кислотой одной и той же концентрации. Реакция омыления сложного эфира щёлочью практически заканчивается через 10-12 часов.
Пусть n0 мл – количество кислоты, которое пошло на титрование 5 мл исходной щелочи в 15 мл воды. Пусть по времени t на титрование пробы смеси потребуется nt мл кислоты. Для времени, когда реакция практически полностью доходит до конца, количество кислоты затраченной на титрование, будет n¥ мл.
Если нормальность кислоты, взятой для титрования N, то в начале реакции во взятом для титрования объёме V (мл) содержит: n0 × N миллиграмм-эквивалентов щёлочи (миллиграмм-эквивалент/мл = грамм-эквивалент). Ко времени t количество щёлочи, нейтрализованное кислотой, определяется как nt × N миллиграмм-эквивалентов щёлочи. Если щелочь в избытке, как в нашем случае, то количество сложного эфира, подвергающееся омылению, определится как разность между мг-эквивалент щелочи, нейтрализованной кислотой, а именно (n0 - n¥).
Следовательно, ко времени t мы получим следующие количества реагирующих веществ:
- для щелочи: (а – х) = nt × N,
- для сложного эфира: (в – х) = (n0 – n¥) × N – (n0 – nt) × N = N × (nt - n¥),
- для начального количества щелочи: а = n0 × N,
- для начального количества сложного эфира: в = (n0 - n¥) × N, (а – в) = n¥ × N
Если полученные выражения подставить в уравнение (11), то константа скорости реакции для случая, когда в исходной смеси имеется избыток щелочи, определится следующим выражением:
(12)
где V – объем взятой пробы,
N – нормальность кислоты взятой для титрования.
Вода, которая используется при титровании, не должна содержать растворенный углекислый газ, который уделяется кипячением воды в течение часа.
Полученные данные и результаты расчета рекомендуется записывать в виде таблицы:
| t мин | nt | nt - n¥ | |
Из полученных значений констант скоростей омыления эфира находят среднее значение.





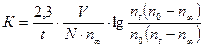 (12)
(12)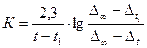
 (1),
интегрируя которое получим:
(1),
интегрируя которое получим:
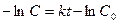 (2) или
(2) или  (3),
откуда:
(3),
откуда:  (4) – уравнение для константы скорости I-го порядка, {t-1}.
где С0 - начальная концентрация эфира;
С - концентрация эфира в данный момент времени t.
В общем виде реакцию гидролиза эфира можно представить уравнением:
RA + H2O = ROH + HA,
гдеRA – сложный эфир;
ROH – образующийся спирт;
HA – образующаяся кислота.
Скорость гидролиза, протекающего как реакция первого порядка, выразится уравнением:
(4) – уравнение для константы скорости I-го порядка, {t-1}.
где С0 - начальная концентрация эфира;
С - концентрация эфира в данный момент времени t.
В общем виде реакцию гидролиза эфира можно представить уравнением:
RA + H2O = ROH + HA,
гдеRA – сложный эфир;
ROH – образующийся спирт;
HA – образующаяся кислота.
Скорость гидролиза, протекающего как реакция первого порядка, выразится уравнением:
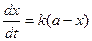 , (5)
где х – количество разложившегося сложного эфира;
а – первоначальное количество сложного эфира.
Интегрируя последнее уравнение, получим выражение для константы скорости гидролиза сложного эфира:
, (5)
где х – количество разложившегося сложного эфира;
а – первоначальное количество сложного эфира.
Интегрируя последнее уравнение, получим выражение для константы скорости гидролиза сложного эфира:
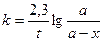 (6)
(6)
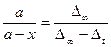 /10/.
В этом случае константа скорости гидролиза сложного эфира выразится следующим образом:
/10/.
В этом случае константа скорости гидролиза сложного эфира выразится следующим образом:
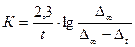 /11/.
Как видно из уравнений (10) и (11) титр применяемой щелочи не нужен для расчета и может даже быть не известен, если для всех определений применять раствор щелочи постоянной концентрации.
Следует отметить, что при вычислении констант скоростей ре
/11/.
Как видно из уравнений (10) и (11) титр применяемой щелочи не нужен для расчета и может даже быть не известен, если для всех определений применять раствор щелочи постоянной концентрации.
Следует отметить, что при вычислении констант скоростей ре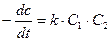 (7)
Пусть a и b, исходные количества молей веществ А и В, V-объем системы. Если к моменту времени t прореагировало x молей ве
(7)
Пусть a и b, исходные количества молей веществ А и В, V-объем системы. Если к моменту времени t прореагировало x молей ве и
и 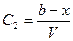 ,
а скорость реакции:
,
а скорость реакции:  После подстановки этих выражений в уравнение (7) получим:
После подстановки этих выражений в уравнение (7) получим:
 (8).
Из этого уравнения видим, что скорость бимолекулярной реакции зависит от разведения. Интегрируя уравнение (8) и находя значение постоянной интегрирования при условиях t=0, x=0 получаем окончательное выражение для константы скорости бимолекулярной реакции:
(8).
Из этого уравнения видим, что скорость бимолекулярной реакции зависит от разведения. Интегрируя уравнение (8) и находя значение постоянной интегрирования при условиях t=0, x=0 получаем окончательное выражение для константы скорости бимолекулярной реакции:
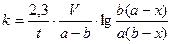 (9).
Константа скорости реакции второго порядка, в отличие от константы скорости первого порядка, имеет размерность /время-1/концентрация-1/, и величина константы, следовательно, зависит от выбранных для концентрации единиц.
Хорошо изученной бимолекулярной реакцией является реакция омыления сложного эфира щёлочью, которая описывается следующим уравнением:
RA + MOH = ROH + MA,
где RA – сложный эфир
MOH – раствор щёлочи
RON – алкоголь
MA – соль
Реакция омыления сложных эфиров щёлочью практически необратима и протекает с заметной скоростью.
Выполнение работы
Внимание!
Работу в кислой и щелочной средах проводить параллельно!
(9).
Константа скорости реакции второго порядка, в отличие от константы скорости первого порядка, имеет размерность /время-1/концентрация-1/, и величина константы, следовательно, зависит от выбранных для концентрации единиц.
Хорошо изученной бимолекулярной реакцией является реакция омыления сложного эфира щёлочью, которая описывается следующим уравнением:
RA + MOH = ROH + MA,
где RA – сложный эфир
MOH – раствор щёлочи
RON – алкоголь
MA – соль
Реакция омыления сложных эфиров щёлочью практически необратима и протекает с заметной скоростью.
Выполнение работы
Внимание!
Работу в кислой и щелочной средах проводить параллельно!

