Язвенная болезнь - полиэтиологична. Главными этиологическими факторами язвенной болезни желудка и двенадцатиперстной кишки являются бактерия Helicobacter pylori и нервно-психический стресс.
В настоящее время есть все основания рассматривать язвенную болезнь как инфекционное заболевание, так как доказана связь между развитием язвенной болезни и инфицированностью Helicobacter pylori (НР). Австралийские ученые Р. Уоррен и Б. Маршалл в 2005 г. получили Нобелевскую премию за «неожиданное и потрясающее» открытие, которое они сделали в 1982 г.: установили, что причиной гастритов и язвенной болезни желудка и двенадцатиперстной кишки является бактерия - НР. Когда Б. Маршалл выделил чистую культуру бактерии, он провел на себе опыт самозаражения, и у него развился острый гастрит. В качестве средства лечения он использовал антибиотикотерапию. В результате этого открытия появилась обоснованная возможность лечить язвенную болезнь антибиотиками, что увеличило частоту излечения язвенной болезни и уменьшило число рецидивов заболевания.
Установлено, что у больных с язвенной болезнью двенадцатиперстной кишки НР обнаруживается в 90-95% случаев, у больных язвенной болезнью желудка - в 80% случаев. Оценку наличия бактерии проводят с помощью серологического анализа крови, иммуноферментного анализа, бактериологического исследования кусочка биопсии слизистой.
Helicobacter pylori является грамотрицательной анаэробной палочкой, которая имеет жгутик и способна вырабатывать уреазу. Этот возбудитель обнаруживается в слизистой оболочке антрального отдела желудка, выявляясь иногда и у здоровых, без какихлибо патологических изменений, но значительно чаще (до 95%) у больных гастритом или язвенной болезнью (рис. 17-3). При попадании в просвет желудка с заглатываемой слюной или с поверхности гастроскопа, желудочного (дуоденального) зонда НР оказывается в сложной для обитания среде (кислое содержимое желудка). Однако благодаря своей уреазной активности бактерии могут существовать в этих условиях. Мочевину, поступающую из
 Рис. 17-3. Микрофотография Helicobacter pylori (окрашивание серебром). Видны многочисленные бактерии на поверхности желудочного эпителия (по Т.Л. Лапиной, 2000)
Рис. 17-3. Микрофотография Helicobacter pylori (окрашивание серебром). Видны многочисленные бактерии на поверхности желудочного эпителия (по Т.Л. Лапиной, 2000)
кровеносного русла, путем пропотевания через стенку капилляров, уреаза превращает в аммиак и СО2, которые и нейтрализуют соляную кислоту желудочного сока, создавая вокруг бактериальной клетки локальное ощелачивание. Аммиак действует раздражающе на G-клетки APUD-системы, увеличивая секрецию гастрина и соответственно НС1.
Жгутики и спиралевидная форма бактерий обеспечивают активное продвижение вперед, и НР в окружении уреазы и аммиака проникает из просвета желудка в слой слизи, где процесс продвижения продолжается. Кроме локального ощелачивания, вокруг бактерий идет снижение вязкости желудочной слизи - муцин разрушается, и НР достигает через защитный слизистый барьер покровно-ямочного эпителия слизистой желудка. Происходит адгезия НР на покровно-ямочный эпителий антрального отдела желудка. Часть микробов пенетрирует в собственную пластинку через межэпителиальные контакты. В эпителиальных клетках возникают дистрофические изменения, что снижает их функциональную активность. Интенсивное размножение и колонизация HP на слизистой антрального отдела желудка ведут к повреждению эпителия вследствие действия фосфолипаз. Выделяют ульцирогенный штамм НР, который синтезирует цитотоксины, активирующие фосфолипазу. В этом случае вероятность изъязвления слизистой оболочки желудка очень велика. Идет разрушение защитных бел-
ковых компонентов, муцина, что открывает путь НР вглубь слизистой оболочки. Аммиак, воздействуя на эндокринные клетки антрального отдела желудка, уменьшает количество D-клеток, вырабатывающих соматостатин, и соответственно падает его концентрация. Выброс гастрина выходит из-под контроля D-клеток, что приводит к гипергастринемии, повышению массы париетальных клеток и гиперпродукции соляной кислоты. Таким образом, инфицирование НР может быть первичным, а повышение секреции соляной кислоты - вторичным звеном в патогенезе язвенной болезни желудка. В подслизистом слое формируется воспалительный инфильтрат (состоящий из нейтрофилов, лимфоцитов, макрофагов, плазматических и тучных клеток), происходит некроз эпителия с образованием язвенного дефекта.
Патогенез язвы ДПК сложнее, чем язвы желудка. НР избирательно заселяют только метаплазированный эпителий и не поражают нормальную слизистую ДПК. Желудочная метаплазия (замещение цилиндрических клеток эпителия ДПК клетками желудочного эпителия) наблюдается у 90% больных дуоденальной язвой. Метаплазия позволяет НР внедряться в клетки слизистой оболочки луковицы ДПК, делая их менее устойчивыми к повреждению соляной кислотой, пепсином, желчью. Длительный заброс в луковицу ДПК кислого желудочного содержимого создает благоприятные условия для развития желудочной метаплазии ее эпителия. Риск развития дуоденальной язвы при выраженном антральном гастрите и проксимальном дуодените, ассоциированных с НР, превышает контрольные в 50 раз, а при нормальной слизистой он практически равен нулю.
Интересно отметить, что инфицированность НР достаточно высока - инфицированность на севере России составляет 50%, на юге и востоке России достигает 80 и 90% соответственно. Только 1/8 инфицированных НР людей заболевает язвенной болезнью.
Однако язвенная болезнь - это не классическая инфекция и одного инфицирования НР недостаточно для ее возникновения.
К главным этиологическим факторам язвенной болезни относят также нервно-психический стресс. Под влиянием длительных или часто повторяющихся психоэмоциональных перенапряжений (тяжелые нервные потрясения, профессиональные неудачи и семейные драмы) нарушается координирующая функция коры головного мозга в отношении подкорковых образований и особенно гипоталамуса. Возникает стойкое возбуждение центров ве-
гетативной нервной системы. Обильная патологическая парасимпатическая импульсация из ЦНС приводит к гиперсекреции НС1 и гипермоторике желудка. Обильная патологическая симпатическая импульсация из ЦНС приводит к выбросу катехоламинов в синапсах и мозговом веществе надпочечников, что вызывает трофические и гемодинамические нарушения в слизистой желудка. Активация гипоталамо-гипофизарно-надпочечниковой системы вызывает усиленную выработку глюкокортикоидов, что влечет за собой гиперсекрецию желудочного сока, спазм сосудов, катаболический эффект (увеличенный распад и сниженный синтез белка). Все вышесказанное обусловливает формирование язвенных дефектов, уменьшение выработки слизи и снижение регенерации.
К предрасполагающим факторам язвенной болезни относят генетические маркеры: высокий уровень продукции НС1 - максимальной кислотопродукции желудка (в результате генетически обусловленного увеличения массы обкладочных клеток и их чувствительности к гастрину); высокий уровень пепсиногена 1 в сыворотке крови - «ульцирогенная фракция пепсиногена»; избыточное выделение гастрина G- клетками в ответ на прием пищи; I группа крови (у этих людей на слизистой оболочке желудка имеются адгезивные рецепторы к Helicobacter pylori); генетически обусловленное уменьшение выработки ряда защитных субстанций (защищающих слизистую от протеолиза), в том числе a1-антитрипсин - ингибитор сериновой протеазы, a2-макроглобулины (составляют 97% общего содержания макроглобулинов плазмы крови - неспецифических ингибиторов протеаз и универсальных регуляторов иммунной системы).
Факторами, способствующими развитию болезни, являются алиментарные факторы (острая, горячая пища, специи, приправы), вредные привычки (курение и злоупотребление крепкими спиртными напитками, определенную роль в развитии язвенной болезни отводят употреблению кофе), ульцирогенные лекарственные средства. Особенно опасны длительные перерывы в приеме пищи, прежде всего у лиц с повышенной секрецией и кислотностью желудочного сока.
Все этиологические факторы потенциируют друг друга и приводят к формированию факторов «агрессии». В конечном итоге, быть или не быть язвенной болезни, определяется соотношением факторов «защиты» и факторов «агрессии».
К факторам «агрессии» относят прежде всего инфицирование НР и разрушение слизисто-бикарбонатного барьера, а также вы-
сокий кислотно-пептический фактор. Причинами гиперсекреции соляной кислоты являются гиперплазия париетальных клеток, повидимому, генетически обусловленная ваготония и гиперпродукция гастрина. Известно, что главные стимуляторы секреции НСb - гистамин, гастрин, ацетилхолин. Кроме того, известно, что недостаточная выработка глюкагона и особенно соматостатина также способствует язвообразованию (рис. 17-4).
Патогенетическим фактором в реализации болезни, наряду с высоким кислотно-пептическим фактором, является гастродуоденальная дисмоторика. Если у здорового человека идет ритмичное поступление желудочного содержимого в ДПК - 3 сокращения в 1 мин, то у больных язвенной болезнью в ДПК констатируются 15-минутные периоды низкого уровня рН. Высокая кислотность не может поддерживать нормальную перистальтику, происходит «закисление» ДПК. Длительный контакт кислого содержимого со слизистой ведет к язвообразованию. «Закисление» ДПК нередко связано с дискинезией и снижением ее ощелачивающей функции в связи с нарушением выработки бикарбонатов панкреатического и билиарного секретов.
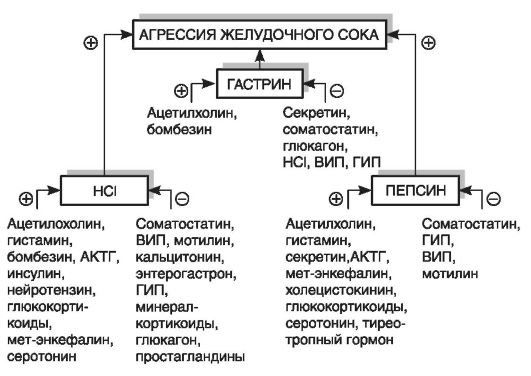 Рис. 17-4. Факторы, стимулирующие и ингибирующие агрессию желудочного сока (по Г.Е. Самониной, 1997). АКТГ - адренокортикотропный гормон, ВИП - вазоактивный интестинальный полипептид, ГИП - гастринингибирующий пептид
Рис. 17-4. Факторы, стимулирующие и ингибирующие агрессию желудочного сока (по Г.Е. Самониной, 1997). АКТГ - адренокортикотропный гормон, ВИП - вазоактивный интестинальный полипептид, ГИП - гастринингибирующий пептид
Определенное значение в развитии язвенной болезни придается дуоденогастральному рефлюксу (ДГР) - забросу желчи (желчных кислот) в желудок. Желчь, воздействуя на слизистую желудка, приводит к нарушению слизистого барьера и к повышению кислотнопептических свойств желудочного сока из-за стимуляции эндокринного аппарата желудка (прежде всего усиливается выработка гастрина). Дискинезия ДПК, особенно по гипомоторному типу, понижение тонуса антрального отдела желудка способствуют ДГР, делают его продолжительным и интенсивным. Доказано, что ДГР встречается значительно чаще при сочетании язвенной болезни с заболеваниями гепатобилиарной системы, особенно с желчекаменной болезнью.
К факторам «агрессии» относят нарушение дуоденального тормозного механизма (недостаточную выработку в ДПК секретина, холецистокинина, энтерогастрона), нарушение обмена биогенных аминов - гистамина и серотонина, выделяющихся в основном из энтерохромафинных клеток слизистой оболочки желудка. Гистамин стимулирует секрецию НС1 через Н2-рецепторы, связанные с цАМФ. В период обострения язвенной болезни процессы синтеза гистамина обычно усиливаются, что влечет за собой появление свободного гистамина в крови. По одной из гипотез, гистамин выполняет роль медиатора парасимпатической нервной системы. Согласно другой широко распространенной точке зрения, гистамин является промежуточным звеном в реализации действия гастрина на секреторные клетки. Изменяется капиллярное кровообращение, повышается проницаемость сосудистой стенки, усиливается выработка пепсина (гистамин - мощный стимулятор главных клеток). Гистамин и серотонин, выполняя роль активаторов кининовой системы (активируют брадикинин), вызывают значительные расстройства микроциркуляции, страдает кровообращение и трофика слизистой оболочки желудка. В норме биогенные амины обезвреживаются за счет аминооксидаз кишечной стенки.
Защитный барьер слизистой оболочки желудка состоит из трех частей: 1) надэпителиальной (слизь, бикарбонаты); 2) эпителиальной (клетки эпителия и их репарация, простагландины, гормоны роста); 3) субэпителиальной (кровоснабжение, микроциркуляция).
Слизистая желудка постоянно подвергается воздействию соляной кислоты, пепсина, а при дуоденогастральном рефлюксе - и воздействию желчных кислот, панкреатических ферментов. В защитном барьере желудка первой линией защиты от повреждающих
факторов являются клетки слизистой оболочки. Это поверхностные клетки и секреторные добавочные, секретирующие слизь и бикарбонаты. За счет этих веществ создается физико-химический барьер, который представляет собой гель, поддерживающий рН нейтральной среды у поверхности эпителия. Все поверхностные эпителиальные клетки, выстилающие желудок и ДПК, синтезируют и секретируют бикарбонаты (рис. 17-5). Слизистая проксимальной части ДПК вырабатывает бикарбонатов в 2 раза больше, чем вся слизистая желудка. Важная роль в поддержании базального уровня секреции бикарбонатов и слизи отводится и эндогенным простагландинам. Слизь, ее нерастворимая фракция, бикарбонаты защищают слизистую оболочку желудка от воздействия соляной кислоты и пепсина. Слизистый барьер предотвращает обратную диффузию Н+ из просвета желудка в кровь. Длительный же контакт слизистой с кислой средой и изменения в составе слизи (в период обострения язвенной болезни в слизи уменьшается содержание сиаловых кислот и гликопротеидов, нейтрализующих соляную кислоту) ведут к прорыву слизистого барьера и возникновению обратной диффузии ионов водорода. В ответ на это высвобождается гистамин из тучных клеток (тканевые базофилы желудка) и рефлекторно возбуждается холинергическая система, отмечаются
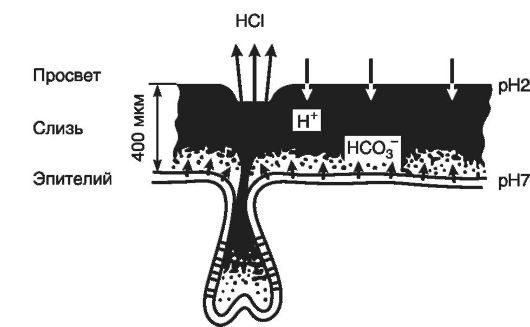 Рис. 17-5. Диаграмма, иллюстрирующая предполагаемый слизебикарбонатный барьер. Ионы НСО3, секретируемые в слой слизи, нейтрализуют медленно диффундирующие к эпителию Н+. Эта зона позволяет небольшому количеству бикарбонатов предохранять слизистую оболочку от большого количества кислоты в просвете (по L. Turberg, 1985)
Рис. 17-5. Диаграмма, иллюстрирующая предполагаемый слизебикарбонатный барьер. Ионы НСО3, секретируемые в слой слизи, нейтрализуют медленно диффундирующие к эпителию Н+. Эта зона позволяет небольшому количеству бикарбонатов предохранять слизистую оболочку от большого количества кислоты в просвете (по L. Turberg, 1985)
венозный стаз, переполнение капилляров, усиливается продукция соляной кислоты и пепсина - все это способствует образованию пептической язвы.
В поддержании устойчивости слизистой оболочки желудка и ДПК к факторам агрессии важную роль играют способность клеток к быстрому обновлению (репарация), хорошее состояние кровообращения и секреция химических медиаторов защиты (простагландины, гормон роста). Известно, что слизистая оболочка желудка и ДПК после повреждения обычно быстро восстанавливается (в течение 15-30 мин). Этот процесс идет не за счет деления клеток, а в результате движения их из покровно-ямочного эпителия желудка вдоль базальной мембраны и закрытия дефекта в участке поврежденного эпителия. Простагландины, особенно простагландин Е2, способствуют повышению защитных свойств слизистой оболочки желудка, так как угнетают активность париетальных клеток, стимулируют секрецию слизи и бикарбонатов и улучшают кровоснабжение слизистой оболочки, снижая обратную диффузию ионов водорода и ускоряя регенерацию. Секреция их осуществляется главными, добавочными и париетальными клетками слизистой оболочки желудка.
Субэпителиальная часть защитного барьера слизистой оболочки желудка включает в себя оптимальное кровоснабжение и микроциркуляцию.
Кроме того, к факторам «защиты» относят щелочную реакцию слюны, панкреатического сока, желчи; оптимальную моторику и эвакуацию желудка; а также механизм дуоденального торможения кислото- и пепсинообразования (выработка холецистокинина, секретина, энтерогастона двенадцатиперстной кишкой).
Когда факторы «агрессии» перевешивают на чаше весов, формируется язва, она становится очагом афферентной импульсации в ЦНС, где возникает патологическая доминанта. В процесс вовлекаются другие органы и системы организма (печень, поджелудочная железа и т.д.), болезнь становится хронической (рис. 17-6).
Клиника язвенной болезни включает болевой синдром, который характеризуется периодичностью (зависит от приема пищи, «голодные» боли), сезонностью (обострения весной и осенью), ритмичностью (ночные, дневные - от суточных ритмов выделения желудочно-кишечных соков). Болевой синдром является ведущим субъективным проявлением болезни в фазе обострения. Синдром диспепсических расстройств характеризуется изжогой, отрыжкой,
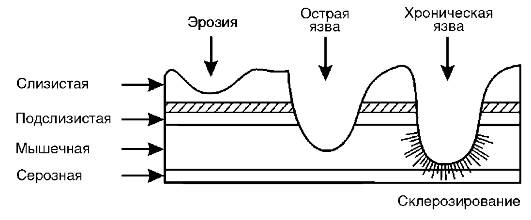 Рис. 17-6. Острые и хронические повреждения оболочек, составляющих стенки желудка и тонкого кишечника (по Brooks, 1985)
Рис. 17-6. Острые и хронические повреждения оболочек, составляющих стенки желудка и тонкого кишечника (по Brooks, 1985)
нередко срыгиванием с саливацией. Аппетит остается хорошим, при дуоденальных язвах даже увеличивается (болезненнное чувство голода). Запоры возникают у 50% больных, беспокоят даже больше, чем болевые ощущения.
К осложнениям язвенной болезни относятся кровотечения (малое - до 500 мл, среднее - до 1000 мл, большое - до 1500 мл, массивное - более 1500 мл), постгеморрагическая анемия (легкая, средняя, тяжелая), пенетрация (в малый сальник, желудочноободочную, печеночно-двенадцатиперстную связку, поджелудочную железу, поперечно-ободочную кишку, печень, желчный пузырь и т.д.), перфорация (в свободную брюшную полость, полость малого сальника), стеноз (компенсированный, субкомпенсированный, декомпенсированный), малигнизация (характерна для язвенной болезни желудка, язвенная болезнь двенадцатиперстной кишки не озлокачествляется), реактивный гепатит, реактивный панкреатит, перивисцерит (перигастрит, перидуоденит).
Исходы язвенной болезни: рубцевание и заживление; стеноз привратника и деформация желудка в результате рубцевания; пожизненное существование язвенной болезни; малигнизация; летальный исход обычно в результате кровотечения или перфорации.
Экспериментальные язвы желудка. Для воспроизведения язвы желудка в эксперименте наиболее часто используются следующие методы:
1. Повреждение слизистой желудка физическими и химическими раздражителями (горячая вода, ляпис, кислоты, кротоновое масло и др.). В стенке желудка развивается острое воспаление и
происходит образование язвенных дефектов, которые обычно быстро заживают.
2. Нарушение кровообращения в стенке желудка или ДПК (перевязка, эмболия, склерозирование сосудов). Кровоток обычно восстанавливается за счет анастомозов, и образующиеся язвы быстро заживают.
3. Длительное введение лекарств, усиливающих желудочную секрецию (атофан, гистамин, пентагастрин, пилокарпин и др.), с последующим образованием язвенного дефекта.
4. Хроническое раздражение n. vagus с усилением желудочной секреции и нарушением микроциркуляции в стенке желудка.
5. Экспериментальные неврозы с дополнительным введением желудочного сока. У собак язвы желудка возникали при сочетании срыва высшей нервной деятельности с ежедневным двухчасовым орошением слизистой желудка желудочным соком.
6. Наложение лигатуры на привратник с сохранением его проходимости (метод Шейя). При этом в желудке крыс через 1-2 суток появлялись эрозии и иногда язвы вследствие сдавления сосудов и раздражающего воздействия лигатуры на n. vagus, что вызывало значительное нарушение кровообращения.
7. Введение гастроцитотоксической сыворотки, полученной путем иммунизации животных-доноров гомогенатом ткани желудка. Например, кролика иммунизируют тканью желудка собаки и полученную сыворотку, содержащую противожелудочные антитела, вводят внутривенно интактной собаке-реципиенту. Антитела взаимодействуют с тканью желудка животного-реципиента и вызывают повреждение этой ткани в результате реакции антиген-антитело.
Описанные методы экспериментального моделирования язв вызывают в основном острые язвенные дефекты. По механизму возникновения и особенностям течения (обычно быстро заживают) они принципиально отличаются от язвенной болезни, больше воспроизводя картину симптоматических язв человека. Однако частично удается моделировать отдельные проявления этого заболевания, что ориентирует в разрабатываемой противоязвенной терапии.






