Мета: з’ясування особливості дії природних антиоксидантів, визначити в експерименті концентрацію аскорбінової кислоти
Основні поняття: біоантиоксиданти, вітаміни, ферменти
Питання для теоретичної підготовки:
- Аскорбінова кислота
- Вітамін Е
- Каротиноїди
- Вітаміни А, К, кретиноїди
- Фенольні сполуки
- Показники ПАС в організмі
Хід роботи:
Принцип методу: даний метод заснований на екстракції дегідроаскорбінової кислоти (ДАК) та аскорбінової кислоти (АК) за допомогою трихлороцтової кислоти (ТХО), окисненні АК до ДАК за допомогою 2,6-дихлорфеноліндофеноляту натрію (2,6-ДХФІФ), визначенні суми (АК+ДАК) та ДАК. Вміст АК визначається за різницею (АК+ДАК)-ДАК. ДАК при реакції з 2,4-динітрофенілгідразином (2,4-ДНФГ) утворює забарвлений продукт, який фотометрується.
Хід визначення: готували центрифужні пробірки по кількості проб та стільки ж центрифужних пробірок для 6% розчину ТХО. У центрифужні пробірки наливали по 10 мл 6% ТХО. Наважку серця 0,2 г розтирали у ступці, добавляли спочатку 2-3 краплі ТХО із набраної пробірки, продовжували розтирати, поступово додаючи невеликі порції ТХО. Переносили вміст ступки у пусту центрифужну пробірку, добавляли, змиваючи ступку, залишок з 6% ТХО. Таким чином, у пробірці виявилася розтерта наважка та 10 мл 6% ТХО. Гомогенат центрифугували при 3000 об/хв. 10 хв. Для кожної проби готували 4 хімічні пробірки та дві пробірки для контролю (загальні для всіх проб). Пробірки 1, 2 – паралелі для сумарного визначення ДАК+АК. Пробірки 3, 4 – для визначення ДАК. В усі пробірки приливали по 2 мл центрифугату, у контроль – 2 мл 6% ТХО. У 1, 2 пробірки додавали по 0,05 мл 0,2% дихлорфеноліндофеноляту натрію (ДХФІФ) для окиснення АК до ДАК. В усі 4 пробірки додавали по 0,1 мл 5% розчину тіосечовини у 6% ТХО (проби знебарвлювалися). У 3, 4 пробірки додавали по 1 краплі 0,2% ДХФІФ. В усі пробірки (крім “контроль”) додавали по 0,5 мл 2,4-ДНФГ. Всі пробірки інкубували у термостаті 3 години при 37°С. Після інкубації пробірки охолоджували за допомогою льоду, у кожну пробірку обережно, по стінках приливали 2,5 мл 85% сірчаної кислоти. У пробу “контроль” приливали 0,5 мл 2,4-ДНФГ (2 г у 100 мл 9 н сірчаної кислоти). Після додавання сірчаної кислоти витримували 1 год. Коли розчин набував жовто-червоного кольору, проби фотометрували при 540 нм у кюветі 10 мм проти контрольної проби. Екстинкцію АК визначали як різницю 3, 4 пробірок та 1, 2 пробірок: Е(АК)=Е(ДАК+АК)-Е(ДАК). Вміст АК визначали за калібрувальною кривою (5-30 мкг АК у 2 мл). При прямій пропорційній залежності концентрація–екстинкція знаходили коефіцієнт пропорційності К.
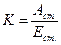
де: Аст – вміст АК у стандартному розчині, мкг (кожна крапка графіку);
Ест – екстинкція, яка відповідна стандартному розчину.
Розрахунок:
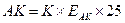
де: АК – вміст аскорбінової кислоти у тканині, мкг/г (мг/кг);
К – вміст аскорбінової кислоти на одиницю екстинкції;
ЕАК – екстинкція аскорбінової кислоти у колориметруємої пробі;
25 – коефіцієнт перерахунку на г тканини (0,2 г: 5=0,04 г – наважка тканини, що бере участь у замірі екстинкції: 1: 0,04=25).
Коефіцієнт переводу у систему СІ 56,7859.
Контрольні питання:
1.Природні антиоксиданти
2. вітамін А
3. Вплив вітаміну Е на атеросклероз
1. Поліфеноли як потужні антиоксиданти
2. Вітамін Е
3. Антиоксидантні вітаміни і серцево-судинна хвороба
1. Антиоксиданти прямої та непрямої дії
2. Вітамін К
3. Вплив вітаміну С на перебіг хвороб
Тестові питання:
1. Вітамін С:
а) впливає на ріст






