58. Реакция протекает по схеме 2А+3В =С. Концентрация А уменьшилась на 0,1 моль/л. Как при этом изменятся концентрации веществ В и С?
59. Начальные концентрации веществ, участвующих в реакции
СО+Н2О = СО2 +Н2,
были равны (моль/л, слева на право): 0,3; 0,4; 0,4; 0,05. Каковы концентрации всех веществ в момент, когда прореагировала половина от начальной концентрации СО?
60. Начальные концентрации веществ, участвующих в реакции
N2+3H2 = 2NH3,
равны (моль/л, слева на право): 0,2; 0,3; 0. Каковы концентрации азота и водорода в момент, когда концентрация аммиака станет равной 0,1 моль/л?
61. Во сколько раз изменится скорость реакции 2А + В 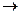 С, если концентрацию вещества А увеличить в 2 раза, а концентрацию вещества В уменьшить в 3 раза?
С, если концентрацию вещества А увеличить в 2 раза, а концентрацию вещества В уменьшить в 3 раза?
62. Через некоторое время после начала реакции 3А + В 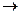 2С +D концентрации веществ составляли (моль/л, слева на право): 0,03; 0,01; 0,008. Каковы исходные концентрации веществ А и В?
2С +D концентрации веществ составляли (моль/л, слева на право): 0,03; 0,01; 0,008. Каковы исходные концентрации веществ А и В?
63. В системе СО + СI2 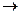 CОCI2 концентрацию СО увеличивали от 0,03 до 0,12 моль/л, а концентрацию хлора – от 0,02 до 0,06 моль/л. Во сколько раз возросла скорость прямой реакции?
CОCI2 концентрацию СО увеличивали от 0,03 до 0,12 моль/л, а концентрацию хлора – от 0,02 до 0,06 моль/л. Во сколько раз возросла скорость прямой реакции?
64. Начальные концентрации веществ А и В в реакции А+2В 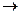 С были равны 0,03 и 0,05 моль/л соответственно. Константа скорости реакции равна 0,4. Найти начальную скорость реакции и скорость по истечении некоторого времени, когда концентрация вещества А уменьшится на 0,01 моль/л.
С были равны 0,03 и 0,05 моль/л соответственно. Константа скорости реакции равна 0,4. Найти начальную скорость реакции и скорость по истечении некоторого времени, когда концентрация вещества А уменьшится на 0,01 моль/л.
65. Как изменится скорость реакции 2NO + O2 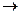 2NO2, если: а) увеличить давление в системе в 3 раза; б) уменьшить объем системы в 3 раза?
2NO2, если: а) увеличить давление в системе в 3 раза; б) уменьшить объем системы в 3 раза?
66. Во сколько раз следует увеличить концентрацию вещества В в системе 2А + В 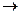 А2В, чтобы при уменьшении концентрации вещества А в 4 раза скорость прямой реакции не изменилась?
А2В, чтобы при уменьшении концентрации вещества А в 4 раза скорость прямой реакции не изменилась?
67. Во сколько раз следует увеличить концентрацию оксида углерода (II) в системе 2СО 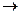 СО2 + С, чтобы скорость реакции увеличилась в 100 раза? Как изменится скорость реакции при увеличении давления в 5 раз?
СО2 + С, чтобы скорость реакции увеличилась в 100 раза? Как изменится скорость реакции при увеличении давления в 5 раз?
68. Начальные концентрации веществ в реакции СО + Н2О 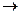 СО2 + Н2 были равны (моль/л, слева на право): 0,05; 0,06; 0,4 и 0,2. Вычислить концентрации всех участвующих в реакции веществ после того, как прореагировала 60% воды.
СО2 + Н2 были равны (моль/л, слева на право): 0,05; 0,06; 0,4 и 0,2. Вычислить концентрации всех участвующих в реакции веществ после того, как прореагировала 60% воды.
69. При повышении температуры на 600С скорость реакции увеличилась в 4000 раз. Вычислить температурный коэффициент скорости реакции.
70. Сколько времени потребуется для завершения реакции при 180 С, если при 900С она завершается за 20 секунд, а температурный коэффициент скорости реакции равен 3,2?
71. При 100С реакция заканчивается за 95 с, а при 200С за 60с. Вычислить энергию активации.
72. Во сколько раз возрастет скорость реакции при повышении температуры с 300 до 500С, если энергия активации равна 125,5 кДж/моль?
73. Каково значение энергии активации реакции, скорость которой при 300 К в 10 раз больше, чем при 280 К?
74. Чему равна энергия активации реакции, если при повышении температуры от 290 до 300 К скорость ее увеличится в 2 раза?
75. Энергия активации некоторой реакции равна 100 кДж/моль. Во сколько раз изменится скорость реакции при повышении температуры от 27 до 370С?
76. При 1500С некоторая реакция заканчивается за 16 минут. Принимая температурный коэффициент скорости за 2,5 рассчитать, через какое время закончится эта реакция, если проводить её: а) при 2000 С, б) при 800С?
77. При какой температуре реакция закончится за 45 минут, если при 293К на это требуется 3 часа? Температурный коэффициент скорости реакции равен 3,2.
78. Энергия активации реакции NO2 = NO + 1/2O2 равна 103,5 кДж/моль. Константа скорости этой реакции при 298К равна 2,03∙104 с-1. Вычислить константу скорости этой реакции при 288 К.
79. Реакция CO + CI2 ⇆ COCI2 протекает в объеме 10 литров. Состав равновесной смеси: 14г СО; 35,6г CI2; и 49,5г СOCI2. Вычислить константу равновесия реакции.
80. Константа равновесия реакции FeO + CO ⇆ Fe + CO2 при некоторой температуре равна 0,5. Найти равновесные концентрации СО и СО2, если начальные концентрации этих веществ составляли (моль/л): 0,05 для СО и 0,01 для CO2.
81. Найти константу равновесия реакции N2O4 ⇆ 2NO2, если начальная концентрация N2O4 составляет 0,08моль/л, а к моменту наступления равновесия продиссоциировало 50% N2O4.
82. Константа равновесия реакции А+В⇆С+D равна единице. Начальная концентрация вещества А равна 0,02моль/л. Сколько процентов А подвергнется превращению, если начальные концентрации В, С и D равны соответственно 0,02; 0,1 и 0,2 моль/л?
83. В начальный момент реакции синтеза аммиака концентрации были равны (моль/л): 1,5 для N2; 2,5 для H2 и 0 для NH3. Какова концентрация азота и водорода при концентрации аммиака 0,15 моль/л?
84. Равновесие в системе H2+I2⇆2HI установилось при следующих концентрациях (моль/л): [H2] = 0,025; [I2] = 0,005; [HI] = 0,09. Определить исходные концентрации йода и водорода, если в начальный момент реакции концентрация HI равнялась нулю.
85. Оксид углерода (II) и хлор были помещены в закрытый сосуд при постоянной температуре. Начальные их концентрации равны 1 моль/л, давление в сосуде 101325 Па. В результате реакции CO + Cl2⇆COCl2 к моменту равновесия осталось 50% СО. Каково давление в сосуде при равновесии?
86. Как изменится давление при наступлении равновесия в реакции синтеза аммиака в закрытом сосуде при постоянной температуре, если начальные концентрации азота и водорода составляют соответственно 2 и 6 моль/л и если равновесие наступит тогда, когда прореагирует 10% первоначального количества азота?
87. После смешения газов А и В в системе А + В⇆С + D устанавливается равновесие при следующих концентрациях (моль/л): [B] = 0,05; [C] = 0,02. Константа равновесия реакции равна 4∙103. Найти исходные концентрации А и В.






