См Алканов Алкенов и Алкинов…Там всё есть)))
Вопрос 16. Гомологи бензола. Номенклатура и изомерия \ Гомологи бензола – соединения, образованные заменой одного или нескольких атомов водорода в молекуле бензола на углеводородные радикалы (R):
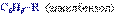
 Общая формула гомологического ряда бензола
Общая формула гомологического ряда бензола  Номенклатура. Широко используются тривиальные названия (толуол, ксилол, кумол и т.п.). Систематические названия строят из названия углеводородного радикала (приставка) и слова бензол (корень):
Номенклатура. Широко используются тривиальные названия (толуол, ксилол, кумол и т.п.). Систематические названия строят из названия углеводородного радикала (приставка) и слова бензол (корень): 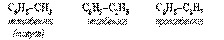 Если радикалов два или более, их положение указывается номерами атомов углерода в кольце, с которыми они связаны. Нумерацию кольца проводят так, чтобы номера радикалов были наименьшими. Например:
Если радикалов два или более, их положение указывается номерами атомов углерода в кольце, с которыми они связаны. Нумерацию кольца проводят так, чтобы номера радикалов были наименьшими. Например: 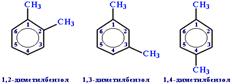 Для дизамещенных бензолов R-C6H4-R используется также и другой способ построения названий, при котором положение заместителей указывают перед тривиальным названием соединения приставками:
Для дизамещенных бензолов R-C6H4-R используется также и другой способ построения названий, при котором положение заместителей указывают перед тривиальным названием соединения приставками:
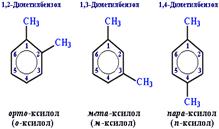
орто - (о -) заместители у соседних атомов углерода кольца, т.е. 1,2-;
мета - (м -) заместители через один атом углерода (1,3-);
пара - (п -) заместители на противоположных сторонах кольца (1,4-).
 Ароматические одновалентные радикалы имеют общее название " арил ".
Ароматические одновалентные радикалы имеют общее название " арил ".
Из них наиболее распространены в номенклатуре органических соединений два: C6H5- (фенил) и C6H5CH2 - (бензил). Изомерия (структурная):
1) положения заместителей для ди -, три - и тетра -замещенных бензолов (например, о -, м - и п -ксилолы);
2) углеродного скелета в боковой цепи, содержащей не менее 3-х атомов углерода:

3) изомерия заместителей R, начиная с R = С2Н5.
Например, молекулярной формуле С8Н10 соответствует 4 изомера:
три ксилола CH3-C6H4-CH3 (о-, м-, п-) и этилбензол C6H5-C2H5. Пространственная изомерия относительно бензольного кольца в алкилбензолах отсутствует. Замещение в алкилбензолах
Гомологи бензола (алкилбензолы) С6Н5–R более активно вступают в реакции замещения по сравнению с бензолом. Например, при нитровании толуола С6Н5CH3 (70°С) происходит замещение не одного, а трех атомов водорода с образованием 2,4,6-тринитротолуола:
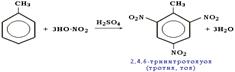 При бромировании толуола также замещаются три атома водорода:
При бромировании толуола также замещаются три атома водорода:
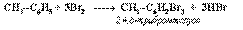 Здесь ярко проявляется взаимное влияние атомов в молекуле на реакционную способность вещества. С одной стороны, метильная группа СH3 (за счет + I -эффекта) повышает электронную плотность в бензольном кольце в положениях 2,4 и 6:
Здесь ярко проявляется взаимное влияние атомов в молекуле на реакционную способность вещества. С одной стороны, метильная группа СH3 (за счет + I -эффекта) повышает электронную плотность в бензольном кольце в положениях 2,4 и 6: 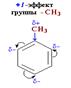 и облегчает замещение именно в этих положениях. Взаимное влияние атомов определяет направление реакций электрофильного замещения в гомологах бензола и его производных – правила ориентации. С другой стороны, под влиянием бензольного кольца метильная группа СH3 в толуоле становится более активной в реакциях окисления и радикального замещения по сравнению с метаном СH4 (раздел 2.5.5). Толуол, в отличие от метана, окисляется в мягких условиях (обесцвечивает подкисленный раствор KMnO4 при нагревании):
и облегчает замещение именно в этих положениях. Взаимное влияние атомов определяет направление реакций электрофильного замещения в гомологах бензола и его производных – правила ориентации. С другой стороны, под влиянием бензольного кольца метильная группа СH3 в толуоле становится более активной в реакциях окисления и радикального замещения по сравнению с метаном СH4 (раздел 2.5.5). Толуол, в отличие от метана, окисляется в мягких условиях (обесцвечивает подкисленный раствор KMnO4 при нагревании):
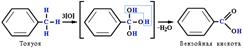
Легче, чем в алканах, протекают реакции радикального замещения в боковой цепи алкилбензолов:  Это объясняется тем, что на лимитирующей стадии легко (при невысокой энергии активации) образуется радикал бензил ·CH2-C6H5. Он более стабилен, чем алкильные свободные радикалы (·СН3, ·СH2R), т.к. его неспаренный электрон делокализован за счет взаимодействия с p-электронной системой бензольного кольца.
Это объясняется тем, что на лимитирующей стадии легко (при невысокой энергии активации) образуется радикал бензил ·CH2-C6H5. Он более стабилен, чем алкильные свободные радикалы (·СН3, ·СH2R), т.к. его неспаренный электрон делокализован за счет взаимодействия с p-электронной системой бензольного кольца.
Вопрос. 17Спирты Спирты - соединения алифатического ряда, содержащие одну или несколько гидроксильных групп. Общая формула спиртов с одной гидроксигруппой R–OH. Классификация спиртов Спирты классифицируют по различным структурным признакам.
1. По числу гидроксильных групп спирты подразделяются на
o одноатомные (одна группа -ОН),
o многоатомные (две и более групп -ОН).
Современное название многоатомных спиртов - полиолы (диолы, триолы и т.д). Примеры:
o двухатомный спирт – этиленгликоль(этандиол)
HO–СH2–CH2–OH
o трехатомный спирт – глицерин(пропантриол-1,2,3)
HO–СH2–СН(ОН)–CH2–OH
Двухатомные спирты с двумя ОН-группами при одном и том же атоме углерода R–CH(OH)2 неустойчивы и, отщепляя воду, сразу же превращаются в альдегиды R–CH=O. Спирты R–C(OH)3 не существуют.
2. В зависимости от того, с каким атомом углерода связана гидроксигруппа, различают спирты
o первичные R–CH2–OH,
o вторичные R2CH–OH,
o третичные R3C–OH.
Например: 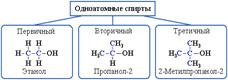 В многоатомных спиртах различают первично-, вторично- и третичноспиртовые группы. Например, молекула трехатомного спирта глицерина содержит две первичноспиртовые (HO–СH2–) и одну вторичноспиртовую (–СН(ОН)–) группы.
В многоатомных спиртах различают первично-, вторично- и третичноспиртовые группы. Например, молекула трехатомного спирта глицерина содержит две первичноспиртовые (HO–СH2–) и одну вторичноспиртовую (–СН(ОН)–) группы.
3. По строению радикалов, связанных с атомом кислорода, спирты подразделяются на
o предельные, или алканолы (например, СH3CH2–OH)
o непредельные, или алкенолы (CH2=CH–CH2–OH)
o ароматические (C6H5CH2–OH).
Непредельные спирты с ОН-группой при атоме углерода, соединенном с другим атомом двойной связью, очень неустойчивы и сразу же изомеризуются в альдегиды или кетоны. Например, виниловый спирт CH2=CH–OH превращается в уксусный альдегид CH3–CH=O Номенклатура спиртов Систематические названия даются по названию углеводорода с добавлением суффикса -ол и цифры, указывающей положение гидроксигруппы (если это необходимо). Например: 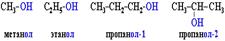 Нумерация ведется от ближайшего к ОН-группе конца цепи. Цифра, отражающая местоположение ОН-группы, в русском языке обычно ставится после суффикса "ол". Это разгружает словесную часть названия от цифр (например, 2-метилбутанол-1). В англоязычной литературе цифру ставят перед названием главной цепи: 2-метил-2-бутанол. Правила IUPAC разрешают учитывать особенности национального языка. По другому способу названия спиртов производят от названий радикалов с добавлением слова " спирт ". В соответствии с этим способом приведенные выше соединения называют: метиловый спирт, этиловый спирт, н -пропиловый спирт, изопропиловый спирт. Изомерия спиртов Для спиртов характерна структурная изомерия: · изомерия положения ОН-группы (начиная с С3);
Нумерация ведется от ближайшего к ОН-группе конца цепи. Цифра, отражающая местоположение ОН-группы, в русском языке обычно ставится после суффикса "ол". Это разгружает словесную часть названия от цифр (например, 2-метилбутанол-1). В англоязычной литературе цифру ставят перед названием главной цепи: 2-метил-2-бутанол. Правила IUPAC разрешают учитывать особенности национального языка. По другому способу названия спиртов производят от названий радикалов с добавлением слова " спирт ". В соответствии с этим способом приведенные выше соединения называют: метиловый спирт, этиловый спирт, н -пропиловый спирт, изопропиловый спирт. Изомерия спиртов Для спиртов характерна структурная изомерия: · изомерия положения ОН-группы (начиная с С3);
например:
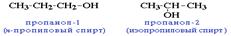
· углеродного скелета (начиная с С4);
например, формуле C4H9OH соответствует 4 структурных изомера:

· межклассовая изомерия с простыми эфирами
(например, этиловый спирт СН3CH2–OH и диметиловый эфир CH3–O–CH3). Возможна также пространственная изомерия - оптическая (зеркальная)
Например, бутанол-2 СH3CH(OH)СH2CH3, в молекуле которого второй атом углерода (выделен цветом) связан с четырьмя различными заместителями, существует в форме двух зеркальных изомеров. Таким образом, формуле C4H9OH соответствует 5 изомерных спиртов (4 структурных изомера и один из них - бутанол-2 - в виде двух зеркальных изомеров).
Получение спиртов
1. Щелочной гидролиз галогеноуглеводородов:
CH3–Br + NaOH (водн.) ® CH3–OH + NaBr
ClCH2–CH2Cl + 2 NaOH (водн.) ® HOCH2–CH2OH + 2NaCl
C6H5Cl + NaOH (P, 340°С) ® C6H5OH + NaCl
2. Гидратация алкенов:
CH2=CH2 + H2O (кат.) ® CH3CH2OH
Присоединение воды к несимметричным алкенам идет по правилу Морковников с образованием вторичных и третичных спиртов:
CH3–CH=CH2 + H2O (кат.) ® CH3CH(OH)CH3
(CH3)2C=CH2 + H2O (кат.) ® (CH3)3C–OH физические свойства
Следствием полярности связи О–Н и наличия неподеленных пар электронов на атоме кислорода является способность гидроксисоединений к образованию водородных связей 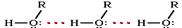 Ассоциация молекул ROH Это объясняет, почему даже низшие спирты - жидкости с относительно высокой температурой кипения (т.кип. метанола +64,5°С). При переходе от одноатомных к многоатомным спиртам или фенолам температуры кипения и плавления резко возрастают.Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде:
Ассоциация молекул ROH Это объясняет, почему даже низшие спирты - жидкости с относительно высокой температурой кипения (т.кип. метанола +64,5°С). При переходе от одноатомных к многоатомным спиртам или фенолам температуры кипения и плавления резко возрастают.Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде: 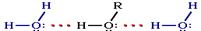 Гидратация молекул ROH Способность растворяться в воде уменьшается с увеличением углеводородного радикала и от многоатомных гидроксисоединений к одноатомным. Метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин смешиваются с водой в любых соотношениях. Химические свойства гидроксисоединений В химических реакциях гидроксисоединений возможно разрушение одной из двух связей: · С–ОН с отщеплением ОН-группы · О–Н с отщеплением водорода. Это могут быть реакции замещения, в которых происходит замена ОН или Н, или реакция отщепления (элиминирования), когда образуется двойная связь. Полярный характер связей С–О и О–Н способствует гетеролитическому их разрыву и протеканию реакций по ионному механизму. При разрыве связи О–Н с отщеплением протона Н+ проявляются кислотные свойства гидроксисоединения, а при разрыве связи С–О - свойства основания и нуклеофильного реагента.
Гидратация молекул ROH Способность растворяться в воде уменьшается с увеличением углеводородного радикала и от многоатомных гидроксисоединений к одноатомным. Метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин смешиваются с водой в любых соотношениях. Химические свойства гидроксисоединений В химических реакциях гидроксисоединений возможно разрушение одной из двух связей: · С–ОН с отщеплением ОН-группы · О–Н с отщеплением водорода. Это могут быть реакции замещения, в которых происходит замена ОН или Н, или реакция отщепления (элиминирования), когда образуется двойная связь. Полярный характер связей С–О и О–Н способствует гетеролитическому их разрыву и протеканию реакций по ионному механизму. При разрыве связи О–Н с отщеплением протона Н+ проявляются кислотные свойства гидроксисоединения, а при разрыве связи С–О - свойства основания и нуклеофильного реагента.  Таким образом, гидроксисоединения могут вступать в многочисленные реакции, давая различные классы соединений. Вследствие доступности гидроксисоединений, в особенности спиртов, каждая из этих реакций является одним из лучших способов получения определенных соединений. Реакции по связи О–Н К наиболее характерным реакциям гидроксисоединений, идущим с разрывом связи О–Н, относятся: · реакции замещения атома водорода на металл (кислотные свойства);· реакции замещения атома водорода на остаток кислоты (образование сложных эфиров); · реакции отщепления водорода при окислении и дегидрировании. Легкость этих реакций и строение образующихся продуктов зависят от строения углеводородного радикала и взаимного влияния атомов. Реакционная способность одноатомных спиртов в реакциях по связи О–Н: CH3OH > первичные > вторичные > третичные. Если в многоатомных спиртах ОН-группы находятся при соседних атомах углерода, то вследствие взаимного влияния этих групп (– I -эффект одной ОН-группы по отношению к другой), разрыв связи О-Н происходит легче, чем в одноатомных спиртах.
Таким образом, гидроксисоединения могут вступать в многочисленные реакции, давая различные классы соединений. Вследствие доступности гидроксисоединений, в особенности спиртов, каждая из этих реакций является одним из лучших способов получения определенных соединений. Реакции по связи О–Н К наиболее характерным реакциям гидроксисоединений, идущим с разрывом связи О–Н, относятся: · реакции замещения атома водорода на металл (кислотные свойства);· реакции замещения атома водорода на остаток кислоты (образование сложных эфиров); · реакции отщепления водорода при окислении и дегидрировании. Легкость этих реакций и строение образующихся продуктов зависят от строения углеводородного радикала и взаимного влияния атомов. Реакционная способность одноатомных спиртов в реакциях по связи О–Н: CH3OH > первичные > вторичные > третичные. Если в многоатомных спиртах ОН-группы находятся при соседних атомах углерода, то вследствие взаимного влияния этих групп (– I -эффект одной ОН-группы по отношению к другой), разрыв связи О-Н происходит легче, чем в одноатомных спиртах.
Многоатомные спирты с несоседними ОН-группами подобны по свойствам одноатомным спиртам (не проявляется взаимное влияние групп ОН). Кислотные свойства гидроксисоединений Одноатомные спирты реагируют с активными металлами (Na, K, Mg, Al и др), образуя соли - алкоголяты (алкоксиды): 2R–OH + 2Na ® 2RO–Na+ + H2
2C2H5OH + 2K ® 2C2H5O–K+ + H2 Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла: C2H5OК + H2O ® C2H5OH + КOH Спирты – более слабые кислоты, чем вода, т.к. алкильный радикал, проявляя + I -эффект, повышает электронную плотность на атоме кислорода и уменьшает полярность связи О–Н. Поэтому при взаимодействии спиртов со щелочами алкоголяты практически не образуются: 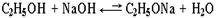 (равновесие этой реакции сдвинуто влево,
(равновесие этой реакции сдвинуто влево,
т.к. соли спиртов в воде гидролизуются) Кроме того, спирты способны вытеснять углеводороды, которые можно рассматривать как еще более слабые кислоты, из их солей (например, из реактивов Гриньяна RMgHal): R–OH + R'MgBr ® R'H + Mg(OR)Br Кислотность одноатомных спиртов убывает в ряду: CH3OH > первичный > вторичный > третичный. Многоатомные спирты с ОН-группами у соседних атомов углерода (этиленгликоль, глицерин и т.п.) вследствие взаимного влияния атомов (- I -эффект ОН-групп) являются более сильными кислотами, чем одноатомные спирты. Они образуют соли не только в реакциях с активными металлами, но и под действием их гидроксидов: HO–CH2CH2–OH + 2NaOH ® NaO–CH2CH2–ONa + 2H2O Такие спирты, в отличие от одноатомных, взаимодействуют с раствором гидроксида меди (II), образуя комплексные соединения, окрашивающие раствор в ярко-синий цвет (качественная реакция): 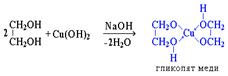 Многоатомные спирты с несоседними ОН-группами подобны по свойствам одноатомным спиртам (не проявляется взаимное влияние групп ОН). Спирты вступают в реакции с минеральными и органическими кислотами, образуя сложные эфиры. Реакция обратима (обратный процесс – гидролиз сложных эфиров).
Многоатомные спирты с несоседними ОН-группами подобны по свойствам одноатомным спиртам (не проявляется взаимное влияние групп ОН). Спирты вступают в реакции с минеральными и органическими кислотами, образуя сложные эфиры. Реакция обратима (обратный процесс – гидролиз сложных эфиров). 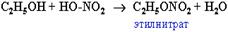
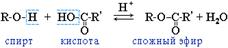 Окисление Окислители - KMnO4, K2Cr2O7+H2SO4, O2+катализатор. Легкость окисления спиртов уменьшается в ряду: первичные > вторичные > третичные. Первичные спирты при окислении образуют альдегиды, которые затем легко окисляются до карбоновых кислот.
Окисление Окислители - KMnO4, K2Cr2O7+H2SO4, O2+катализатор. Легкость окисления спиртов уменьшается в ряду: первичные > вторичные > третичные. Первичные спирты при окислении образуют альдегиды, которые затем легко окисляются до карбоновых кислот. 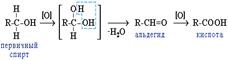 При окислении вторичных спиртов образуются кетоны.
При окислении вторичных спиртов образуются кетоны. 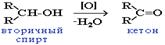 Предельное окисление происходит при горении, например: 2CH3OH + 3O2 ® 2CO2 + 4H2O Реакции по связи С–О Наиболее характерные реакции гидроксисоединений, происходящие с разрывом связи С–О: · реакция замещения OH-группы на галоген или другую нуклеофильную группу (RO-, NH2- и т.п.), идущая по механизму нуклеофильного замещения SN; · реакция отщепления (элиминирования) ОН и Н от соседних атомов углерода (внутримолекулярная дегидратация спиртов – образование алкенов); · реакция замещения группы ОН при разрыве связи С–О в одной молекуле и замещения атома Н с разрывом связи О–Н - в другой молекуле гидроксисоединения (межмолекулярная дегидратация – образование простых эфиров). Реакционная способность спиртов в реакциях по связи С-О:
Предельное окисление происходит при горении, например: 2CH3OH + 3O2 ® 2CO2 + 4H2O Реакции по связи С–О Наиболее характерные реакции гидроксисоединений, происходящие с разрывом связи С–О: · реакция замещения OH-группы на галоген или другую нуклеофильную группу (RO-, NH2- и т.п.), идущая по механизму нуклеофильного замещения SN; · реакция отщепления (элиминирования) ОН и Н от соседних атомов углерода (внутримолекулярная дегидратация спиртов – образование алкенов); · реакция замещения группы ОН при разрыве связи С–О в одной молекуле и замещения атома Н с разрывом связи О–Н - в другой молекуле гидроксисоединения (межмолекулярная дегидратация – образование простых эфиров). Реакционная способность спиртов в реакциях по связи С-О:
третичные > вторичные > первичные > CH3OH Для фенолов реакции этого типа не характерны, поскольку атом кислорода прочно связан с атомом углерода бензольного кольца за счет участия своей неподеленной электронной пары в системе сопряжения. Реакции дегидратации спиртов Отщепление воды от молекул спирта (дегидратация спиртов) в зависимости от условий происходит как внутримолекулярная или межмолекулярная реакция.
1. Внутримолекулярная дегидратация спиртов с образованием алкенов идет в присутствии концентрированной серной кислоты при нагревании выше 140 °С. Например: 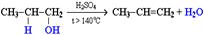
В тех случаях, когда возможны 2 направления реакции, например: 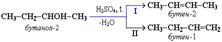 дегидратация идет преимущественно в направлении I, т.е. по правилу Зайцева– с образованием более замещенного алкена (водород отщепляется от менее гидрогенизированного атома углерода).
дегидратация идет преимущественно в направлении I, т.е. по правилу Зайцева– с образованием более замещенного алкена (водород отщепляется от менее гидрогенизированного атома углерода).
2. Межмолекулярная дегидратация спиртов происходит при температуре ниже 140 °С с образованием простых эфиров:  Применение гидроксисоединений Метанол (метиловый спирт) CH3OH · производство формальдегида, муравьиной кислоты; · растворитель. Этанол (этиловый спирт) С2Н5ОН · производство ацетальдегида, уксусной кислоты, бутадиена, простых и сложных эфиров; · растворитель для красителей, лекарственных и парфюмерных средств; · производство ликеро-водочных изделий; · дезинфицирующее средство в медицине; · горючее для двигателей, добавка к моторным топливам. Реакции замещения ОН-группы Замещение гидроксила ОН на галоген происходит в реакции спиртов с галогеноводородами в присутствии катализатора – сильной минеральной кислоты (например, конц. H2SO4). При этом спирты проявляют свойства слабых оснований.
Применение гидроксисоединений Метанол (метиловый спирт) CH3OH · производство формальдегида, муравьиной кислоты; · растворитель. Этанол (этиловый спирт) С2Н5ОН · производство ацетальдегида, уксусной кислоты, бутадиена, простых и сложных эфиров; · растворитель для красителей, лекарственных и парфюмерных средств; · производство ликеро-водочных изделий; · дезинфицирующее средство в медицине; · горючее для двигателей, добавка к моторным топливам. Реакции замещения ОН-группы Замещение гидроксила ОН на галоген происходит в реакции спиртов с галогеноводородами в присутствии катализатора – сильной минеральной кислоты (например, конц. H2SO4). При этом спирты проявляют свойства слабых оснований.  Механизм реакции –нуклеофильного замещения SN. Нуклеофил – хлорид-анион Cl:– – замещает группу HO:– Данная реакция является одним из способов получения галогеноуглеводородов. При межмолекулярной дегидратации спиртов также происходит нуклеофильное замещение: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы.
Механизм реакции –нуклеофильного замещения SN. Нуклеофил – хлорид-анион Cl:– – замещает группу HO:– Данная реакция является одним из способов получения галогеноуглеводородов. При межмолекулярной дегидратации спиртов также происходит нуклеофильное замещение: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. 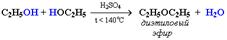 · Этиленгликоль HOCH2–CH2OH · производство пластмасс; · компонент антифризов; · сырье в органическом синтезе. Глицерин HOCH2–CH(OH)–CH2OH · фармацевтическая и парфюмерная промышленность; · смягчитель кожи и тканей; · производство взрывчатых веществ.
· Этиленгликоль HOCH2–CH2OH · производство пластмасс; · компонент антифризов; · сырье в органическом синтезе. Глицерин HOCH2–CH(OH)–CH2OH · фармацевтическая и парфюмерная промышленность; · смягчитель кожи и тканей; · производство взрывчатых веществ.
Вопрос 18. Фенолы Фенолы – гидроксисоединения, в молекулах которых ОН-группы связаны непосредственно с бензольным ядром. 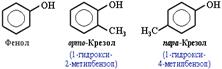 В зависимости от числа ОН-групп различают одноатомные фенолы (например, вышеприведенные фенол и крезолы) и многоатомные. Среди многоатомных фенолов наиболее распространены двухатомные:
В зависимости от числа ОН-групп различают одноатомные фенолы (например, вышеприведенные фенол и крезолы) и многоатомные. Среди многоатомных фенолов наиболее распространены двухатомные:
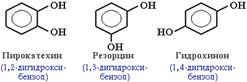
Как видно из приведенных примеров, фенолам свойственна структурная изомерия (изомерия положения гидроксигруппы).
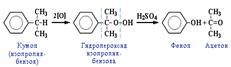
Гликоли получают окислением алкенов щелочным раствором KMnO4: 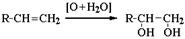 Кумольный способ получения фенола (СССР, Сергеев П.Г., Удрис Р.Ю., Кружалов Б.Д., 1949 г.). Преимущества метода: безотходная технология (выход полезных продуктов > 99%) и экономичность. В настоящее время кумольный способ используется как основной в мировом производстве фенола.
Кумольный способ получения фенола (СССР, Сергеев П.Г., Удрис Р.Ю., Кружалов Б.Д., 1949 г.). Преимущества метода: безотходная технология (выход полезных продуктов > 99%) и экономичность. В настоящее время кумольный способ используется как основной в мировом производстве фенола.
 Химические свойства гидроксисоединений
Химические свойства гидроксисоединений
В химических реакциях гидроксисоединений возможно разрушение одной из двух связей:
· С–ОН с отщеплением ОН-группы
· О–Н с отщеплением водорода.
Это могут быть реакции замещения, в которых происходит замена ОН или Н, или реакция отщепления (элиминирования), когда образуется двойная связь.
Полярный характер связей С–О и О–Н способствует гетеролитическому их разрыву и протеканию реакций по ионному механизму. При разрыве связи О–Н с отщеплением протона Н+ проявляются кислотные свойства гидроксисоединения, а при разрыве связи С–О - свойства основания и нуклеофильного реагента.
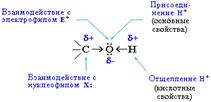 Таким образом, гидроксисоединения могут вступать в многочисленные реакции, давая различные классы соединений. Вследствие доступности гидроксисоединений, в особенности спиртов, каждая из этих реакций является одним из лучших способов получения определенных соединений.
Таким образом, гидроксисоединения могут вступать в многочисленные реакции, давая различные классы соединений. Вследствие доступности гидроксисоединений, в особенности спиртов, каждая из этих реакций является одним из лучших способов получения определенных соединений.
Фенолы в большинстве реакциий по связи О-Н активнее спиртов, поскольку эта связь более полярна за счет смещения электронной плотности от атома кислорода в сторону бензольного кольца (участие неподеленной электронной пары атома кислорода в системе p-сопряжения).
Фенолы являются более сильными кислотами, чем спирты и вода, т.к. за счет участия неподеленной электронной пары кислорода в сопряжении с p-электронной системой бензольного кольца полярность связи О–Н увеличивается.
Фенолы реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты: C6H5OH + NaOH ® C6H5ONa + H2O Образование фенолята железа под действием раствора хлорида железа (III) является качественной реакцией на фенолы (раствор приобретает коричнево-фиолетовую окраску).
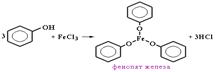 Фенолы не образуют сложные эфиры в реакциях с кислотами. Для этого используются более реакционноспособные производные кислот (ангидриды, хлорангидриды).
Фенолы не образуют сложные эфиры в реакциях с кислотами. Для этого используются более реакционноспособные производные кислот (ангидриды, хлорангидриды).
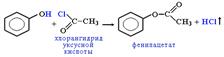 Для фенолов реакции этого типа не характерны, поскольку атом кислорода прочно связан с атомом углерода бензольного кольца за счет участия своей неподеленной электронной пары в системе сопряжения.
Для фенолов реакции этого типа не характерны, поскольку атом кислорода прочно связан с атомом углерода бензольного кольца за счет участия своей неподеленной электронной пары в системе сопряжения.
Реакции фенола по бензольному кольцу Взаимное влияние атомов в молекуле фенола проявляется не только в особенностях поведения гидроксигруппы (см.выше), но и в большей реакционной способности бензольного ядра. Гидроксильная группа повышает электронную плотность в бензольном кольце, особенно, в орто- и пара-положениях (+ М -эффект ОН-группы): 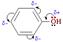 Поэтому фенол значительно активнее бензола вступает в реакции электрофильного замещения (SE) в ароматическом кольце. · Нитрование. Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов
Поэтому фенол значительно активнее бензола вступает в реакции электрофильного замещения (SE) в ароматическом кольце. · Нитрование. Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов
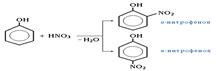
При использовании концентрированной HNO3 образуется 2,4,6- тринитрофенол (пикриновая кислота)
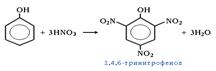 · Галогенирование. Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол)
· Галогенирование. Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол)

· Конденсация с альдегидами. Например:
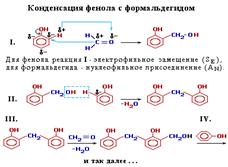
Данная реакция имеет большое практическое значение и используется при получении фенолфольмадегидных смол
· Фенол C6H5OH
· производство фенолформальдегидных смол;
· полупродукт в органическом синтезе.
Крезолы, их используют для получения синтетических смол, в синтезе красителей ядохимикатов, водные эмульсии крезолы с раствором мыла –антипсептик, применяемые в ветеринарии
Тимол содержиться во многих эфирных маслах и применяется кака антисептическое и противоглистное средство.






