Ионные реакции — это процессы, идущие с гетеролитическим разрывом ковалентных связей, когда оба электрона связи остаются с одной из ранее связанных частиц:
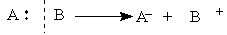
В результате гетеролитического разрыва связи получаются заряженные частицы: нуклеофильная и электрофильная.
Нуклеофильная частица (нуклеофил) — это частица, имеющая пару электронов на внешнем электронном уровне. За счет пары электронов нуклеофил способен образовывать новую ковалентную связь.
Электрофильная частица (электрофил) — это частица, имеющая незаполненный внешний электронный уровень. Электрофил представляет незаполненные, вакантные орбитали для образования ковалентной связи за счет электронов той частицы, с которой он взаимодействует.
В органической химии все структурные изменения рассматриваются относительно атома (или атомов) углерода, участвующего в реакции. Наиболее часто встречаются следующие типы превращений:
присоединение
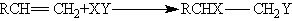
замещение
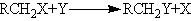
отщепление
(элиминирование)
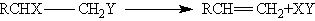
полимеризация
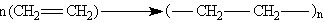
В соответствии с вышеизложенным хлорирование метана под действием света классифицируют как радикальное замещение, присоединение галогенов к алкенам — как электрофильное присоединение, а гидролиз алкилгалогенидов — как нуклеофильное замещение.
Структурная изомерия
Структурная изомерия — результат различий в химическом строении. К этому типу относят:
Изомерия углеводородной цепи (углеродного скелета)
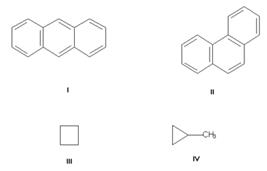
Изомерия углеродного скелета, обусловленная различным порядком связи атомов углерода. Простейший пример — бутан СН3—СН2—СН2—СН3 и изобутан (СН3)3СН. Другие примеры: антрацен и фенантрен (формулы I и II, соответственно), циклобутан и метилциклопропан (III и IV).
Валентная изомерия
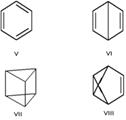
Валентная изомерия — особый вид структурной изомерии, при которой изомеры можно перевести друг в друга лишь за счёт перераспределения связей. Например, валентными изомерами бензола (V) являются бицикло[2.2.0]гекса-2,5-диен (VI, «бензол Дьюара»), призман (VII, «бензол Ладенбурга»), бензвален (VIII).
Изомерия функциональной группы
Различается характером функциональной группы; например, этанол (CH3—CH2—OH) и диметиловый эфир (CH3—O—CH3).
Изомерия положения
Тип структурной изомерии, характеризующийся различием положения одинаковых функциональных групп или двойных связей при одинаковом углеродном скелете. Пример: 2-хлорбутановая кислота и 4-хлорбутановая кислота.
] Пространственная изомерия (стереоизомерия)
[Энантиомерия (оптическая изомерия)
Пространственная изомерия (стереоизомерия) возникает в результате различий в пространственной конфигурации молекул, имеющих одинаковое химическое строение. Этот тип изомеров подразделяют на энантиомерию (оптическую изомерию) и диастереомерию.
Энантиомерами (оптическими изомерами, зеркальными изомерами) являются пары оптических антиподов — веществ, характеризующихся противоположными по знаку и одинаковыми по величине вращениями плоскости поляризации света при идентичности всех других физических и химических свойств (за исключением реакций с др. оптически активными веществами и физических свойств в хиральной среде). Необходимая и достаточная причина возникновения оптических антиподов — принадлежность молекулы к одной из следующих точечных групп симметрии: C n, D n, T, O или I (хиральность
). Чаще всего речь идет об асимметрическом атоме углерода, то есть об атоме, связанном с четырьмя разными заместителями.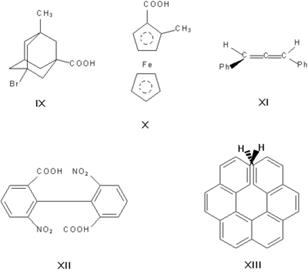
Асимметрическими могут быть и другие атомы, например атомы кремния, азота, фосфора, серы. Наличие асимметрического атома — не единственная причина энантиомерии. Так, имеют оптические антиподы производные адамантана (IX), ферроцена (X), 1,3-дифенилаллена (XI), 6,6'-динитро-2,2'-дифеновой кислоты (XII). Причина оптической активности последнего соединения — атропоизомерия, то есть пространственная изомерия, вызванная отсутствием вращения вокруг простой связи. Энантиомерия также проявляется в спиральных конформациях белков, нуклеиновых кислот, в гексагелицене (XIII).
(R)-, (S)- номенклатура оптических изомеров (правило наименования)
Четырём группам, присоединенным к асимметрическому атому углерода Cabcd, приписывается различное старшинство, отвечающее последовательности: a>b>c>d. В простейшем случае, старшинство устанавливается по порядковому номеру атома, присоединенного к асимметрическому атому углерода: Br(35), Cl(17), S(16), O(8), N(7), C(6), H(1).
Например, в бромхлоруксусной кислоте:
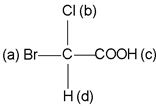
Старшинство заместителей при асимметрическом атоме углерода следующее: Br(a), Cl(b), C группы COOH (c), H(d).
У бутанола-2 кислород является старшим заместителем (а), водород — младшим (d):
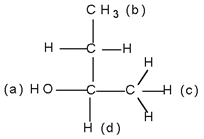
Требуется решить вопрос о заместителях —CH3 и —CH2CH3. В этом случае старшинство определяется порядковым номером или номерами других атомов в группе. Первенство остается за этильной группой, так как в ней первый атом С связан с другим атомом С(6) и с другими атомами Н(1), тогда как в метильной группе углерод соединен с тремя атомами Н с порядковым номером 1. В более сложных случаях продолжают сравнивать все атомы, пока не доходят до атомов с различными порядковыми номерами. Если имеются двойная или тройная связи, то находящиеся при них атомы считаются соответственно за два и за три атома. Так, группу —COH рассматривают как С (O, O, H), а группу —COOH — как С(О, О, ОН); карбоксильная группа старше альдегидной, поскольку содержит три атома с порядковым номером 8.
В D-глицериновом альдегиде старшей является группа ОН(а), затем следует CHO(b), CH2OH(c) и Н(d):
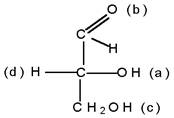
Следующий этап заключается в определении, является ли расположение групп правым, R (лат. rectus), или левым, S (sinister). Переходя к соответствующей модели, её ориентируют так, чтобы младшая группа (d) в перспективной формуле оказалась внизу, и затем рассматривают сверху вдоль оси, проходящей через заштрихованную грань тетраэдра и группу (d). В D-глицериновом альдегиде группы
a→b→c→d
расположены в направлении правого вращения, и следовательно, он имеет R-конфигурацию:
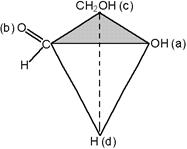
(R)-глицериновый альдегид
В отличие от D-, L- номенклатуры, (R)- и (S)- в обозначении изомеров заключают в скобки.
[ править ] Диастереомерия
[ править ] σ—диастереомерия
Диастереомерными считают любые комбинации пространственных изомеров, не составляющие пару оптических антиподов. Различают σ и π-диастереомеры. σ-диастереомеры отличаются друг от друга конфигурацией части имеющихся в них элементов хиральности. Так, диастереомерами являются (+)-винная кислота и мезо-винная кислота, D-глюкоза и D-манноза, например:
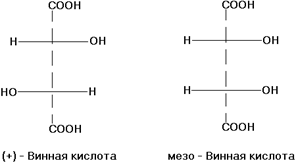
Для некоторых типов диастереомерии введены специальные обозначения, например, трео- и эритро-изомерия — это диастереомерия с двумя асимметрическими атомами углерода и пространственным расположением заместителей у этих атомов, напоминающим соответствующую треозу (родственные заместители находятся по разные стороны в проекционных формулах Фишера) и эритрозу (заместители — по одну сторону):
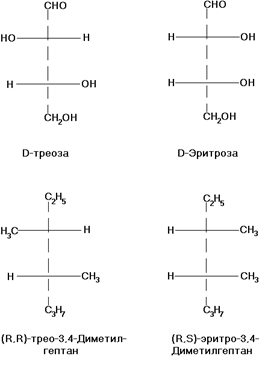
Эритро-изомеры, которых асимметрические атомы связаны с одинаковыми заместителями, называются мезо-формами. Они, в отличие от остальных σ-диастереомеров, оптически неактивны из-за внутримолекулярной компенсации вкладов во вращение плоскости поляризации света двух одинаковых асимметрических центров противоположной конфигурации.
Пары диастереомеров, различающиеся конфигурацией одного из нескольких асимметрических атомов, называются эпимерами, например:
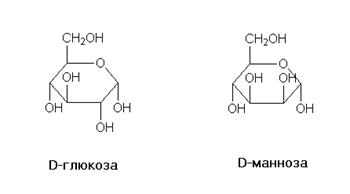
Термин «аномеры» обозначает пару диастереомерных моносахаридов, различающихся конфигурацией гликозидного атома в циклической форме, например, аномерны α-D- и β-D-глюкозы.
[ править ] π—диастереомерия (геометрическая изомерия)
π-диастереомеры, называемые также геометрическими изомерами, отличаются друг от друга различным пространственным расположением заместителей относительно плоскости двойной связи (чаще всего С=С и С=N) или цикла. К ним относятся, например, малеиновая и фумаровая кислоты (формулы XIV и XV соответственно), (Е)- и (Z)-бензальдоксимы (XVI и XVII), цис- и транс-1,2-диметилциклопентаны (XVIII и XIX).
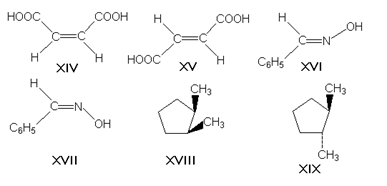
[ править ] Конформеры. Таутомеры
Явление неразрывно связано с температурными условиями его наблюдения. Так, например, хлорциклогексан при комнатной температуре существует в виде равновесной смеси двух конформеров — с экваториальной и аксиальной ориентацией атома хлора:

Однако при −150 °C можно выделить индивидуальную а-форму, которая ведет себя в этих условиях как устойчивый изомер.
С другой стороны, соединения, в обычных условиях являющиеся изомерами, при повышении температуры могут оказаться находящимися в равновесии таутомерами. Например, 1-бромпропан и 2-бромпропан — структурные изомеры, однако при повышении температуры до 250 °C между ними устанавливается равновесие, характерное для таутомеров.
Изомеры, превращающиеся друг в друга при температуре ниже комнатной, можно рассматривать как нежесткие молекулы.
Существование конформеров иногда обозначают термином «поворотная изомерия». Среди диенов различают s-цис- и s-транс-изомеры, которые, по существу, являются конформерами, возникающими в результате вращения вокруг простой (s — от англ. single, «одиночный») связи:
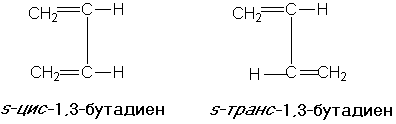
Изомерия также характерна для координационных соединений. Так, изомерны соединения, различающиеся по способу координации лигандов (ионизационная изомерия), например, изомерны:
[Co(NH3)5Br]+SO4−
и
[Co(NH3)5SO4]+Br−
Здесь, по существу, имеется аналогия со структурной изомерией органических соединений.
[ править ] Изомеризация
Химические превращения, в результате которых структурные изомеры превращаются друг в друга, называется изомеризацией. Такие процессы имеют важное значение в промышленности. Так, например, проводят изомеризацию нормальных алканов в изоалканы для повышения октанового числа моторных топлив; изомеризуют пентан в изопентан для последующего дегидрирования в изопрен. Изомеризацией являются и внутримолекулярные перегруппировки, из которых большое значение имеет, например, перегруппировка Бекмана — превращение циклогексаноноксима в капролактам (сырье для производства капрона).
Процесс взаимопревращения энантиомеров называется рацемизацией: она приводит к исчезновению оптической активности в результате образования эквимолярной смеси (−)- и (+)-форм, то есть рацемата. Взаимопревращение диастереомеров приводит к образованию смеси, в которой преобладает термодинамически более устойчивая форма. В случае π-диастереомеров — обычно транс-форма. Взаимопревращение конформационных изомеров называется конформационным равновесием.
Явление изомерии в огромной степени способствует росту числа известных (и ещё в большей степени — числа потенциально возможных) соединений. Так, возможное число структурно-изомерных дециловых спиртов более 500 (известно из них около 70), пространственных изомеров здесь более 1500.
При теоретическом рассмотрении проблем изомерии все большее распространение получают топологические методы; для подсчёта числа изомеров выведены математические формулы. Для обозначения пространственных изомеров разных типов разработана стереохимическая номенклатура, собранная в разделе Е Номенклатурных правил ИЮПАК по химии.
Опти́ческая изомери́я (энантиомерия) — разновидность пространственной изомерии, являющаяся прямым следствием хиральности молекул, проявляется способностью некоторых веществ поворачивать плоскость поляризованного луча в противоположные стороны. Оптическая изомерия свойственна молекулам органических веществ, не имеющим плоскости симметрии, которые относятся друг к другу как предмет к своему зеркальному отражению.
Оптическая изомерия
Если атом углерода в молекуле связан с четырьмя различными атомами или атомными группами, например:
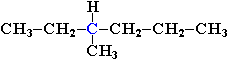
то возможно существование двух соединений с одинаковой структурной формулой, но отличающихся пространственным строением. Молекулы таких соединений относятся друг к другу как предмет и его зеркальное изображение и являются пространственными изомерами.
Изомерия этого вида называется оптической, изомеры – оптическими изомерами или оптическими антиподами:
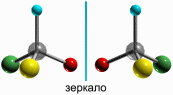
См. также анимацию и
виртуальные (VRML) модели оптических изомеров.
Молекулы оптических изомеров несовместимы в пространстве (как левая и правая руки), в них отсутствует плоскость симметрии.
Таким образом,
· оптическими изомерами называются пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение.
Оптические изомеры имеют одинаковые физические и химические свойства, но различаются отношением к поляризованному свету. Такие изомеры обладают оптической активностью (один из них вращает плоскость поляризованного света влево, а другой - на такой же угол вправо). Различия в химических свойствах наблюдаются только в реакциях с оптически активными реагентами.
Оптическая изомерия проявляется в органических веществах различных классов и играет очень важную роль в химии природных соединений.






