В наст. время невозможно рассчитать или экспериментально определить абсолютное значение скачка потенциала на отдельно взятом электроде. Поэтому значение потенциала на электроде всегда определяется по отношению к эталонному электроду, потенциал к-го условно принимается =0.В электрохимии таким электродом является нормальный водородный элемент (н.в.э.).Потенциал н.в.э. при опред-х условиях =0. В стеклянный сосуд сложной формы залит раствор серной кислоты такой концентрации, что [H+]»1 г-ион/л.Платиновая чернь (губчатая пластина) – платиновый электрод.Р=1атм.Водород омывает платину, растворяется в ней. Насыщенная водородом платина начинает вести себя как водородный электрод, т.е.
H++к «1/2H2
2H+ЅH2
jH=0
Т.о. за величину электродного потенциала данного электрода принимается ЭДС гальванического элемента, составленного из исследуемого электрода и н.в.э. Электродному потенциалу присваевается знак, одинаковый со знаком заряда данного электрода в паре с н.в.э.
Например Zn в паре с н.в.э. заряжается отрицательно, а это значит, что потенциал Zn-го электрода равен ЭДС Zn-го водородного элемента с обратным знаком.
jZn=j0Zn+RT/nФ*ln aZn2+ jMe=j0Me+RT/nФ*ln[Men+] j0-стандартное значение потенциала.Т=298К(250С). jМе=j0Ме+0.059/n*lg[Men+]
Если все металлы выстроить в ряд повелечинам их j0, то мы получим т.н. ряд напряжений. В ряду напряжений помещен и jН=0. Все металлы, расположенные в ряду напряжений выше Н имеют j0<0, ниже - j0>0В водородном электроде протекает реакция: H++к «H – n=1 jH= j0H+0.059/1*lg[H+], j0H =0 по условию. jH =0.059lg[H+], pH=-lg[H+], jH=-0.059pH. потенциала более положительного электрода вычесть потенциал менее положительного. Cu – Zn: E=jCu-jZn=j0Cu-j0Zn+RT/nФ*ln([Cu2+]-[Zn2+])=E0 E0-RT/nФ*ln[Zn2+]/[Cu2+] n=2; E0=j0Cu-j0Zn=0.34-(-0.763)=1.103B;E0экспериментальное=1.087В, DE=0.016B-диффузионный скачок потенциалов на границе 2 растворов.
Типы электродов и цепей. Окислительно-восстановительные электроды и цепи.
1. Электроды 1 рода. Металлические, обратимые относительно катиона.



2. Металлические электроды, обратимые относительно аниона.






3. Газовые электроды, обратимые как относительно катионов, так и анионов.


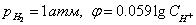


4. Окислительно-восстановительные электроды.
Металлическая пластина не принимает участия, она токоотвод.








Типы цепей
1. Химические цепи – 2 разных металлических электрода (Al-Zn).
2. Окислительно-восстановительные цепи (2 ОВ-электрода)
ОВР течет самопроизвольно в сторону превращения сильного окислителя в слабый сопряженный окислитель, сильного восстановителя в слабый сопряженный восстановитель.
3. Концентрационные цепи.

Разные концентрации электролитов.






