Виды сточных вод. Сточные воды, отводимые с территории промышленных предприятий, по своему составу могут быть разделены на 3 вида:
-производственные – использованные в технологическом процессе производства или получающиеся при добыче полезных ископаемых;
-бытовые – от санитарных узлов производственных и не производственных корпусов и зданий, а также от душевых установок, имеющихся на территории, промышленных предприятий;
-атмосферные – дождевые и оттаивание снега.
Основные источники загрязнения:
1)Атмосферные стоки: а) дожди, вымывающие из атмосферы газообразные вещества и взвешенные частицы. б) ливневые стоки с городских улиц, промышленных и с/х территорий, несут собой нефтепродукты, хим. соединения. удобрения., пестициды.
2)Городские стоки, загрязнены детергентами, микроорганизмами, бактериями.
3)Промышленные стоки, загрязнены хим-ми реагентами, тяжелыми металлами, ПАВ, нефтепродуктами.
Производственные сточные воды делятся на 2 две основные категории: загрязнённые и незагрязненные (условно чистые).
Загрязненные производственные сточные воды содержат различные примеси и подразделяются на 3 группы:
1)загрязнённые преимущественно минеральными примесями (предприятия металлургической, машиностроительной, угледобывающей промышленности);
2)органическими примесями (предприятия рыбной, мясной, молочной, пищевой, целлюлозно-бумажной промышленности);
3)минеральными неорганическими примесями (предприятия нефтедобывающей, нефтеперерабатывающей, текстильной, лёгкой промышленности).
44.Антропогенное воздействие на водные ресурсы: загрязнения, изъятие, эвтрофикация водоёмов. Экологические проблемы морей, рек (Арала, Байкала).
Гидросфера — водная оболочка Земли; масса (1,5-2,5)*1018 тонн; находится в виде паров и облаков, океанов и морей (91,3% массы), ледников, подземных вод. Вода в природных условиях всегда содержит растворенные соли, газы, органические вещества. При концентрации солей до 1г/кг вода считается пресной, до 25 г/кг – солоноватой, более 25 г/кг – соленой. В пресных водах обычно преобладают ионы HCO3(-), Ca(2+), Mg(2+). По мере роста минерализации увеличивается концентрация SO4(-), Cl(-), Na(+), K(+). Пресная вода — 1% от общей массы.
Загрязнение водоемов – это снижение их биосферных функций и экологического значения, в результате поступления в них вредных веществ. Загрязнение водных систем представляет большую опасность; чем загрязнение атмосферы, т.к.
1)процессы регенерации и самоочищения протекают гораздо медленнее.
2)более разнообразны источники загрязнения.
3)естественные процессы осуществляются в водной среде и которые подвергаются загрязнениям имеют большие значение для жизни.
Загрязнители:
химические. В этом виде участвуют все виды промышленного, с/х производства, транспорт. Представляет собой изменение естественных химических свойств воды из-за увеличения в ней вредных примесей как неорганической. (кислоты, щелочи, соли, нефтепродукты, пестициды, диоксины, тяжелые металлы, фенолы, аммонийный и нитридный азот)
биологические. Вызывается микроорганизмами и способными к брожению органическими веществами, приводит к бактериологическому заражению. (вирусы, бактерии, другие болезнетворные организмы, водоросли, дрожжевые и плесневые грибы)
физические. Связано со сбросом тепла в воду, что приводит к потрясению всего биоценоза водоемов. Источником служат подогретые сбросные воды ТЭЦ и промышленности; повышение температуры изменяет естественные условия для водных организмов, снижает количество растворенного кислорода, изменяет скорость обмена веществ. Также к физическому загрязнению относятся радиоактивное загрязнение вод, попадание различных взвесей в водные системы. (радиоактивные элементы, взвешенные твердые частицы, тепло, органолептические (цвет, запах), шлам, песок, ил, глина)
Загрязнители:
1. Целлюлозно-бумажный комплекс, деревообработка: органические вещества (смолы, жиры, лигнины, фенол), аммонийный азот, сульфаты, вывешенные вещества.
2. Нефтегазо добыча: нефтепродукты, СПАВ, фенолы, аммонийный азот, сульфиды.
3. Машиностроение, металлообработка, металлургия: тяжелые металлы, взвешенные вещества, цианиды, аммонийный азот, нефтепродукты, смолы, фенолы, фотореагенты.
4. Химическая, нефтехимическая промышленность: фенолы, нефтепродукты, СПАВ, полициклические ароматические углеводороды, бензапирен, взвешенные вещества.
5. Горнодобывающая, угольная: флотореагенты, минеральные взвешенные вещества, фенолы.
6. Легкая, текстильная, пищевая: СПАВ, нефтепродукты, органические красители, органические вещества.
Эвтрофикация — повышение уровня первичной продуктивности водоемов из-за повышения в них концентрации биогенных веществ, в основном азота и фосфора; часто приводит к цветению вод.
Эвтрофикация водоемов
Качественный и количественный состав биоценоза и особенности питания (степень трофности) в озере обусловливаются химическим составом воды.
Олиготрофные озера (от греч. oligos — незначительный, бедный, trophe — питание, пища). Их воды бедны минеральным азотом и особенно фосфором, встречающимся в виде следов. Благодаря низкой плотности биоценоза в воде присутствует много кислорода, а содержание С02 невелико, вследствие чего, в частности, отмечается нерастворимость соединений железа. Вода прозрачная, синего или зеленого цвета. К такому типу относят глубокие озера с песчаными берегами.
Эвтрофные озера (от греч. - хорошо). Их воды богаты азотом и фосфором. Обилие организмов ведет к истощению кислорода в глубинных слоях во время фаз застоя. Вода малопрозрачная, от зеленовато-коричневой до коричневой. Для таких озер характерны небольшие глубины, благоприятствующие образованию широких поясов прибрежной растительности.
Дистрофные озера. Это неглубокие озера с берегами, поросшими торфообразующими растениями. Вода мало прозрачна, окрашена в бурый цвет гуминовыми веществами; кислород в дефиците; реакция воды слабо кислая.
Между этими типами озер существуют все переходные стадии. Кроме того, одно и то же озеро (пруд) может переходить из одного типа в другой.
Трагедия Арала. В 1911-1960 гг. природный комплекс Аральского моря и впадающих в него рек Амударьи и Сырдарьи находились в равновесном состоянии; так, в Арал поступало 56 км воды, приток грунтовых вод был не менее 1 км,с осадками поступало 9 км, объем моря составлял 1064 км, с испарениями терялось 66 км.
Море отступило под натиском цивилизованного варварства. В бассейне Аральского моря в самые многоводные годы находилось 56 км воды, сейчас не более 10-15 км3, так как вода разбирается на орошение. В связи со строительством Каракумского канала речной сток сократился в.1965 г. до 29,9 км3 в 1981-1987 гг. в Аральское море поступало 4,0-9,3 км3 воды, объем моря составлял 404 км3, т. е. сократился почти в 2,5 раза, при этом уровень моря понизился на 14 м, а соленость увеличилась в 2,5-3 раза. Таким образом, море потеряло биологическую продуктивность, в 1988 г. произошел раздел моря на Большое (342 км) и Малое (121 км3). В результате засоления, загрязнения почвы нитратами, пестицидами погибли плодовые сады, произошло опустынивание на больших территориях. Вода сильно минерализована, кроме того, вода загрязнена удобрениями и ядохимикатами. высыхают рукава дельты, исчезают озерные системы, увеличивается повторяемость пыльно-солевых бурь. Опустыниваются территория прилегающие к Аралу, деградирует само море.
В экологической катастрофе Арала повинно сооружение главных оросительных каналов: большого Ферганского, а также строительство большого количества водохранилищ. В 1982 г. основное русло Арата было перекрыто глухой насыпной плотиной и весь речной сток направили на орошение окружающих территорий.
Резко сократились рыбные запасы водоема, уменьшилась численность и изменился состав обитающих в нем микроорганизмов. Теперь Арал раньше и быстрее замерзает и дольше освобождается ото льда. Резко изменился климат региона. Арал утратил хозяйственное и транспортное значение Появилась проблема с трудоустройством и переселением живущих на его берегах людей.
Озеро Байкал - уникальный резервуар пресной воды. Объем Байкала 23015 км", площадь водосборного бассейна 588000 км. В Байкале водятся более 500 видов животных, 50 видов рыб, более 1200 видов растений, половина всех живых организмов обитает только в Байкале и нигде в мире не встречается.
В Байкале происходит самоочищение воды под действием мельчайших водорослей, рачков, которые извлекают из воды минеральные и органические вещества. В Байкал впадает 336 рек, а вытекает только одна река Ангара.
Предприятия химической, биологической и с/х отраслей способствуют загрязнению озера, разрушению биохимического и физического состава и структуры водных масс. До нормативных показателей очищается 15 % вод, с основным стоком Байкальского целлюлозно-бумажного комбината (ЦБК) и Селенгинского целлюлозно-карбонатного комбината (ЦКК) поступает в воды Байкала до 70 % трудно растворимых органических веществ. В настоящее время не решена проблема перепрофилирования ЦБК и ЦКК, не реализован проект лесоустройства в водоохраной зоне, лишь частично построены природоохранные и очистные сооружения, мало используются биологически чистые топлива, не вос-ся биолог. ресурсы озер, не прекращается вырубка леса акватории Байкала.
45.Показатели качества воды: значения, от каких факторов зависят.Физические (цвет, запах, вкус, наличие взвесей);Химические (рН, жесткость, содержание ионов металлов, органических веществ, растворенного кислорода, ОВП и электропроводность); Биологические (наличие гидробионтов и гидрофлоры); Бактериологические.
Питьевая вода – вода пригодная к употреблению человеком и отвечающая критериям.
1)Физические: Взвешенные вещ-ва могут иметь минеральное и органическое происхождение. Цветность воды обусловлена присутствием в воде гумусовых вещ-в, жиров, органических кислот и других органических соединений. Запах и вкус воды оцениваются по по 5-тибальной системе.
Цвет. Качественную оценку цветности воды производят, сравнивая ее с дистиллированной водой. Для этого в стаканы из бесцветного стекла наливают исследуемую и дистиллированную воду и рассматривают их на фоне белой бумаги при дневном освещении сбоку и сверху. При наличии окраски указывают цвет воды (слабо-желтый, бурый); при отсутствии ее воду называют бесцветной. Количественно цветность воды определяют методом колориметрии, сравнивая ее со шкалой эталонов, имитирующих эту цветность.
Запах. При оценке запаха сначала дают его качественную характеристику (болотный, землистый, гнилостный, рыбный, ароматический); затем оценивают запах воды по пятибалльной системе. Для этого воду наливают в колбу с притертой пробкой до 2/3 объема и сильно встряхивают в закрытом состоянии, затем открывают колбу и сразу же отмечают интенсивность запаха. Наличие запаха в очищенных водах свидетельствует о недостаточной степени очистки или неполном удалении использованных при очистке реагентов (например, хлора).
2) Химические: главные ионы, растворенный газ, биогенные вещ-ва, микроэлементы и органические вещ-ва. Наиболее распространенные в природных водах анионы: HCO3, SO2-4, CL-, CO2-3, HSiO-3; катионы: Na, Ca, Mg2+, K, Fe3+.
Кислотность. Кислотность воды обусловлена присутствием в ней свободной угольной кислоты, а также других кислот или гидролитически кислых солей. Перед сбросом кислых стоков в водоем кислотность должна быть нейтрализована. Кислотность сточных вод определяют титриметрическим методом, используя в качестве индикатора фенолфталеин.
Щелочность. Щелочность воды зависит от присутствия в ней свободных щелочей и гидролитически щелочных солей. Общая щелочность сточных вод определяется титриметрически, путем титрования воды соляной кислотой по индикатору метиловому оранжевому. I Степень кислотности или щелочности сточных вод (рН) определяют потенциометрически с помощью специальных приборов - рН-метров.
Контроль активной реакции среды сточных вод необходим не только на выходе из очистных сооружений, но и на входе в них, поскольку для обеспечения нормальной жизнедеятельности микроорганизмов, осуществляющих биохимическую очистку воды, требуется реакция среды, близкая к нейтральной (рН ~ 6,5 - 8,5). При резком отклонении рН от этих значений процесс биохимической очистки может нарушиться и даже полностью прекратиться.
Азот. При анализе сточных вод определяют содержание азотааммонийного (NH+4) и азота нитритов и нитратов (NO-2, NO-3).Обычно концентрацию NH+4,NO-2и NO-3определяютколориметрическим методом, основанным на реакции этих ионов с соответствующими реактивами с образованием окрашенных соединений и с последующим определением интенсивности окраски на фотоколориметре.
Окисляемость. Окисляемость воды обусловлена наличием в ней органических веществ и легко окисляющихся неорганических соединений (Fe2+, сульфитов, нитритов, сероводорода и др.) и выражается массой кислорода, потраченного на окисление органических веществ, содержащихся в I л воды (мг О2*л-1). При ее определении в качестве окислителя органических веществ применяют КМп04 (перманганатная окисляемость).
Хим-ая потребность в кислороде (ХПК) (дихроматная окисляемость). ХПК дает представление о содержании в анализируемой воде органических веществ, способных к окислению сильными окислителями, и определяется титриметрически с использованием в качестве окислителя Дихромата калия.
Биохимическая потребность в кислороде (БПК). БПК - показатель, используемый для характеристики степени загрязнения сточных вод органическими примесями, способными разлагаться микроорганизмами с потреблением кислорода. БПК показывает, какое количество кислорода (мг*л-1) расходуется аэробными микроорганизмами на окисление органических примесей. Полное биохимическое окисление органических веществ в воде требует длительного времени. В лабораторных условиях обычно определяют биохимическое потребление кислорода за 5 суток или БПК5 (стандартное БПК). Сущность метода сводится к тому, что в анализируемой воде определяют содержание растворенного кислорода до и после термостатирования. Определение проводят йодометрическим методом.
Жесткость – это содержание солей магния и кальция. Различают карбонатную жесткость, обусловленную присутствием в воде гидрокарбонатов кальция и магния, и некарбонатную, вызываемую присутствием в воде хлоридов и сульфатов кальция и магния. Суммарное содержание в воде всех солей кальция и магния составляет общую жесткость. Общую жесткость определяют комплексонометрическим методом, карбонатную - титрованием соляной кислотой в присутствии метилового оранжевого, некарбонатную жесткость по разности результатов этихопределений.
3) Биологические показатели качества воды - содержание гидробионатов и гидрофлоры.
Гидробиониты подразделяются на: а)планктон (обитатели, пребывающие в толще воды от дна до поверхности)различают фитопланктон(водоросли) и зоопланктон (простейшие). б)Бентос- обитатели, находящиеся на дне водоема, в)нейстон - организмы, неподвижные или плавающие на поверхности (икра); г)перифитон – организмы, прикрепленные к листьям или другим выступам над дном (губки, гидры).
Гидрофлора водных объектов определяется макро- и микрофитами. а) Макрофиты - высшая, водная растительность, б)микрофиты - водоросли. При отмирании и разложении макрофитов вода обогащается органическими веществами, ухудшаются органолептические свойства. Микрофиты поглощают углекислый газ и выделяют кислород.
4) Бактериологические показатели качества воды характеризуют безвредность воды относительно присутствия болезнетворных микроорганизмов. Важным бактериологическим показателем является содержание бактерии группы кишечной палочки в 1 л воды, которое определяет величину Коли-индекса.
46.Методы анализа воды: гравиметрические, титриметрические, фотометрические, потенциометрические, вольтамперометрические.
Гравиметрический – основан на определении массы вещ-ва. В ходе анализа вещ-во отгоняется в виде какого-либо летучего соединения или осаждается из раствора в виде малорастворимого соединения. Осадок взвешивается в виде соединения строго определенного состава, весовая форма по составу совпадает с осаждаемой. По весу высушенного или прокаленного осадка вычисляется содержание определенного компонента в данном образце. Достоинства: высокая точность, отсутствие необходимости калибровки, простота. Недостатки: значительный расход времени на выполнение анализа. Титриметрический. Основан на точном измерении количества реактива израсходованного на реакцию с определенными веществами. Титрированный раствор – раствор, концентрация которого известна с высокой точностью. Титрование – прибавление титрованного раствора к анализируемому для точного определения эквивалентного количества. Момент титрирования – точка эквивалентности. Титрирующий раствор – титрант. Используются реакции кислотно-основного взаимодействия, удовлетворяющие требованиям, которые предъявляются к титриметрическим реакциям. Взаимодействие должно происходить полностью и с высокой скоростью. Достоинства: быстрота выполнения, простота оборудования, удобство выполнения серийных анализов, большой набор химических реакций. Недостатки: необходимость предварительной стандартофикации растворов титранта и калибровки мерной посуды.
Фотометрический. Измеряет поглощение света анализируемым раствором обычно после введения в него реактива, реагирующего с определенным компонентом сточной воды с образованием интенсивно поглощающего свет соединения. Приборы: Источник света – светофильтр – кювета с раствором – детектор. Конструкция прибора зависит от области спектра применения. Излучение выбирают такое, что бы соединение имело max светопоглощение, а примеси – min. Достоинства – широкая область применения, высокая чувствительность. Недостатки: калибровка аппаратуры, посуды.
Потенциометрия и потенциометрическое титрование. Потенциометрия основана на измерении небольших равновесных напряжений между электродами гальванической ячейки. Метод можно применять для установления активности веществ в растворе (прямая потенциометрия) и для нахождения точки эквивалентности при титриметрических определениях (потенциометрическое титрование). Прямая ПМ находит применение при определении рН растворов, а также многих ионов с использованием ионоселективных электродов. В анализе природных вод и питьевой воды ионоселективные электроды применяют для определения кадмия, меди, свинца, серебра, щелочных металлов, бромид-, хлорид-, цианид-, фторид-, иодид - и сульфид ионов.
Вольтамперометрические методы анализа. Это совокупность методов исследования кривых ток-потенциал и их зависимостей от электродных реакций и концентраций определяемых веществ. Один из основных ВАМ методов – полярография. Метод заключается в получении и анализе кривых ток-потенциал на ртутном капельном электроде. Методом полярографии можно определить любые вещества, способные к эл-хим превращениям на электродах. Качественная информация следует из значения потенциала полуволны (φ1/2), количественная – из определения высоты волны.Типичная полярографическая волна, используемая для качественного и количественного определения электродно -активных веществ.
47 Контроль, управление качеством воды в водных объектах: а)ПДКзагрязняющих вещ-в; б)предельно-допустимая нагрузка на водный объект (ПДН), чем она определяется;в)предельно-допустимый сброс(ПДС).Понятие о ХПК и БПК.
а) Для водной среды ПДК загрязняющих веществ означает такую концентрацию вещества выше которой вода становится неприродной для одного или нескольких видов водопользования.
б) Степень предельно - допустимого загрязнения воды определяется его физическими особенностями (температурой, скоростью течения), а так же способность к нейтрализации примеси, есть предельно допустимая нагрузка на водный объект ПДН, так как использование воды связано с её изъятием, а значит с угрозой истощения водного объекта, разрушение его экологической системы.
в) Сброс сточных вод должен осуществляться до уровня саморазгрузки. Либо сточные воды должны очищаться или разбавляться перед сбросом, либо рассеиваться сразу после сброса до установления норматива.
ПДС – устанавливается санитарной службой для каждого предприятия с учетом:
а) ПДК вредного вещества
б) осимиллирующие способности водного объекта
в) сброс других производств
г) скорости течения воды
д) с учетом хим. состава и рельефа.
ХПК – хим. потребл. кислорода. Определяется как количество кислорода потребляемого при хим. окислении под воздействием окислителей, содержащихся в воде органич и не органич веществ.
БПК–биологическая потребляемость кислорода. Это количество кислорода, израсходованного за определенный промежуток времени (5, 20 суток) на аэробное биохимич окисление, то есть на разложение органич соединений микроорганизмами.
Защита гидросферы.
1) Развитие безотходных и безводных технологий, систем замкнутого водоснабжения
2) очистка сточных вод(промышленных, коммунально-бытовых и др.)
3) очистка и обеззараживание поверхностных вод, использующихся для водоснабжения.
4) закачка сточных вод в глубокие водоносные горизонты.
49. Механические методы очистки сточных вод: процеживание, отстаивание, фильтрация, центрифугирование. Типовое оборудование.
Механические методы применяются как первая стадия в общей схеме очистки сточных вод. Выбор механического метода очистки осуществляется с учётом размера взвешенных частиц. Механическая очистка состоит из:
1. процеживания через решётки
2. отстаивание – преаэрацией, биокоагуляцией, осветвлением во взвешенном слое (отстойники - осветлители) или в тонком слое (тонкослойные отстойники), а также с помощью гидроциклонов.
3. фильтрование – пропускание воды через слой различного зернистого материала(кварцевого песка, гранитного щебня, дробленого антрацита и керамзита, горелых пород и других материалов) или через сетчатые барабанные фильтры микрофильтры, через высоко производственные напорные фильтры и фильтры с плавающей загрузкой.
4. Центрифугирование. Типовое оборудование для механической очистки – решетки, отстойники, фильтры, гидроциклы, центрифуги, жидкостные сепараторы.
50. Химические методы очистки: комплексообразования, нейтрализации, осаждения, окисления-восстановления Примеры используемых реакций.
Химические методы очистки сточных вод основаны на применении химических реакций, в результате которых загрязнения превращаются в безопасные соединения или легко выделяются в виде осадков. В особую группу химических методов следует выделить хлорирование и озонирование сточных вод, содержащих органические примеси, а также цианиды и другие пахнущие не органические вещества. Хлорирование и озонирование наиболее часто применяют для доочистки и обезвреживания питьевой воды на городских водопроводных станция.
1. Осаждение – это отделение определяемого компонента от сопутствующих веществ путем перевода его в осадок Ме2++2ОН à Ме(ОН)2
Ме3++3ОН à Ме(ОН)3
2. окисления-восстановления – объединяют многочисленную группу окислительно-восстановительных реакций.  +6
+6  + 14
+ 14 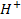 2
2  + 6
+ 6 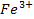 +7
+7 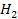 O
O
3. Комплексообразования – используют реакции образования координационных соединений. 2KCN+ 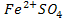
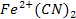 + 4 KCN +
+ 4 KCN + 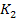 [
[  ]
]
3 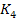 [
[  ] +4
] +4 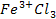
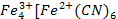 ]3 + 12 KCl.
]3 + 12 KCl.
4. Нейтрализация Н++ ОН à-Н2О (рН=6,5-8,5)
51. Физико-химические методы очистки: флотация, коагуляция, адсорбция, ионный обмен, обратный осмос, ультрафильтрация, электрохимические методы. Сущность и особенности каждого метода.
Флотация - процесс молекулярного прилипания частиц флотируемого материала к поверхности раздела двух фаз, обычно газа (чаще воздуха; и жидкости, обусловленный избытком свободной энергии поверхностных пограничных слоев, а также поверхностными явлениями смачивания.
Процесс очистки производственных сточных вод, содержащих ПАВ, нефть, нефтепродукты, масла, волокнистые материалы, методом флотации заключается в образовании комплексов "частицы-пузырьки", всплывании этих комплексов и удалении образовавшегося пенного слоя с поверхности обрабатываемой жидкости Прилипание частицы, находящейся в ней, к поверхности газового пузырька возможно только тогда, когда наблюдается не смачивание или плохое смачивание частицы жидкостью. Внешним проявлением способности жидкости к смачиванию является величина поверхностного натяжения ее по границе с газовой фазой, а также разность полярностей на границе жидкой и твердой фаз. Процесс флотации идет -эффективно при поверхностном натяжении воды не более (60-65)-10-3 Н/м. Большое значение при флотации имеют размер, количество и равномерность распределения воздушных пузырьков в сточной воде. Оптимальные размеры воздушных пузырьков 15-30 мкм, а максимальные -100-200 мкм.
Адсорбционный метод - один из наиболее доступных в эффективных методов глубокой очистки от растворенных органических веществ сточных вод предприятий целлюлозно-бумажной, химической, нефтехимической, текстильной и других отраслей промышленности.
Сорбция - это процесс поглощения вещества из окружающей среды твердым телом или жидкостью. Преимуществами этого метода являются возможность адсорбции веществ многокомпонентных смесей и высокая Эффективность очистки, особенно слабо концентрированных сточных вод. Сорбционные методы весьма эффективны для извлечения из сточных вод ценных растворенных веществ с их последующей утилизацией и использования очищенных сточных вод в системе оборотного водоснабжения промышленных предприятий.
В качестве сорбентов применяют различные искусственные и природные пористые материалы: золу, опилки, торф, коксовую мелочь, силикагели, активные глины и др. Эффективными сорбентами являются активированные угли различных марок. Активность сорбента характеризуется количеством поглощаемого вещества на единицу объема или массы сорбента (кг/м3, кг/ кг).
Обратный осмос (гиперфильтрация) - процесс молекулярного разделения растворов путем их фильтрования под давлением через полупроницаемые мембраны, задерживающие полностью или частично молекулы либо ионы растворенного вещества. При приложении давления выше осмотического (равновесного) осуществляется перенос растворителя в обратном направлении (от раствора к чистому растворителю через мембрану) и обеспечивается достаточная селективность очистки. Необходимое давление, превышающее осмотическое давление растворенного вещества в растворе, составляет при концентрации солей % 0,1 -1 МПа и при концентрации солей 20-3 0 г/л 5-10 МПа.
Ул ьтрафильтрация - мембранный процесс разделения растворов осмотическое давление которых мало. Этот метод используется при отделении сравнительно высокомолекулярных веществ, взвешенных -коллоидов. Ультрафильтрация по сравнению с обратным осмосом высокопроизводительный процесс, так как высокая проницаемость мембран д остигается при давлении 0,2-1 МПа.
Коагуляция – способность дисперсных систем выделяться на растворе под влиянием внешних воздействий. Вещества, обуславливающие коагуляцию называются коагулянтами. Центробежное отделение твердой фазы под действием центробежных и центростремительных сил происходит таких аппаратах, как центрифуги и гидроциклоны.
Применяется для очистки стоков от мелкодисперсных и коллоидных примесей.
Al+3 +H2O = Al(OH)2+ + H+
Al(OH)2+ + H2O = Al(OH)2+2 + H+
Al(OH)2+ + H2O = Al(OH)+3 + H+
Коагуляция. Для очистки стоков от мелкодисперсных и коллоид примесей используют их удаление с помощью коагулянтов и флокулянтов. Коагуляцию осуществляют непосредственно после удаления крупных взвесей.
При очистке питьевых и сточных вод в качестве коагулянтов используют соли алюминия, соли железа и их смеси в разных пропорциях. Реже применяют соли магния, цинка и титана. На станциях в специальных баках, защищенных от коррозии, готовят рабочие растворы коагулянтов определенной концентрации и дозируют их в обрабатываемую воду.
Ионообменный метод - процесс обмена ионами, находящимися в растворе, и ионами, присутствующими на поверхности твердой фазы -ионита. Очистка производственных сточных вод методом ионного обмена позволяет извлекать и утилизировать ценные примеси (соединения мышьяка,(фосфора, а также хром, цинк, свинец, медь, ртуть и другие металлы), ПАВ и радиоактивные вещества, очищать сточную воду до предельно допустимых концентраций с последующим ее использованием в технологических процессах или в системах оборотного водоснабжения.
По знаку заряда обменивающихся ионов иониты делят на катиониты и аниониты, проявляющие соответственно кислотные и основные свойства. Иониты подразделяются на природные и искусственные или синтетические. Практическое значение имеют неорганические природные и искусственные (алюмосиликаты, гидроокиси и соли многовалентных металлов; применяются также иониты, полученные химической обработкой угля, целлюлозы и лигнина. Однако ведущая роль принадлежит синтетическим органическим ионитам - ионообменным смолам.
Важнейшим свойством ионитов является их подготовительная способность, так называемая обменная емкость. (Полная емкость ионита (количество находящихся в сточной воде грамм-эквивалентов ионов, которое может поглотить 1 м3 ионита до полного насыщения. Рабочая емкость ионита - количество находящихся в воде грамм-эквивалентов ионов, которое может поглотить 1 м3 ионита до начала проскока в фильтрат поглощаемых ионов.
Электрохимические методы. Для очистки сточных вод применяют электрохимическое окисление или восстановление, электрофлотацию, электрофорез, электродиализ и электрокоагуляцию.
Общим для всех методов является осуществление электролиза сточных вод, при котором имеет место направленное движение ионов и заряженных дисперсных частиц и протекание реакций окисления на аноде и восстановления на катоде.
Электрохимическое окисление на индифферентном аноде (графит, титан, покрытый оксидами рутения, свинца и др.) различных органических соединений происходит путем образования окислителей С12,О2ClO которые способствуют разложению органических веществ обрабатываемой сточной воды. Электрохимическим окислением можно удалить фенолы, цианид- ионы и др. Электрохимическим вост. на катоде можно удалить из сточных металлы с положительным значением электродного потенциала, такие как Hg2+, Cr2+,Pb2+, Ni2+, можно восстановить непредельные органические соединения, осуществить восстановление соединений Сr6+ до Сr3+ и др. процесс электрохимического восстановления и окисления в значительной степени определяется электролита и величиной рН сточных вод, условиями проведения электролиза. При электрофлотации на катоде и аноде образуются пузырьки водорода и кислорода, которые оказывают флотационное действие Прилипая к частицам дисперсной фазы, поднимают их на поверхность. Очистка сточных вод электрофорезом и электродиализам основана на использовании направленного движения ионов и заряженных частиц процессе электролиза. Осуществляют такую очистку с помощью селективных ионообменных мембран (электродиализ) или фильтрующих материалов (электрофорез).
Электрокоагуляция. В процессе анодного растворения образуется коагулянты - гидроксиды металлов, которые снижают поверхностный заряд частиц под воздействием электрического поля. В электролитах, содержащих активирующие ионы такие как С1-,Вr-, стальной электрод при наложении электрического поля ионизируется по реакции
Fe° - е + Н20 = Fe(OH)адс + Н+;
Fе(ОН)адс - е + Н20= Fe(OH)2адс+ Н+.
В результате анодного растворения и последующего происходит накопление коагулирующего компонента. Гидроксид Fe(OH)2 образуется при рН > 4,5 и потенциале 0,8. В виде коллоидного раствора.
52. Биолог-ая очистка сточных вод. Факторы, влияющие на эффект-ть биолог-ой очистки.
Биологическая очистка. Биологическое окисление осуществляется сообществом микроорганизмов, включающим множество различных бактерий, простейших и ряд более высокоорганизованных организмов, связанных между собой единый комплекс сложными взаимоотношениями. Главенствующая роль в том сообществе принадлежит бактериям.
1. аэробный
2. анаэробный
При термической очистке сжигают, жидки отходы нефтепродуктов и других горючих веществ в печах и горелках.
1.) огневое концентрирование 2). огневое обезвреживание
Большое влияние на биологическое окисление оказывает кислородный режим и наличие токсичных веществ в среде. Токсичное действие на биологические процессы могут оказывать органические и неорганические вещества. Биологическая очистка сточных вод может осуществляться как в естественных условиях (поля орошения, поля фильтрации, биологические пруды), так и в специальных сооружениях (аэротенки – огромные резервуары из железобетона, метантенки).
Использование бактерий для очистки вод.
Органические вещества + O2 + N + Pà(микроорганизмы) + CO2 + H2 + биологически не окисляемые растворимые вещества.
Факторы влияющие на биологическую очистку:
концентрация водородных ионов (pH)
кислородный режим и наличие токсичных веществ в среде
53. Литосфера, её состав и строение.
Земля сформировалась 4,7 млрд. лет назад. Площадь поверхности - 510,2 млн км2, масса - 5976 1021т, средняя плотность—5518 кг/м3.Наша планета состоит из геосфер (концентрических оболочек) – внутренних и внешних.
Внутренние геосферы: ядро, мантия. Мантия делится на нижнюю и верхнюю.
Внешние геосферы: атмосфера, гидросфера, литосфера.
Литосфера – каменная оболочка Земли включающая земную кору толщиной от 6 (под океаном) до 80 км (в горных системах). Земная кора сложена горными породами из которых: 1) более 70% - магматические породы (базальт, гранит, диориты, эффузивы, габбро и т.д.). 2)около 17% - метаморфические, т.е. преобразованные давлением и высокой температурой породы. (кристаллические сланцы,…). 3) более 12% осадочные породы (глина, пески, карбонатные породы). Земная кора – важнейший ресурс для человечества; она содержит:
А) горючие полезные ископаемые (уголь, нефть).
Б) рудные полезные ископаемые (железо, алюминий, и т.д.).
В) нерудные полезные ископаемые (фосфориты, апатиты, и т.д.).
Г) естественные строительные материалы (известняки, гранит, глина, и т.д.).
По физическим свойствам земная кора делится на два типа материковый и океанический. Земная кора материкового типа - равнинных и горных районов - богата кремнием и алюминием, характерными для пород группы гранита. Мощность гранитного слоя увеличивается в горах. Океанический тип земной коры представлен породами типа базальта с преобладанием кремния и магния. Здесь гранитный слой отсутствует, а мощность базальтового слоя доходит до 15 км.






