Диаграмма равновесия (состояния) двухкомпонентных сплавов – это график в координатах: температура (вертикальная ось) – процентное соотношение компонентов (горизонтальная ось). На диаграмме вычерчиваются две вертикальные оси, соответствующие компонентам. На осях указывается масштаб, а на горизонтальной, кроме того (стрелкой) - направление увеличения концентрации одного из компонентов. Компоненты – химические элементы, образующие систему сплавов. Фаза – однородная часть системы, отделенная от других частей границей раздела, при переходе через которую состав и свойства меняются скачком. При рассмотрении процессов кристаллизации (и плавления) и превращений в твердом состоянии могут быть одна жидкая (расплав) и несколько твердых фаз (чистые компоненты, твердые растворы, химические соединения). Однофазные области существования твердых растворов обозначаются греческими буквами α, β, γ, δ и т.д. точки пересечения сплошных линий между собой и с осями обозначаются большими латинскими буквами. Равновесие в нашем случае – это термодинамическое понятие, ранее рассматривавшееся в курсах общей химии и физики.
При анализе диаграмм состояния пользуются правилом фаз: с = к – f + 1, где к – число компонентов, f – число фаз, с – число степеней свободы (в термодинамическом смысле). При постоянном давлении с может принимать значения: 2 (это означает что может меняться и температура и концентрация компонентов), 1 (может меняться или температура, или концентрация компо-нентов), 0 (температура и концентрация компонентов меняться не могут).
Вид диаграммы состояния зависит от характера взаимодействия атомов. В жидком состоянии (в расплаве) атомы имеют высокую кинетическую энергию, легко перемещаются друг относительно друга и свободно перемешиваются. Внутри кристалла атомы находятся в строго определенных положениях и только колеблются вокруг положений равновесия. Перемещения атомов, т.е. диффузия, возможны только при наличии вакансий (для крупных металлических атомов), или по междоузлиям (для мелких атомов легких элементов). Скорость диффузии в кристаллах на порядки медленнее, чем в расплаве.
Повышение температуры приводит к ряду следствий, имеющих в материаловедении очень большое значение. Растет амплитуда колебаний атомов, вследствие чего увеличивается и период кристаллической решетки, т.е. происходит так называемое тепловое расширение. Чем выше температура плавления металла, тем меньше коэффициент теплового расширения. Увеличение периода решетки при росте температуры сопровождается улучшением растворимости инородных атомов при образовании твердых растворов замещения в кристаллической решетке матрицы. Увеличиваются и размеры междоузлий, а соответственно, и растворимость инородных атомов при образовании твердых растворов внедрения. Повышение температуры сопровождается экспоненциальным ростом плотности вакансий, а соответственно, и скорости самодиффузии и гетеродиффузии металлов по вакансионному механизму. Увеличивается скорость диффузии атомов газов и других легких элементов по междоузлиям. Все эти процессы зависят от типа и размеров взаимодействующих атомов.
Полная взаимная растворимость атомов внутри металлического кристалла возможна только при малом различии их диаметров (не более 10%), одинаковом или близком электрон-

 ном строении и одним и тем же типом кристаллической решетки, которые могли-бы образовывать эти элементы при соответствующих температурах самостоятельно. На рис.6.8 показана диаграмма равновесия таких компонентов (сигарообразная диаграмма). Кристаллизация компонентов А и В осуществляется при постоянных температурах А ׳ и В ׳ соответственно. Процесс кристаллизации – экзотермический и идет с выделением тепла. Поэтому на кривых охлаждения мы видим ступеньку. Постоянство температуры кристаллизации компонентов подтверждает и правило фаз: с = к – f + 1. Число компонентов - 1, число фаз – 2 (расплав Ж и кристалл А); с=0, т.е. температура в процессе кристаллизации меняться не может. До и после кристаллизации с=1; появляется одна степень свободы - температура падает.
ном строении и одним и тем же типом кристаллической решетки, которые могли-бы образовывать эти элементы при соответствующих температурах самостоятельно. На рис.6.8 показана диаграмма равновесия таких компонентов (сигарообразная диаграмма). Кристаллизация компонентов А и В осуществляется при постоянных температурах А ׳ и В ׳ соответственно. Процесс кристаллизации – экзотермический и идет с выделением тепла. Поэтому на кривых охлаждения мы видим ступеньку. Постоянство температуры кристаллизации компонентов подтверждает и правило фаз: с = к – f + 1. Число компонентов - 1, число фаз – 2 (расплав Ж и кристалл А); с=0, т.е. температура в процессе кристаллизации меняться не может. До и после кристаллизации с=1; появляется одна степень свободы - температура падает.
Для сплавов процесс кристаллизации осуществляется в интервале температур между линиями ликвидус и солидус. Линия ликвидус на диаграмме равновесия – это геометрическое место точек (А׳- 1- 3- 5- В׳), выше которых все сплавы расплавлены. Линия солидус на диаграмме равновесия – это геометрическое место точек (А׳- 2- 4- 6- В׳), ниже которых все сплавы твердые, кристаллические. Рассмотрим кристаллизацию сплава с концентрацией компонента В, равной n1. Кристаллизация начинается при температурах ниже t1, соответствующей точке 1, находящейся на линии ликвидус. В равновесии с расплавом, соответствующим этой точке, находится твердый раствор замещения α с составом, соответствующим точке 3, находящейся на линии солидус. В равновесии находятся насыщенные между собой расплав и твердый раствор. Внутри однофазных областей растворы не насыщены. Между линиями ликвидус и солидус идет процесс кристаллизации. Здесь присутствуют и жидкая фаза (расплав) и кристаллическая (твердый раствор замещения).
Для формализации процессов кристаллизации (и других типов фазовых превращений на диаграммах равновесия) введен термин конода. Конода – это горизонтальный отрезок, соединяющий концы двухфазной области (в нашем случае – это отрезок 1-2). Концы коноды указывают, какие фазы находятся в равновесии в двухфазной области. Проекции концов коноды на ось концентраций указывают, какие фазы находятся в равновесии в двухфазной области. Точка 1 характеризует расплав с составом n1. Справа-вверх от этой точки располагается однофазная область, соответствующая расплаву. Другой конец коноды – точка 2 прилегает к другой однофазной области, области существования твердого раствора α (слева-вниз). Состав твердого раствора в этой точке – ее проекция на ось концентраций. При описании процессов, происходящих при охлаждении сплава, по достижении расплавом температуры t1 мы обязаны построить коноду, которая покажет, что ниже этой температуры должна начаться кристаллизация твердого раствора. При дальнейшем охлаждении кристаллы будут расти.
 Можно рассчитать объемную долю (а значит и массу) каждой из фаз. Для этого служит правило рычага (правило отрезков). Его действие наглядно показано на рис.6.9. При температуре Т для сплава А0 конода представляет собой отрезок α - S, а проекции концов коноды на ось концентраций дают нам концентрацию этого компонента в расплаве (АS) и твердом растворе (АF). Общая масса сплава W0 должна быть равна сумме масс жидкой (WS) и твердой (WF) фаз: W0 = WS + WF. Масса компонента В в сплаве получается из суммы масс этого компонента в расплаве и твердом растворе. Отсюда следует, что:
Можно рассчитать объемную долю (а значит и массу) каждой из фаз. Для этого служит правило рычага (правило отрезков). Его действие наглядно показано на рис.6.9. При температуре Т для сплава А0 конода представляет собой отрезок α - S, а проекции концов коноды на ось концентраций дают нам концентрацию этого компонента в расплаве (АS) и твердом растворе (АF). Общая масса сплава W0 должна быть равна сумме масс жидкой (WS) и твердой (WF) фаз: W0 = WS + WF. Масса компонента В в сплаве получается из суммы масс этого компонента в расплаве и твердом растворе. Отсюда следует, что:

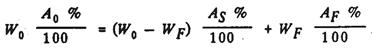
Тогда для массы твердой фазы:

 ,
,
а для массы жидкой фазы: WS = W0 - WF.
 Вернемся к диаграмме равновесия, изображенной на рис.6.8. При температуре t2 состав расплава будет соответствовать точке 3, а твердого раствора – точке 4. Объемная доля этих фаз приб
Вернемся к диаграмме равновесия, изображенной на рис.6.8. При температуре t2 состав расплава будет соответствовать точке 3, а твердого раствора – точке 4. Объемная доля этих фаз приб 

 лизительно одинакова, т.е. закристаллизовалось около половины расплава. При температуре t3 состав расплава будет соответствовать точке 5, а твердого раствора точке 6. Кристаллизация завершается. Запись реакции кристаллизации сплава в развернутом виде представлена ниже.
лизительно одинакова, т.е. закристаллизовалось около половины расплава. При температуре t3 состав расплава будет соответствовать точке 5, а твердого раствора точке 6. Кристаллизация завершается. Запись реакции кристаллизации сплава в развернутом виде представлена ниже. 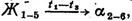 В процессе кристаллизации состав расплава меняется по линии ликвидус (от точки 1 до точки 5), а состав кристаллизующегося твердого раствора – по линии солидус (от точки 2 до точки 6).
В процессе кристаллизации состав расплава меняется по линии ликвидус (от точки 1 до точки 5), а состав кристаллизующегося твердого раствора – по линии солидус (от точки 2 до точки 6).
Следует обратить внимание на изменение состава кристаллов в процессе кристаллизации. Получается, что в момент зарождения кристалла он имел один химический состав, а по мере

 роста он меняется. И меняется не по всему объему, а послойно. Из сопоставления рис.6.10 и 6.11 видно, как меняется состав по сечению растущего кристалла. Явление изменения состава растущего кристалла по сечению называется дендритной ликвацией. Заметим, что реальный состав кристалла несколько отличается от теоретического вследствие различной скорости диффузии атомов. В кристалле диффузия осуществляется медленнее и его состав меняется по линии 2 на рис.3. Интервал кристаллизации расширяется от ΔТ до ΔТ ׳׳.
роста он меняется. И меняется не по всему объему, а послойно. Из сопоставления рис.6.10 и 6.11 видно, как меняется состав по сечению растущего кристалла. Явление изменения состава растущего кристалла по сечению называется дендритной ликвацией. Заметим, что реальный состав кристалла несколько отличается от теоретического вследствие различной скорости диффузии атомов. В кристалле диффузия осуществляется медленнее и его состав меняется по линии 2 на рис.3. Интервал кристаллизации расширяется от ΔТ до ΔТ ׳׳.

 В реальности кристаллы в сплавах имеют дендритное (древовидное) строение (рис.6.12). В соответствии с вышеизложенным, оси дендритов имеют один химсостав, а периферия – другой. На рис.6.13а схематически показано дендритное строение кристаллических зерен сплава, а на рис.6.13б – контуры зерен. Дендритную ликвацию можно устранить термической обработкой – диффузионным отжигом – нагревом слитка до температур ниже линии солидус и выдержкой при этой температуре. При этом взаимная диффузия атомов ускоряется и химический состав выравнивается.
В реальности кристаллы в сплавах имеют дендритное (древовидное) строение (рис.6.12). В соответствии с вышеизложенным, оси дендритов имеют один химсостав, а периферия – другой. На рис.6.13а схематически показано дендритное строение кристаллических зерен сплава, а на рис.6.13б – контуры зерен. Дендритную ликвацию можно устранить термической обработкой – диффузионным отжигом – нагревом слитка до температур ниже линии солидус и выдержкой при этой температуре. При этом взаимная диффузия атомов ускоряется и химический состав выравнивается.
Явление ликвации находит практическое применение при очистке металлов от примесей или нежелательных элементов. Для этого применяется зонная плавка (рис.6.14). Если мы хотим избавиться от компонента В в сплаве, заготовка в виде прутка 4 помещается в узкую цилиндрическую печь 2 длиной ℓ (как правило, индукционную), в которой металл нагревается до расплавления (участок 3). Так как расплав обогащен компонентом В (с концентрацией Св, соответствующей точке Т1 на рис. 3), перемещая печь слева направо мы сдвигаем зону, обогащенную этим компонентов в правую часть заготовки. Повторив этот процесс много раз и отрезов правый конец заготовки мы получим металл А, очищенный от компонента В.

 Один из типов диаграмм равновесия сплавов с полной растворимостью в жидком и частичной – в твердом состоянии - эвтектического типа, приведен на рис. 6.15. Это самый
Один из типов диаграмм равновесия сплавов с полной растворимостью в жидком и частичной – в твердом состоянии - эвтектического типа, приведен на рис. 6.15. Это самый 

 распространенный тип диаграммы равновесия. На диаграмме присутствуют граничные твердые растворы α и β на основе компонентов, прилегающие к вертикальным осям. Они образуются при несоблюдении условий образования непрерывного ряда твердых растворов, т.е. когда атомы компонентов отличаются электронным строением, размерами и типом образуемых кристаллических решеток. Граничные твердые растворы могут образовываться по типу замещения и внедрения (рис.6.16). Растворы внедрения в металлах могут образовывать только атомы легких неметаллических элементов (С, N, O и др.), атомный радиус которых значительно меньше, чем у металла-растворителя. Атомы неметалла располагаются не в узлах, а в междоузлиях решетки металла А. Если для растворов замещения число атомов различного вида в кристаллической решетке постоянно и равно 100%, то для растворов внедрения оно переменно и зависит от количества внедренных атомов. Диаграммы равновесия металлов с легкими неметаллами всегда ограничены справа каким-либо химическим соединением.
распространенный тип диаграммы равновесия. На диаграмме присутствуют граничные твердые растворы α и β на основе компонентов, прилегающие к вертикальным осям. Они образуются при несоблюдении условий образования непрерывного ряда твердых растворов, т.е. когда атомы компонентов отличаются электронным строением, размерами и типом образуемых кристаллических решеток. Граничные твердые растворы могут образовываться по типу замещения и внедрения (рис.6.16). Растворы внедрения в металлах могут образовывать только атомы легких неметаллических элементов (С, N, O и др.), атомный радиус которых значительно меньше, чем у металла-растворителя. Атомы неметалла располагаются не в узлах, а в междоузлиях решетки металла А. Если для растворов замещения число атомов различного вида в кристаллической решетке постоянно и равно 100%, то для растворов внедрения оно переменно и зависит от количества внедренных атомов. Диаграммы равновесия металлов с легкими неметаллами всегда ограничены справа каким-либо химическим соединением.
 Первичная кристаллизация сплава n1 (рис.6.15б), расположенного левее точки e, называемой эвтектической, начинается в точке 5 с образованием твердого раствора α с составом, соответствующим точке 4. Запись этой реакции в развернутом виде:
Первичная кристаллизация сплава n1 (рис.6.15б), расположенного левее точки e, называемой эвтектической, начинается в точке 5 с образованием твердого раствора α с составом, соответствующим точке 4. Запись этой реакции в развернутом виде:  . Следует обратить внимание на то обстоятельство, что в конце первичной кристаллизации состав расплава соответствует эвтектической точке e, а твердого раствора точке a. Можно показать, что и в сплавах, соответствующих линии е-b, например d, при завершении первичной кристаллизации состав расплава также будет соответствовать эвтектической точке е, а состав твердого раствора – точке b.
. Следует обратить внимание на то обстоятельство, что в конце первичной кристаллизации состав расплава соответствует эвтектической точке e, а твердого раствора точке a. Можно показать, что и в сплавах, соответствующих линии е-b, например d, при завершении первичной кристаллизации состав расплава также будет соответствовать эвтектической точке е, а состав твердого раствора – точке b.
 Расплав соответствующий эвтектической точке е, при температуре tе насыщенодновременно относительно твердых растворов α и β в точках αа и βа и находится с ними в равновесии
Расплав соответствующий эвтектической точке е, при температуре tе насыщенодновременно относительно твердых растворов α и β в точках αа и βа и находится с ними в равновесии  . Это - запись реакции эвтектического равновесия. Равновесие является трехфазным, при котором С= 0, и на кривой охлаждения (Рис.6.15б) наблюдается ступенька. Ниже этой температуры начнется реакция двухфазной или эвтектической кристаллизации
. Это - запись реакции эвтектического равновесия. Равновесие является трехфазным, при котором С= 0, и на кривой охлаждения (Рис.6.15б) наблюдается ступенька. Ниже этой температуры начнется реакция двухфазной или эвтектической кристаллизации  . Сплавыс концентрациями а-е называются доэвтектическими, а с концентрациями е - b – заэвтектическими. В доэвтектическом сплаве n1 после окончания первичной кристаллизации присутствует расплав в объеме е - b/а-b. Этот расплав, имеющий эвтектический состав (Же) при эвтектической температуре tе, также находится в условиях эвтектического равновесия и будет кристаллизоваться по эвтектической реакции
. Сплавыс концентрациями а-е называются доэвтектическими, а с концентрациями е - b – заэвтектическими. В доэвтектическом сплаве n1 после окончания первичной кристаллизации присутствует расплав в объеме е - b/а-b. Этот расплав, имеющий эвтектический состав (Же) при эвтектической температуре tе, также находится в условиях эвтектического равновесия и будет кристаллизоваться по эвтектической реакции  . Аналогичная картина будет наблюдаться и у заэвтектических сплавов е - b.
. Аналогичная картина будет наблюдаться и у заэвтектических сплавов е - b.

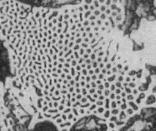


 Эвтектическая кристаллизация – это совместная кристаллизация двух фаз. При кристаллизации эвтектики одна из фаз является ведущей, а другая – ведомой. Так как процесс кристаллизации является диффузионным и требует перемещения атомов, появление кристаллов ведущей фазы тут же вызывает появление рядом кристаллов ведомой фазы. Эти кристаллы одновременно растут, а в расплаве на фронте кристаллизации происходит диффузионное перераспределение атомов компонентов (рис.6.17). Процесс обычно начинается на подложке из уже имеющихся центров кристаллизации: стенках формы, первичных кристаллах, включениях. Из каждого центра кристаллизации растет эвтектическая колония, представляющая собой сильно разветвленные, взаимно проросшие дендриты обеих фаз (рис.6.18). Подложкой для ведомой фазы является ведущая. По существу эвтектическая колония – это двухфазный сросток двух сильно разветвленных кристаллов (бикристалл).
Эвтектическая кристаллизация – это совместная кристаллизация двух фаз. При кристаллизации эвтектики одна из фаз является ведущей, а другая – ведомой. Так как процесс кристаллизации является диффузионным и требует перемещения атомов, появление кристаллов ведущей фазы тут же вызывает появление рядом кристаллов ведомой фазы. Эти кристаллы одновременно растут, а в расплаве на фронте кристаллизации происходит диффузионное перераспределение атомов компонентов (рис.6.17). Процесс обычно начинается на подложке из уже имеющихся центров кристаллизации: стенках формы, первичных кристаллах, включениях. Из каждого центра кристаллизации растет эвтектическая колония, представляющая собой сильно разветвленные, взаимно проросшие дендриты обеих фаз (рис.6.18). Подложкой для ведомой фазы является ведущая. По существу эвтектическая колония – это двухфазный сросток двух сильно разветвленных кристаллов (бикристалл).



 Существует несколько типов эвтектик. На металлографическом шлифе, представляющем собой сечение эвтектики, округлые выделения столбчатой эвтектики (Рис. 6.19). При эвтектической кристаллизации сплавов, прилегающих к точкам а и b на рис.6.15, когда доля оставшегося расплава мала и он сосредоточен на границах первичных кристаллов, формируется так называемая вырожденная эвтектика, одна составляющая которой сливается с первичным дендритом, а вторая представляет собой разветвленный дендрит на поверхности последнего (рис.6.20). Вырожденная эвтектика несмотря на свой небольшой объем существенно снижает прочность из-за ослабления границ зерен. На рис.6.21 показан излом стального образца при хрупком межзеренном разрушении в присутствии вырожденной эвтектики.
Существует несколько типов эвтектик. На металлографическом шлифе, представляющем собой сечение эвтектики, округлые выделения столбчатой эвтектики (Рис. 6.19). При эвтектической кристаллизации сплавов, прилегающих к точкам а и b на рис.6.15, когда доля оставшегося расплава мала и он сосредоточен на границах первичных кристаллов, формируется так называемая вырожденная эвтектика, одна составляющая которой сливается с первичным дендритом, а вторая представляет собой разветвленный дендрит на поверхности последнего (рис.6.20). Вырожденная эвтектика несмотря на свой небольшой объем существенно снижает прочность из-за ослабления границ зерен. На рис.6.21 показан излом стального образца при хрупком межзеренном разрушении в присутствии вырожденной эвтектики.
На рис. 6.22 приведен пример структуры сплавов свинец – сурьма, образующих механические смеси из чистых компонентов при различных содержаниях сурьмы.





а б в г д
Рис. 6.22. Структура сплавов свинец-сурьма, × 100:
а – чистый свинец; б ‑ 6% Sb (доэвтектический сплав); в – 13 % Sb (эвтектический сплав): г – 30 %Sb (заэвтектический сплав); д – чистая сурьма.
Перитектическая кристаллизация.
Приведенная на рис. 6.15 диаграмма равновесия соответствует случаю, когда добавление атомов каждого из компонентов А или В снижает температуры начала и конца кристаллизации граничных твердых растворов α и β. Однако, бывают случаи, когда один из компонентов, например А, снижает температуры начала и конца кристаллизации твердого раствора β, акомпонент В повышает температуры начала и конца кристаллизации твердого раствора α. Диаграмма равновесия таких сплавов приведена на рис. 6.23а. Здесь расплав (жидкая фаза) оказывается в перитектическом  равновесии с этими твердыми растворами. Точку р, в которой пересекаются линии ликвидуса А ׳ –р для твердого раствора α и В ׳ –р – для твердого раствора β, а также горизонталь р-а-b
равновесии с этими твердыми растворами. Точку р, в которой пересекаются линии ликвидуса А ׳ –р для твердого раствора α и В ׳ –р – для твердого раствора β, а также горизонталь р-а-b 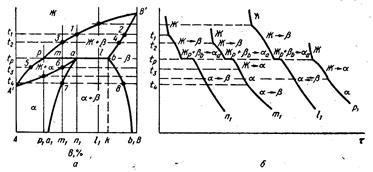 называют перитектическими. Особенностью такой диаграммы является то, что перитектическая точка р, в отличие от эвтектической, находится в стороне от точек а и b максимальной взаимной растворимости компонентов в твердом состоянии. Поэтому перитектическая реакция в сплавах на участке р-а-b -
называют перитектическими. Особенностью такой диаграммы является то, что перитектическая точка р, в отличие от эвтектической, находится в стороне от точек а и b максимальной взаимной растворимости компонентов в твердом состоянии. Поэтому перитектическая реакция в сплавах на участке р-а-b -  не носит характера кристаллизации расплава с образованием смеси двух типов кристаллов, как при эвтектической кристаллизации, а заключается во взаимодействии расп-лава состава Жр с ранее выпавшими первичными
не носит характера кристаллизации расплава с образованием смеси двух типов кристаллов, как при эвтектической кристаллизации, а заключается во взаимодействии расп-лава состава Жр с ранее выпавшими первичными  кристаллами βb, в результате чего образуются новые αа- кристаллы (смотри кривую охлаждения сплава n1 на рис. 6.23б). Другими словами, кристаллы βb растворяются в жидкости с одновременным образованием кристаллов αа.
кристаллами βb, в результате чего образуются новые αа- кристаллы (смотри кривую охлаждения сплава n1 на рис. 6.23б). Другими словами, кристаллы βb растворяются в жидкости с одновременным образованием кристаллов αа.
 В сплавах, расположенных левее и правее точки а, результат перитектического превращения отличается. В сплавах, с концентрациями, между точками р и а, например m1, будет оставаться расплав в объеме, соответствующем отрезку m-а, а в сплавах с концентрациям, между точками а и b, например ℓ1, будет сохраняться часть первичного твердого раствора β в объеме, соответствующем отрезку а-ℓ. Кривые охлаждения соответствующих сплавов приведены на рис 6.23б. Перитектическое превращение протекает на границе между расплавом и первичными кристаллами β, где образуется прослойка перитектической фазы α (смотри схему на рис. 6.24). Процесс идет до полного исчезновения расплава и первичных кристаллов (сплав а), до исчерпания расплава (сплавы а – b) или до исчерпания первичных кристаллов (сплавы а – р).
В сплавах, расположенных левее и правее точки а, результат перитектического превращения отличается. В сплавах, с концентрациями, между точками р и а, например m1, будет оставаться расплав в объеме, соответствующем отрезку m-а, а в сплавах с концентрациям, между точками а и b, например ℓ1, будет сохраняться часть первичного твердого раствора β в объеме, соответствующем отрезку а-ℓ. Кривые охлаждения соответствующих сплавов приведены на рис 6.23б. Перитектическое превращение протекает на границе между расплавом и первичными кристаллами β, где образуется прослойка перитектической фазы α (смотри схему на рис. 6.24). Процесс идет до полного исчезновения расплава и первичных кристаллов (сплав а), до исчерпания расплава (сплавы а – b) или до исчерпания первичных кристаллов (сплавы а – р).


 Диаграммы равновесия сплавов, образующих промежуточные твердые фазы (Рис. 6.25). Промежуточными называются все твердые фазы, которые образуются в интервале концентраций между компонентами А и В и отделены от граничных твердых растворов на основе
Диаграммы равновесия сплавов, образующих промежуточные твердые фазы (Рис. 6.25). Промежуточными называются все твердые фазы, которые образуются в интервале концентраций между компонентами А и В и отделены от граничных твердых растворов на основе
 |
компонентов двухфазными областями. Как правило, это химические соединения. Для промежуточных фаз характерна своя кристаллическая решетка, отличная от кристаллических решеток компонентов. Пример кристаллической решетки химсоединений приведен на рис.6.26. В ней можно выделить подрешетки, образованные атомами одного сорта. В сплавах могут образовываться твердые растворы на основе химсоединений.
Различают различные типы интерметаллидов (соединения металлов с металлами – электронные соединения, фазы Лавеса, Сигма-фазы и др.), соединения с нормальной валентностью, которые образуются между металлами и элементами, проявляющими и металлические и неметаллические свойства (например, полупроводниковые), фазы внедрения. Последние образуются между металлами и неметаллами с малым атомным радиусом (углерод, азот, бор и др.). Кристаллическую структуру фаз внедрения определяет размерный фактор. При Rx /RMe ≤ 0.59 (здесь Rx и RMe радиусы атомов неметалла и металла соответственно) образуется простая кубическая решетка (как, например, на рис.6.26). Если это соотношение больше, чем 0.59, то кристаллическая решетка сложная с большим количеством атомов. На рис.6.25 показаны основные типы диаграмм равновесия, образуемых компонентами, у которых образуются химические соединения, устойчивые во всем интервале кристаллизации. В таких сплавах химическое соединение можно рассматривать как компонент. В этом случае справа и слева от химсоединения АmBn будут располагаться диаграммы равновесия уже известных нам типов. На рис.6.25а приведена диаграмма равновесия сплавов с компонентами, которые практически не растворяются друг в друге. Такие диаграммы образуются между металлами и элементами, проявляющими и металлические и неметаллические свойства, а химсоединение часто представляет собой полупроводниковую фазу.
 На рис.6.25б представлена диаграмма равновесия, на которой представлены широкие области твердых растворов на основе компонентов (α и β) и большая область растворимости компонентов γ на основе химсоединения АmBn (заштриховано). Слева от пунктирной линии в заштрихованной области располагаются твердые растворы замещения компонента В атомами компонента А в подрешетке В химсоединения АmBn. Справа от пунктирной линии, наоборот, располагаются твердые растворы замещения компонента А атомами компонента В в подрешетке А химсоединения. Такие диаграммы равновесия образуют компоненты металлических атомов.
На рис.6.25б представлена диаграмма равновесия, на которой представлены широкие области твердых растворов на основе компонентов (α и β) и большая область растворимости компонентов γ на основе химсоединения АmBn (заштриховано). Слева от пунктирной линии в заштрихованной области располагаются твердые растворы замещения компонента В атомами компонента А в подрешетке В химсоединения АmBn. Справа от пунктирной линии, наоборот, располагаются твердые растворы замещения компонента А атомами компонента В в подрешетке А химсоединения. Такие диаграммы равновесия образуют компоненты металлических атомов.
 Третий вариант, представленный на рис. 6.25в, интересен тем, что область γ -растворов располагается только слева от ординаты химического соединения АmBn. Такие области гомогенности характерны для фаз внедрения. В данном случае промежуточная γ -фаза представляет собой твердый раствор вычитания неметаллического компонента В в соединении АmBn за счет существования большого количества вакансий в подрешетке последнего. За счет этого наблюдается избыток атомов металлического компонента А по сравнению со стехиометрическим составом. В то же время со стороны неметаллического компонента В твердый раствор отсутствует, т.к. все узлы заполняются только по достижении стехиометрии.
Третий вариант, представленный на рис. 6.25в, интересен тем, что область γ -растворов располагается только слева от ординаты химического соединения АmBn. Такие области гомогенности характерны для фаз внедрения. В данном случае промежуточная γ -фаза представляет собой твердый раствор вычитания неметаллического компонента В в соединении АmBn за счет существования большого количества вакансий в подрешетке последнего. За счет этого наблюдается избыток атомов металлического компонента А по сравнению со стехиометрическим составом. В то же время со стороны неметаллического компонента В твердый раствор отсутствует, т.к. все узлы заполняются только по достижении стехиометрии.
На рис. 6.27 показаны диаграммы равновесия сплавов с компонентами, образующими химическое соединение, устойчивое при температурах ниже линии ликвидус. Здесь образование химического соединения происходит фактически по перитектической реакции. На рис.6.27б – это реакция  . Здесь γ представляет собой твердый раствор замещения на основе химического соединения АmBn.
. Здесь γ представляет собой твердый раствор замещения на основе химического соединения АmBn.






