
Ф - формальдегид, ВВ - взвешенные вещества, БП - бенз(а)пирен, HF - фторид водорода, NO - оксид азота, NO2 - диоксид азота, CS2 - сероуглерод, NH3 - аммиак, НС1 - хлористый водород, ЭБ - этилбензол.
Поступление бенз(а)пирена на европейскую территорию России обусловлено работой региональных источников (автотранспорт, металлургия, ТЭС и т.п.) и трансграничным переносом из сопредельных стран Европы (Польша, Украина, Белоруссия, прибалтийские страны).
Значительно загрязнение атмосферного воздуха тяжелыми металлами (кадмий, ртуть, свинец). Уровень загрязнения воздуха тяжелыми металлами обычно характеризуют показателем поступления (выпадения) этих веществ в почву.
Фотохимический смог. Общая схема реакций образования фотохимического смога в городах сложна и в упрощенном виде может быть представлена реакциями
NO2 + hv → NO + О
О + О2 → О3
……………………
CnHm + О }
CnHm + О3 } ПАН (пероксиацилнитраты)
Смог весьма токсичен, так как его составляющие обычно находятся в пределах: О3 - 60-75%; ПАН, Н2О2, альдегиды и др. - 25-40%.
Для образования смога в атмосфере в солнечную погоду необходимо наличие оксидов азота и углеводородов (их выбрасывают в атмосферу автотранспорт, промышленные предприятия). Характерное распределение концентрации фотохимического смога относительно времени суток показано на рис. 2.23.
Фотохимические смоги, впервые обнаруженные в 1940-х гг. в Лос-Анджелесе, теперь периодически наблюдаются и в других городах мира.
Кислотные дожди известны более 100 лет, однако проблема этих дождей возникла около 35 лет назад.
Источниками кислотных дождей служат газы, содержащие серу и азот. Наиболее важные из них: SO2, NOx, H2S. Кислотные дожди возникают вследствие неравномерного распределения этих газов в атмосфере. Например, концентрация SO2 (мкг/м3) обычно такова: в городе 50-1000, на территории в радиусе около 50 км вокруг города – 10-50, в радиусе около 150 км - 0,1-2, над океаном - 0,1.
Основными реакциями в атмосфере являются:
• вариант 1: SO2 + ОН → HSO3; HSO3 + ОН → H2SO4 (молекулы в атмосфере быстро конденсируются в капли);

Рис. 2.23. Относительные концентрации NO2 и О3 в атмосферном воздухе
• вариант 2: SO2 + Hv → SO2* (активированная молекула диоксида серы); SO2 +О2 → SO4; SO4 + О2 → SO3 + О3; SO3 + Н2О → H2SO4.
Реакции обоих вариантов в атмосфере идут одновременно. Для сероводорода характерна реакция H2S + О2 → SO2 + Н2О и далее 1 или 2 вариант реакции.
Источники поступления соединений серы в атмосферу:
• естественные (вулканическая деятельность, действия микроорганизмов и др.) – 31-41%;
• антропогенные (ТЭС, промышленность и др.) – 59-69%.
Всего в окружающую среду поступает 91-112 млн. т соединений серы в год.
Концентрации соединений азота составляют: в городе 10-100 мкг/м3, на территории в радиусе 50 км вокруг города 0,25-2,5 мкг/м3, над океаном 0,25 мкг/м3.
Из соединений азота основную долю кислотных дождей дают NO и NO2. В атмосфере возникают реакции: 2NO + О2 → 2NO2, NO2 + ОН → HNO3. Источники соединений азота:
• естественные (почвенная эмиссия, грозовые разряды, горение биомассы и др.) - 63%;
• антропогенные (ТЭС, автотранспорт, промышленность) - 37%.
Всего в окружающую среду поступает 51-61 млн. т соединений азота в год.
 Серная и азотная кислоты поступают в атмосферу также в виде тумана и паров от промышленных предприятий и автотранспорта. В городах их концентрация достигает 2 мкг/м3.
Серная и азотная кислоты поступают в атмосферу также в виде тумана и паров от промышленных предприятий и автотранспорта. В городах их концентрация достигает 2 мкг/м3.
Соединения серы и азота, попавшие в атмосферу, вступают в химическую реакцию не сразу, сохраняя свои свойства соответственно в течение 2 и 8-10 суток. За это время они могут вместе с атмосферным воздухом пройти расстояния до 2000 км и лишь после этого выпадают с осадками на земную поверхность.
Различают два вида седиментации: влажную и сухую. Влажная - это выпадение кислот, растворенных в капельной влаге, она возникает при влажности воздуха 100,5%; сухая реализуется в тех случаях, когда кислоты присутствуют в атмосфере в виде капель диаметром около 0,1 мкм. Скорость седиментации в этом случае весьма мала, и капли могут проходить большие расстояния (следы серной кислоты обнаружены даже на Северном полюсе). В нашей стране повышенная кислотность осадков (рН = 4-5,5) отмечается в отдельных промышленных регионах. Наиболее неблагополучны города Тюмень, Тамбов, Архангельск, Северодвинск, Вологда, Петрозаводск, Омск и др. Плотность выпадения осадков серы, превышающая 4 т/км2 в год, зарегистрирована в 22 городах страны, а более 8-12 т/км2 в год в городах Алексин, Новомосковск, Норильск, Магнитогорск.
Парниковый эффект. Возникновение глобального парникового эффекта также связано с поступлением в атмосферу различных газовых примесей.
Суть парникового эффекта заключается в том, что Земля поглощает солнечное излучение (преимущественно в видимом диапазоне) и испускает теплоту в инфракрасном диапазоне. Главными поглотителями теплового излучения от земной поверхности служат диоксид углерода, метан и некоторые другие атмосферные примеси. Эти атмосферные примеси действуют подобно прозрачной крыше парника, пропуская к Земле коротковолновую часть спектра и задерживая у Земли длинноволновое тепловое излучение. Отсюда и их название - парниковые газы. Чем выше их концентрация в атмосфере, тем выше парниковый эффект.
Рост содержания СО2 в атмосфере обусловлен потреблением углеводородных топлив - газа, нефти, угля. Другой источник СО2 связан с изменениями растительного и почвенного покрова континентов. Вырубка лесов, а также распашка целинных земель и общая интенсификация земледелия приводят к более быстрому извлечению углерода из гумуса почв. За последние 100 лет сжигание топлива дало выброс углерода в среднем около 168 гт, а эмиссия вследствие изменения растительности континентов и необратимого нарушения почвенного покрова за это же время оценивается средней величиной 68 гг.
Основным каналом стока избыточного углерода из атмосферы является Мировой океан. Около 60% углерода поглощается океанами, а остальное количество - биотой континентов. Современная человеческая деятельность вносит значительные изменения в функционирование морских экосистем, через несколько десятилетий Мировой океан из-за загрязнения будет поглощать избыточный углерод менее эффективно и доля остающегося в атмосфере СО2 станет выше.
Метан поступает в атмосферу из природных (донные отложения водоемов и болот) и техногенных источников (сельскохозяйственное производство, свалки бытовых отходов).
Техногенные источники закиси азота N2O связаны в основном с высокотемпературным окислением молекулярного азота в процессе горения различных топлив. В естественных условиях N2O поступает в атмосферу из почв, лесов и при грозовых разрядах.
Из-за высокой химической инертности и малой растворимости в воде среднее время жизни NO2 в атмосфере велико и составляет 120-150 лет.
Увеличение концентрации диоксида углерода в атмосфере особенно интенсивное в последние годы, приводит к росту эффективности поглощения инфракрасного излучения, в результате чего температура земли возрастает (рис. 2.24). К повышению температуры может привести и увеличение концентрации в атмосфере таких газов, как О3, CH4, N2O, NO2, SO2, фреонов.
Структура выбросов парниковых газов в России (рис. 2.25) более чем на 70% определяется сжиганием углеводородного топлива в энергетике, промышленности и жилищно-коммунальном хозяйстве.
В 1995 г. по общему объему выбросов СО2 на душу населения Россия занимала пятое место в мире после СЩА, Кана 


 ды, Австралии и Новой Зеландии. Сегодня на долю главного
ды, Австралии и Новой Зеландии. Сегодня на долю главного
парникового газа – CO2 приходится около 80% парникового эффекта, около 10% дает метан, на вклад остальных газов закиси азота, фреонов) приходится остальное.

Рис. 2.24. Изменение средней концентрации углекислого газа в атмосфере Земли

Рис.2.25. Структура выбросов парниковых газов в России
По причине резкого спада промышленного производства России в период с 1990 по 1999 г. почти на треть сократились и выбросы парниковых газов (рис. 2.26). Однако вследствие экономического роста выбросы парниковых газов наминая с 2000 г. медленно нарастают.
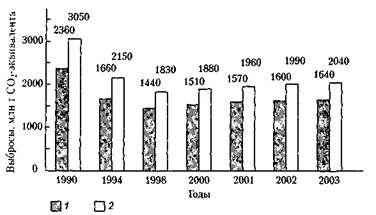
Рис. 2.26. Техногенные выбросы парниковых газов (СО2 — эквивалент в год):
1 - СО2, 2 - все парниковые газы
Разрушение озонового слоя. Озоновым слоем называют область атмосферы, расположенную на высотах от 18 км (в полярных областях - от 10 км) до 45 км и характеризующуюся повышенным содержанием озона. Поглощение озоновым слоем большей части биологически активного ультрафиолетового излучения Солнца с длиной волны λ < 310 нм и перевод его в теплоту играет важнейшую роль в сохранении жизни на Земле. Во-первых, озон является единственным компонентом атмосферного воздуха, защищающим все живое на суше от губительных доз ультрафиолетового облучения в диапазоне длин волн λ = 240-310 нм. Во-вторых, нагревая атмосферу, озоновый слой ограничивает глобальные циркуляции воздуха тропосферой, принимая тем самым непосредственное участие в формировании погоды и климата на Земле. Равновесие между процессами образования и разрушения озона нарушается при изменении солнечной активности, а также при появлении в озоновом слое веществ - катализаторов разложения озона. Среди таких катализаторов важнейшая роль принадлежит оксидам азота:
NO + O3 → NO2 + O2
NO2 + О → NO + O2,
атомам хлора:
Cl + O3 → CIO + O2,
а также НО'-радикалам:
НО' + O3 → O2 + 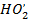 (гидропероксидный радикал).
(гидропероксидный радикал).
По теоретическим оценкам, в результате протекания цепных каталитических реакций одна молекула NO разрушает до 10-12 молекул О3. Однако антропогенные выбросы NO в приземном слое существенной опасности для озонового слоя не представляют, так как за время, необходимое для подъема молекул NO на высоту 25-35 км, составляющее, по оценкам, от 30 до 120 лет, оксид азота разрушается, вступая в химические реакции с другими веществами. Более опасна эмиссия оксида азота непосредственно в озоновом слое или в близлежащих областях из двигательных установок баллистических ракет и высотных реактивных самолетов.
Однако несравнимо большую опасность для озона представляет атомарный хлор. Согласно расчетам, один атом хлора по цепной каталитической реакции разрушает до 105 молекул Оз. В настоящее время выявлено два основных источника поступления атомарного хлора в стратосферу. Первый из них связан с непосредственной эмиссией хлора в озоновый слой при запусках твердотопливных баллистических ракет и космических аппаратов типа американского «Шаттла», использующих смесевые топлива на основе перхлоратов, например перхлората аммония NH4C1O4, суммарные выбросы хлора в атмосферу при эпизодических запусках ракет и космических аппаратов невелики и оцениваются сотнями тонн в год.
Гораздо более мощным источником поступления хлора в атмосферу является производство фторхлоруглеродов.
Фторхлоруглеводороды (фреоны) с середины 1930-х гг. находят широкое применение в промышленности. Фреон-11 и фреон-12 использовались в качестве вспенивателей при получении пористых полимерных материалов, наполнителей в аэрозольных упаковках, а также хладагентов в холодильниках и кондиционерах.
Во второй половине 1980-х гг. во многих промышленно развитых странах были введены ограничения на производство и потребление этой продукции в связи с достигнутыми международными договоренностями о постепенном отказе от использования фторхлоруглеродов.
Однако концентрации фреонов в атмосфере будут увеличиваться еще долгие годы даже после полного прекращения их производства, поскольку среднее время пребывания фреона-11 и фреона-12 в атмосфере оценивается примерно в 55-120 лет. Кроме того, значительные концентрации фреонов 11 и 12 и некоторых других соединений этого класса были зарегистрированы в газовых выбросах действующих вулканов и гидротермальных источников в сейсмически активных районах.
В 1986 г. в мире было произведено 700 тыс. т этих веществ, а всего с начала их массового производства в 1960-х гг. - около 5 млн. т. Благодаря своей высокой химической стойкости хлорфторуглероды в процессе многолетней циркуляции с воздухом поступают из приземных слоев атмосферы в озоновый слой, где подвергаются фотодиссоциации с выделением атомарного хлора.
Еще большую опасность для озонового слоя по сравнению с хлорфторуглеродами представляют бромсодержащие фреоны СF2ОВг и С2F2Вr2, применяемые в пожаротушении. Атомы брома в несколько раз активнее разрушают озоновый слой, по сравнению с хлором.
При истощении озонового слоя возрастает доза облучения человека ультрафиолетовыми лучами, что ведет к росту заболеваний катарактой, кожными заболеваниями, ослаблению иммунной системы организма, повреждению молекул ДНК, передающих генетическую информацию. Наибольшую опасность представляет рост заболеваемости злокачественной меланомой (раком кожи). Согласно медицинским данным истощение озонового слоя на 1% сопровождается ростом заболеваемости меланомой на 6%.
Увеличение ультрафиолетовой радиации представляет опасность для всех живых организмов на суше и в воде. Высокие дозы этого излучения за счет действия на ДНК могут вызвать мутации у микроорганизмов, привести к ухудшению качества семян, понижению сопротивляемости растений вредителям и болезням. Установлено, что ультрафиолетовые лучи вызывают повреждение клеток и тканей у растений. По расчетам, потеря 25% озона вызовет такой рост радиации, что количество фитопланктона в океане сократится на 35% с соответствующим уменьшением его продуктивности. Истощение озонового слоя оказывает негативное влияние и на климат Земли: ведет к снижению нагрева стратосферы с соответствующим изменением характера поведения температуры воздуха в этой области и нарушением циркуляции воздушных масс в тропосфере.
Данные оценки потерь озона в Арктике весьма противоречивы. Согласно данным спутникового наблюдения к 1981 г. истощение озонового слоя составило 1%, а за семилетний период с 1981 по 1988 г. - 4%. К 2050 г. ожидается 30-50%-ное истощение озонового слоя. По другим данным, к 2015 г. истощение озонового слоя достигнет 17% и затем стабилизируется на этом уровне.
В результате техногенного воздействия на атмосферу наблюдаются следующие негативные последствия:
• превышение ПДК многих токсичных веществ (СО, NO2, SO2, СnНm, бенз(а)пирена, свинца, бензола и др.) в городах и природных зонах;
• образование в городах фотохимического смога при интенсивных выбросах NOx, СnНm;
• выпадение кислотных дождей в регионах при интенсивных выбросах SOx, NOx;
• проявление парникового эффекта при повышенном содержании СО2, N0x, О3, СН4 в атмосфере, что способствует повышению ее средней температуры;
• разрушение озонового слоя при поступлении в него NOx и соединений хлора, что создает опасность УФ-облучения биосферы.
Воздействие на гидросферу. Гидросфера - водная среда Земли, образованная совокупностью океанов, морей, поверхностных вод суши, включая лед и снег высокогорных и полярных районов. Гидросфера на 94% состоит из вод океанов и морей, 0,03% - поверхностные воды, 4% - подземные воды, 2% - снег и льды.
В структуре забора воды из природных источников преобладает вид деятельности по производству и распределению электроэнергии, газа и воды. Его доля в 2006 и 2007 гг. составила 54%, а в 2008 г. - 56%. На сельское хозяйство, охоту и лесное хозяйство приходится около 23-24%, на обрабатывающее производство – 7-8% общего забора воды из природных источников в целом по России.
Состав основных веществ, загрязняющих воды, приведен в табл. 2.21.
Таблица 2.21






