1. Возбуждающие.
2. Тормозные.
Проведение воз-я по меж/кл контактам:
21.Обычно тормозными являются глицинергические (медиатор — глицин) и ГАМК-ергические синапсы (медиатор — гамма-аминомасляная кислота).
Тормозные синапсы бывают двух видов:
1) синапс, в пресинаптических окончаниях которого выделяется медиатор, гиперполяризующий постсинаптическую мембрану и вызывающий возникновение тормозного постсинаптического потенциала;
2) аксо-аксональный синапс, обеспечивающий пресинаптическое торможение. Синапс холинергический (s. cholinergica) — синапс, медиатором в котором является ацетилхолин.
В некоторых синапсах присутствует постсинаптическое уплотнение — электронно-плотная зона, состоящая из белков. По её наличию или отсутствию выделяют синапсы асимметричные и симметричные. Известно, что все глутаматергические синапсы асимметричны, а ГАМКергические — симметричны.
22.Медиатор – это группа химических веществ, которая принимает участие в передаче возбуждения или торможения в химических синапсах с пресинаптиче-ской на постсинаптическую мембрану. Критерии, по которым вещество относят к группе медиаторов:
1) вещество должно выделяться на пресинаптиче-ской мембране, терминали аксона;
2) в структурах синапса должны существовать ферменты, которые способствуют синтезу и распаду медиатора, а также должны быть рецепторы на постсинаптической мембране;
3) вещество, претендующее на роль медиатора, должно при передавать возбуждение с пресинаптиче-ской мембраны на постсинаптическую мембрану.
Классификация медиаторов:
1) химическая, основанная на структуре медиатора;
2) функциональная, основанная на функции медиатора.
Химическая классификация:
1. Сложные эфиры – ацетилхолин (АХ).
2. Биогенные амины:катехоламины (дофамин, норадреналин (НА), адреналин (А)); серотонин;гистамин.
3. Аминокислоты: гаммааминомасляная кислота (ГАМК);глютаминовая кислота; глицин; аргинин.
4. Пептиды:
1) опиоидные пептиды: метэнкефалин; энкефалины; лейэнкефалины;
2) вещество «P»;
3) вазоактивный интестинальный пептид;
4) соматостатин.
5. Пуриновые соединения: АТФ.
6. Вещества с минимальной молекулярной массой: NO;CO.
Функциональная классификация:
1. Возбуждающие медиаторы:
1) АХ;
2) глютаминовая кислота;
3) аспарагиновая кислота.
2. Тормозящие медиаторы, вызывающие гиперполяризацию постсинаптической мембраны, после чего возникает тормозной постсинаптический потенциал, который генерирует процесс торможения:
1) ГАМК;
2) глицин;
3) вещество «P»;
4) дофамин;
5) серотонин;
6) АТФ.
23. Нейромедиаторы – биологически активные химические вещества, с помощью которых осуществляется передача электрического импульса с нервной клетки между нейронами через синаптическое пространство.
Нейромедиатор - биологически активное вещество:
- выделяемое нервными окончаниями;
- способное реагировать со специфическими рецепторами клеточной мембраны и изменять ее проницаемость для определенных ионов, вызывая возникновение потенциала действия (активного электрического сигнала).
Нейромедиатор участвует в передаче нервных импульсов с нервного окончания на рабочий орган и с одной нервной клетки на другую. Нейромедиаторы делят на три группы: аминокислоты, пептиды, моноамины
Адреналин, норадреналин и дофамин. Их биологическая активность заключается в способности воздействовать на функциональное состояние органов и систем, а также на интенсивность метаболических процессов в тканях.
Адреналин (эпинефрин) – гормон мозгового вещества надпочечников, синтезируется, в основном, в хромаффинных клетках мозгового вещества надпочечников из дофамина и норадреналина. Поступая в кровоток, он действует на клетки отдаленных органов. Уровень адреналина в крови характеризует гуморальную часть симпатической нервной системы. Секреция адреналина и выброс его в кровь усиливаются в тех случаях, когда необходима срочная адаптивная перестройка обмена веществ.
Плазменный норадреналин происходит из симпатических нервных окончаний. Значительная его часть поглощается нейронами, а 10-20% - попадает в кровь. Только очень небольшая часть норадреналина в крови происходит из мозгового слоя надпочечников. Норадреналин отличается от адреналина более сильным сосудосуживающим действием, меньшим стимулирующим влиянием на сокращение сердца, слабым влиянием на обмен веществ (отсутствие выраженного гипергликемического эффекта). Уровень норадреналина в крови характеризует активность нейронов симпатической нервной системы.
Дофамин – медиатор симпатоадреналовой системы, один из медиаторов возбуждения в синапсах ц. н.с., биосинтетический предшественник норадреналина и адреналина. Дофамин синтезируется в хромаффинных клетках тканей человека и высших животных из диоксифенилаланина — ДОФА. Важную роль в синтезе и секреции дофамина играет активность обратного нейронального захвата дофамина, секретированного в синаптическую щель. Этот процесс может блокироваться фенамином, антихолинергическими и антигистаминными препаратами, некоторыми веществами, применяемыми для лечения паркинсонизма. Дофамин участвует в регуляции секреции катехоламинов.
Дофамин вызывает повышение сердечного выброса, расширение кровеносных сосудов почек и усиление почечного кровотока, увеличение клубочковой фильтрации, диуреза, экскреции с мочой калия и натрия, улучшает кровоток в брыжеечных и венечных сосудах сердца, способен оказывать и сосудорасширяющее действие. Стимулируя гликогенолиз и подавляя утилизацию глюкозы тканями, дофамин вызывает повышение концентрации глюкозы в крови. Он стимулирует образование соматотропного гормона и его концентрацию в крови, но тормозит секрецию пролактина. Недостаточный синтез дофамина обусловливает нарушение двигательной функции – синдром паркинсонизма и гиперкинезы. При гиповитаминозе В6, наблюдающемся, например, при хроническом алкоголизме, в тканях головного мозга увеличивается содержание дофамина, появляются его метаболиты, которые отсутствуют в норме.
Серотонин – биогенный амин, один из основных нейромедиаторов в ЦНС, контролирующий аппетит, сон, настроение и эмоции человека. Физиологические функции серотонина чрезвычайно многообразны. При снижении серотонина повышается чувствительность болевой системы организма, то есть даже самое слабое раздражение отзывается сильной болью. Серотонин облегчает двигательную активность, участвует в регуляции сосудистого тонуса. Наряду с дофамином этот нейромедиатор участвует в механизмах гипоталамической регуляции гормональной функции гипофиза.
Серотонин играет важную роль в процессах свёртывания крови. Тромбоциты крови содержат значительные количества серотонина и обладают способностью захватывать и накапливать серотонин из плазмы крови. Серотонин повышает функциональную активность тромбоцитов и их склонность к агрегации и образованию тромбов. Выделение серотонина из повреждённых тканей является одним из механизмов обеспечения свёртывания крови по месту повреждения.
Серотонин участвует в процессах аллергии и воспаления. Он повышает проницаемость сосудов, усиливает хемотаксис и миграцию лейкоцитов в очаг воспаления, увеличивает содержание эозинофилов в крови, усиливает высвобождение других медиаторов аллергии и воспаления. Также большое количество серотонина производится в кишечнике. Серотонин играет важную роль в регуляции моторики и секреции в желудочно-кишечном тракте, усиливая его перистальтику и секреторную активность. Кроме того, серотонин играет роль фактора роста для некоторых видов симбиотических микроорганизмов, усиливает бактериальный метаболизм в толстой кишке. Сами бактерии толстой кишки также вносят некоторый вклад в секрецию серотонина кишечником, поскольку многие виды симбиотических бактерий обладают способностью декарбоксилировать триптофан. При дисбактериозе и ряде других заболеваний толстой кишки продукция серотонина кишечником значительно снижается. Массивное высвобождение серотонина из погибающих клеток слизистой желудка и кишечника при воздействии цитотоксических химиопрепаратов является одной из причин возникновения тошноты и рвоты, диареи при химиотерапии злокачественных опухолей.
2)Нейромодуляторы, нейроактивные пептиды, или нейропептиды - вещества, модулирующие функцию нейрона. Синаптические модуляторы - вещества, модулирующие передачу информации в синапсах.
Классификация мышц
Мышцы человека классифицируют по форме, положению на теле, направлению волокон, выполняемой функции, по отношению к суставам и др.
| По форме | По отношению к суставам | По расположению в теле человека | По направлению волокон | По выполняемой функции | По отношению к частям тела |
| Длинные Короткие Широкие | Односуставные Двусуставные Многосуставные Сгибатели Разгибатели Отводящие Приводящие Супинаторы Пронаторы Сфинктеры Расширители | Поверхностные Глубокие | Круговые Параллельные Лентовидные Веретенообразные Зубчатые Косые 1)однопе ристые; 2)двуперистые; 3) многоперистые | Дыхательные Жевательные Мимические | Головы Шеи Туловища: 1) груди; 2) спины; 3) живота Конечнос тей: 1) верхних; 2)нижних |
Форма мышц может быть очень разнообразной, она зависит от расположения мышечных волокон к сухожилию. 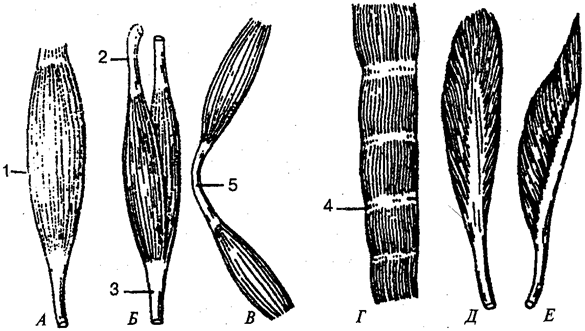
Строение скелетных мышц
Скелетные мышцы состоят из отдельных клеток или мышечных волокон, имеющих поперечную исчерченность. В мышечном волокне содержится неспециализированная цитоплазма — саркоплазма и специализированная — киноплазма. У позвоночных саркоплазма, содержащая ядра, располагается на периферии мышечной клетки непосредственно под ее оболочкой — сарколеммой. Киноплазма состоит из белковых фибрилл — миофибрилл. Миофибриллы делятся на толстые, в основном состоящие из белка миозина, и тонкие, состоящие из белков актина и тропомиозина. Благодаря параллельному расположению миофибрилл под микроскопом видна продольная исчерченность мышечного волокна. Поперечная исчерченность зависит от правильного чередования в миофибриллах, расположенных на одном уровне поперечных дисков, которые различно преломляют свет. Анизотропные диски (А) при рассматривании в поляризованном свете характеризуются сильным положительным одноосным двойным лучепреломлением. В обычном свете они темные и имеют приблизительно ту же высоту, что и светлые диски. В поляризованном свете изотропные, светлые диски (I) имеют слабое и трудно обнаруживаемое двойное преломление. Когда мышцы расслаблены, видны тонкие полоски, делящие анизотропные и изотропные диски на равные части. Эти полоски называются инофрагмами.
Строение гладких мышц
Гладкие мышцы состоят из клеток веретенообразной формы, средняя длина которых 100 мкм, а диаметр 3 мкм. Клетки располагаются в составе мышечных пучков и тесно прилегают друг к другу. Мембраны прилежащих клеток образуют нексусы, которые обеспечивают электрическую связь между клетками и служат для передачи возбуждения с клетки на клетку. Гладкие мышечные клетки содержат миофиламенты актина и миозина, которые располагаются здесь менее упорядоченно, чем в волокнах скелетной мышцы. Саркоплазматическая сеть в гладкой мышце менее развита, чем в скелетной.
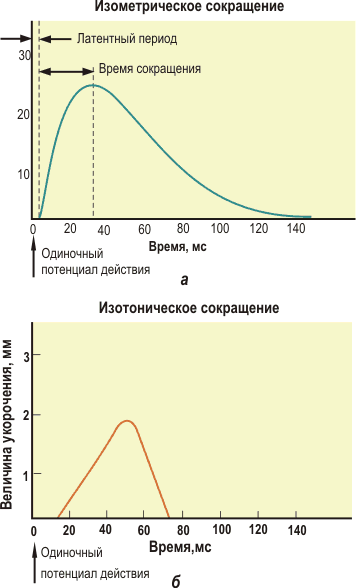
26. Механический ответ отдельного мышечного волокна на одиночный потенциал действия называется одиночным сокращением (twitch). Основные характеристики одиночного изометрического сокращения показаны на рис. 30.20, а. Начало мышечного напряжения запаздывает на несколько миллисекунд по отношению к потенциалу действия. В течение этого латентного периода проходят все этапы электромеханического сопряжения.
Интервал от начала развития напряжения до момента его максимума - это время сокращения. Оно различно для разных типов волокон скелетных мышц. Время сокращения быстрых волокон не превышает 10 мс, тогда как для более медленных волокон оно не меньше 100 мс. Длительность сокращения определяется тем, как долго цитоплазматическая концентрация Са2+ остается повышенной, обеспечивая продолжение циклической активности поперечных мостиков. Время сокращения обусловлено активностью Са2+-АТФазы саркоплазматического ретикулума, которая в быстрых волокнах выше, чем в медленных.
Сравнение одиночных сокращений одного и того же мышечного волокна при разных режимах его деятельности показывает (рис. 30.20, б), что латентный период больше для изотонического сокращения, чем для изометрического, тогда как длительность механического процесса меньше в случае изотонического сокращения (т.е. при укорочении), чем изометрического (т.е. при генерировании силы).
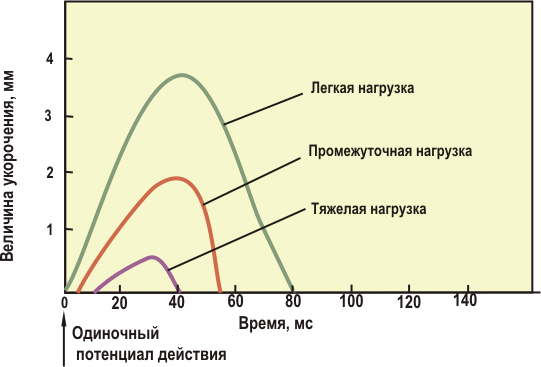
Характеристики изотонического сокращения зависят также от веса поднимаемой нагрузки (рис. 30.21). А именно, при более тяжелой нагрузке:
- латентный период продолжительнее;
- скорость укорочения (величина укорочения мышцы в единицу времени), длительность сокращения и величина укорочения мышцы меньше.
Рассмотрим подробнее последовательность явлений во время изотонического одиночного сокращения. При возбуждении мышечного волокна поперечные мостики начинают развивать силу, однако укорочение не начнется, пока мышечное напряжение не превысит нагрузку на волокно. Таким образом, укорочению предшествует период изометрического сокращения, в течение которого возрастает напряжение. Чем тяжелее нагрузка, тем больше потребуется времени, чтобы оно сравнялось с величиной нагрузки и началось укорочение. Если нагрузку повышать, то в конце концов мышечное волокно не сможет ее поднять, скорость и степень укорочения будут равны нулю и сокращение станет чисто изометрическим.
Электромеханическое сопряжение - это последовательность процессов, в результате которых потенциал действия плазматической мембраны мышечного волокна приводит к запуску цикла поперечных мостиков. Плазматическая мембрана скелетных мышц электрически возбудима и способна генерировать распространяющийся потенциал действия посредством механизма, аналогичного тому, который действует в нервных клетках (см. " Проведение возбуждения между клетками ". Потенциал действия в волокне скелетной мышцы длится 1-2 мс и заканчивается раньше, чем появятся какие-либо признаки механической активности (рис. 30.14). Начавшаяся механическая активность может продолжаться более 100 мс. Электрическая активность плазматической мембраны не оказывает прямого влияния на сократительные белки, а вызывает повышение цитоплазматической концентрации ионов Са2+, которые продолжают активировать сократительный аппарат и после прекращения электрического процесса.
В состоянии покоя в мышечном волокне концентрация свободного ионизированного Са2+ в цитоплазме вокруг толстых и тонких филаментов очень низка, около одной десятимиллионной доли моля/л. При такой низкой концентрации ионы Са2+ занимают очень небольшое количество участков связывания на молекулах тропонина, поэтому тропомиозин блокирует активность поперечных мостиков. После потенциала действия концентрация ионов Са2+ в цитоплазме быстро возрастает, и они связываются с тропонином, устраняя блокирующий эффект тропомиозина и инициируя цикл поперечных мостиков. Источником поступления Са2+ в цитоплазму является саркоплазматический ретикулум мышечного волокна.
Саркоплазматический ретикулум мышц гомологичен эндоплазматическому ретикулуму других клеток. Он располагается вокруг каждой миофибриллы наподобие "рваного рукава", сегментами которого окружены A-диски и I-диски (рис. 30.15). Концевые части каждого сегмента расширяются в виде так называемых латеральных цистерн, соединенных друг с другом серией более тонких трубок. В латеральных цистернах депонируется Са2+; после возбуждения плазматической мембраны он высвобождается.
Отдельную систему составляют поперечные трубочки (T-трубочки), которые пересекают мышечное волокно на границе A-дисков и I-дисков, проходят между латеральными цистернами двух смежных саркомеров и выходят на поверхность волокна, составляя единое целое с плазматической мембраной. Просвет Т-трубочки заполнен внеклеточной жидкостью, окружающей мышечное волокно. Ее мембрана, как и плазматическая, способна к проведению потенциала действия. Возникнув в плазматической мембране, потенциал действия быстро распространяется по поверхности волокна и мембране Т-трубочек в глубь клетки. Достигнув области Т-трубочек, прилегающих к латеральным цистернам, потенциал действия активирует потенциалзависимые "воротные" белки их мембраны, физически или химически сопряженные с кальциевыми каналами мембраны латеральных цистерн. Таким образом, деполяризация мембраны Т-трубочек. обусловленная потенциалом действия, приводит к открыванию кальциевых каналов мембраны латеральных цистерн, содержащих Са2+ в высокой концентрации, и ионы Са2+ выходят в цитоплазму. Повышение цитоплазматического уровня Са2+ обычно бывает достаточным для активации всех поперечных мостиков мышечного волокна.
Процесс сокращения продолжается, пока ионы Са2+ связаны с тропонином, т.е. до тех пор, пока их концентрация в цитоплазме не вернется к исходному низкому значению. Мембрана саркоплазматического ретикулума содержит Са2+-АТФазу - интегральный белок, осуществляющий активный транспорт Са2+ из цитоплазмы обратно в полость саркоплазматического ретикулума. Са2+ высвобождается из ретикулума в результате распространения потенциала действия по Т-трубочкам; для его возвращения в ретикулум нужно гораздо больше времени, чем для выхода. Поэтому повышенная концентрация Са2+ в цитоплазме сохраняется в течение некоторого времени и сокращение мышечного волокна продолжается после завершения потенциала действия.
Подведем итог. Сокращение обусловлено высвобождением ионов Са2+, хранящихся в саркоплазматическом ретикулуме; когда Са2+ поступает обратно в ретикулум, сокращение заканчивается и начинается расслабление (рис. 30.16). Источником энергии для кальциевого насоса служит АТФ - это одна из трех его главных функций в мышечном сокращении
Сократительные белки - это ферменты, в результате каталитической деятельности которых химическая энергия превращается в механическую работу.
Сократительные белки, прежде всего актин, фигурируют и в ряде других клеток и тканей.
Сократительные белки актин и миозин найдены во всех нейронах. Высокая концентрация актина позволяет предположить его непосредственное участие в аксоплазматическом транспорте; однако пока нет четких свидетельств в пользу этой весьма вероятной гипотезы.
| Сократительные белки идентифицированы и в других системах. Из сперматозоидов выделен сократительный АТФ-азный белок спермазин. В хвостовых структурах бактериофагов, как и в движущихся листьях растений (в частности, мимозы), также содержатся АТФ-азные сократительные белки. |
Сократительные белки, прежде всего актин, фигурируют л в ряде других клеток и тканей. Актин составляет около 20 % всего белка в нейронах цыпленка. Актин или актиноподобный белок присутствует в эмбриональной линзе, легких, коже, сердце, поджелудочной железе, почках и в мозговой ткани цыпленка. Ак-тино - и миозиноподобные белки выделены из тромбостеняна, из комплекса сократительных белков в тромбоцитах человека.
| Двигательная функция - сократительные белки вызывают всякое движение. | |
Биохимический цикл мышечного сокращения состоит из 5 стадий:
· 1-2-3 – стадии сокращения;
· 4-5 – стадии расслабления.
1 стадия – в стадии покоя миозиновая «головка» может гидролизовать АТФ до АДФ и Фн, но не обеспечивает освобождения продуктов гидролиза. Образуется стабильный комплекс: миозин-АДФ-Фн.
2 стадия – возбуждение двигательного нерва приводит к освобождению ионов Са2+ из саркоплазматического ритикулума мышечного волокна. Ионы Са2+ связываются тропонином С (Тн-С). В результате этого взаимодействия изменяется конформация всей молекулы тропонина, а затем – тропомиозина. Вследствие этого в актине открываются центры связывания с миозином. Миозиновая «головка» связывается с F-актином, образуя с осью фибриллы угол около 900.
3 стадия – присоединение актина к миозину обеспечивает высвобождение АДФ и Фн из актин-миозинового комплекса. Это приводит к изменению конформации этого комплекса и угол между актином и миозиновой «головкой» изменяется с 900 до 450. В результате изменения угла филаменты актина втягиваются между филаментами миозина, т. е. происходит их скольжение навстречу друг другу. Укорачиваются саркомеры, сокращаются мышечные волокна.
4 стадия – новая молекула АТФ связывается с комплексом актин-миозин.
5 стадия – комплекс миозин-АТФ обладает низким сродством к актину и поэтому происходит отделение миозиновой «головки» от F-актина. Филаменты возвращаются в исходное состояние, мышца расслабляется. Затем цикл возобновляется.
28. Секреция - это функция клеток (групп клеток, органов), представляющая собой совокупность процессов синтеза, резервирования и выведения из клетки в её среду веществ, предназначенных для осуществления определенных функций. Продукт секреции называют секретом.
Различают эндокринную секрецию и экзокринную секрецию. Эндокринная секреция - это функция эндокринных желёз, или желез внутренней секреции. Экзокринная секреция - это функция экзокринных желёз, или желез внешней секреции.
Эндокринные железы - это органы, специализированные на выработке гормонов. Эндокринные железы не имеют выводных протоков. Они выделяют свои продукты секреции - гормоны непосредственно в кровь системы кровообращения. Кроме эндокринных желез гормоны могут вырабатываться в некоторых обособленных группах клеток в составе других органов.
Экзокринные железы - это железы, которые секретируют вещества через проток, открывающийся в одну из полостей тела, имеющую сообщение с внешней средой (например, полость рта, полость тонкой кишки, мочевыводящие пути и т.д.) или во внешнее пространство тела (например на поверхности кожи, глаза).
Существует три механизма секреции. Мерокриновая секреция представляет собой наиболее общий тип секреции и заключается в удалении секретируемых веществ в растворённом состоянии путём диффузии через мембрану клетки. Таким путём происходит, например, выделение гормонов, медиаторов, пищеварительных ферментов. Апокриновая секреция сопровождается отторжением апикальной плазматической мембраны вместе с секретом и некоторыми составными частями цитоплазмы, после чего секретирующая клетка восстанавливается. Этот тип свойствен анальным и молочным железам, коже половых органов и т. д. При голокриновой секреции происходит полное разрушение синтезирующей клетки и её отторжение вместе с секретом от эпителия. Такой тип секреции характерен, например, для сальных желёз. Секреция жидкостей, содержащих высокие концентрации солей (например, пот), часто происходит против осмотических и электрохимических градиентов.






