Бактериоцины – это вещества, которые обладают антибактериальным действием. Впервые были обнаружены А.Грация у E. сoli в 1925 г. Способность к синтезу бактериоцинов обнаружена у различных видов как грамотрицательных, так и грамположительных бактерий.
Бактериоцины вызывают гибель бактерий того же или близких видов, облегчая конкуренцию за жизненно необходимые субстраты внутри отдельного или близкородственных видов. Разнообразие их велико, так же как и диапазон их противомикробного действия: от весьма узкого до чрезвычайно широкого.
В отличие от антибиотиков, секреция (синтез) бактериоцинов сопровождается гибелью клетки-продуцента. В популяции бактерии количество продуцентов бактериоцинов незначительно (в среднем 1:1000 бактерий), их количество при необходимости может резко увеличиваться. Бактериоцины участвуют в формировании и поддержании стабильных бактериальных сообществ (например, в кишечнике человека бактериоцины кишечной палочки вызывают гибель патогенных энтеробактерий — шигелл и сальмонелл).
Бактериоцины – это вещества белковой природы или представленные белком в комплексе с липополисахаридами, но в любом случае за антибактериальную активность бактериоцина отвечает белок. Бактериоцины различаются по спектру действия, по физико-химическим, морфологическим и некоторым другим свойствам.
В большинстве случаев бактериоцины называют в соответствии с видовой принадлежностью бактерий-продуцентов: колицины – Escherichia coli; некоторые авторы используют родовое название бактерий-продуцентов: стафилококкцины – Staphylococcus epidermidis, вибриоцины – Vibrio comma и т. д.
Согласно наиболее принятой классификации Д. Бредли (1967), бактериоцины делят в зависимости от химической природы и свойств на три группы:
1) бактериоцины с низкой молекулярной массой; которые не осаждаются при ультрацентрифугировании; чувствительны к протеолитическому ферменту трипсину, под действием которого они расщепляются на аминокислоты; термостабильны и неразличимы в электронном микроскопе;
2) бактериоцины с высокой молекулярной массой, которые легко осаждаются при ультрацентрифугировании; устойчивы к ферменту трипсину; термолабильны (т.е. подвержены действию температур); выявляются в электронном микроскопе как фагоподобные структуры или их компоненты;
3) бактериоцины, для которых четко показана ферментативная активность.
По механизму действия на бактериальную клетку бактериоцины подразделяют на четыре основные группы:
1) ингибируют окислительное фосфорилирование в цитоплазматической мембране;
2) разрушают ДНК;
3) блокируют синтез белков;
4) нарушают полупроницаемость цитоплазматической мембраны.
Показано, что большинство бактериоцинов проявляют активность, не проникая внутрь клетки. Они передают сигнал на мишень действия посредством цитоплазматической мембраны.
Установлено, что синтез большинства бактериоцинов детерминируется особыми плазмидами, названными бактериоциногенными факторами. Некоторые из этих плазмид передаются при конъюгации, но большинство данных плазмид относится к разряду неконъюгативных.
Кроме того, синтез некоторых бактериоцинов детерминируется также генами, локализованными в бактериальной хромосоме. Это характерно для некоторых грамотрицательных бактерий, например, Pseudomonas aeruginosa, Erwinia chrysanthemi и др.
На биосинтез бактериоцинов оказывают влияние условия культивирования продуцента: состав питательной среды, рН, температура, а также время инкубации продуцента.
Бактериоциногенность (способность к синтезу бактериоцинов) имеет большое значение для развития популяций бактерий. В естественных условиях в результате синтеза бактериоцина одни клетки бактериоциногенной популяции погибают, в то время как большинство клеток сохраняют иммунитет к его действию и вытесняют микроорганизмы других видов, чувствительных к нему. Таким образом формируется определенный микробный ценоз. Необходимо отметить значение микробного ценоза в инфекционной патологии. Способность ряда бактерий синтезировать бактериоцины или другие антимикробные вещества дает этим штаммам селективное преимущество при развитии. Обладая таким преимуществом, патогенные бактерии, например, Vibrio cholerae могут подавлять нормальную микрофлору и активно размножаться в кишечнике человека и животных. Возможно, эти бактерии могут выделять токсические бактериоцины.
Практическое применение бактериоциногенных штаммов бактерий:
1) Для получения бактериоцинов-консервантов, которые используются в пищевых производствах и для консервирования. Например, ежегодно во всем мире тоннами производят низин, продуцируемый лактобактериями.
2) Использование бактериогенных штаммов в качестве заквасочной культуры при различных пищевых производствах. Синтезированный бактериоцин вызывает доминирование нужной микрофлоры и подавление посторонней микрофлоры, что обеспечивает безопасное протекание микробиологических процессов. Например, при производстве сухой колбасы, некоторых сортов салями в качестве заквасочной культуры используется в том числе бактериоциногенный штамм Lactobacillus curvatus, образующий бактериоцин курвацин, который ингибирует рост близкородственных лактобацилл и условно-патогенных бактерий и обеспечивает этим безопасное протекание биохимических процессов при созревании сухой колбасы.
3) Бактериоциногенные штаммы микроорганизмов используют в медицинской практике для лечения заболеваний желудочно-кишечного тракта. Например, выпускаются бактериоциногенные препараты: колибактерин (высушенная суспензия живых бактерий антагонистически активного штамма E. coli М-17), бифидумбактерин (высушенная суспензия живых антагонистически активных бифидобактерий), бификол (высушенная суспензия живых антагонистически активных штаммов бифидобактерий и бактерий E. coli М-17) и др. Такие препараты используют в тех случаях, когда антибиотики при чрезмерном их употреблении приводят к нарушениям витаминного баланса, дисбактериозу (нарушению состава естественной микрофлоры кишечника) и т. п.
4) Бактериоциногенные микроорганизмы используются в научных и лабораторных исследованиях для типирования штаммов бактерий.
Бактериоцины – это совершенно новое направление в микробиологии, биотехнологии, сельском хозяйстве, пищевой промышленности и медицине. Интенсивно это направление развивается в развитых странах Европы, Азии, Америки.
Как аргументы в защиту пользы бактериоцинов для человека можно назвать следующие факты:
1) Бактериоцины человек потребляет с момента своего рождения – с материнским молоком и кисломолочными продуктами.
2) Выявлены бактериоцины, которые продуцируют микроорганизмы нашего кишечника.
3) И самое главное. Любые бактериоцины, в отличие от антибиотиков, полностью расщепляются в организме и вероятность возникновения осложнений от бактериоцинов, по-видимому, минимальна. Применение же антибиотиков, как уже это все хорошо знают, нередко чревато для человека отрицательными последствиями.
Лекция 3. Закономерности роста чистых культур при периодическом выращивании. Кривая роста, характеристика отдельных фаз (лаг-, логарифмической, стационарной, отмирания). Первичные и вторичные метаболиты. Апоптоз
*Рост – это согласованное увеличение количества всех химических компонентов, формирующих клеточные структуры.
В лабораторных и промышленных условиях используют два основных способа культивирования микроорганизмов: периодическое и непрерывное.
Периодическая культура - это популяция клеток в ограниченном жизненном пространстве. Рост бактерий в периодической культуре происходит до тех пор, пока содержание какого-нибудь из необходимых им компонентов питательной среды не достигнет минимума, после чего рост прекращается.
Зависимость концентрации жизнеспособных клеток при периодическом культивировании от длительности инкубирования описывается характерной кривой, которая имеет S-образную форму (рис.). На кривой можно различить несколько основных фаз роста, сменяющих друг друга в определенной последовательности: лаг-фазу; логарифмическую фазу; стационарную фазу; фазу отмирания.
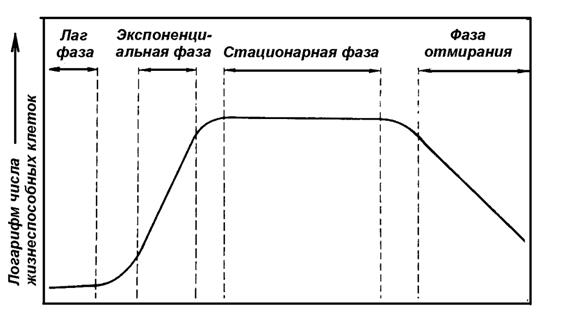
Рис. 1 – Основные фазы кривой роста периодической культуры микроорганизмов
Лаг-фаза охватывает промежуток времени между инокуляцией бактерий (внесением определенного количества бактериального посевного материала в жидкую питательную среду) и достижением ими максимальной скорости деления. В клетках бактерий в этот период идут в основном процессы, связанные с приспособлением их к условиям культивирования. Происходит быстрое увеличение количества РНК (в 8–12 раз).
Продолжительность фазы определяется следующими факторами:
1) начальными условиями культивирования вносимого посевного материала;
2) возрастом посевного материала: чем старше культура, которую используют для инокуляции новой питательной среды, тем большее время занимает лаг-фаза.
Во время лаг-фазы деления клеток не происходит, отмечаются лишь процессы, которые подготавливают клетку к размножению. Лаг-фаза переходит в начальную фазу размножения, когда клетки начинают делиться с постепенно возрастающей скоростью.
Фаза логарифмического (экспоненциального)роста характеризуется постоянной максимальной скоростью деления клеток и скоростью роста. Для различных видов бактерий эти величины могут варьировать в значительных пределах. Например, бактерии E. coli при 37 оС делятся примерно каждые 20 мин, а бактерии родов Nitrosomonas и Nitrobacter – 5–10 ч. В итоге культуры бактерии E. coli вступают в стационарную фазу при концентрации клеток 2–5 . 109/мл.
Характеристика клеток во время логарифмической фазы:
1) все клетки в популяции имеют приблизительно одинаковый размер;
2) содержат максимальное количество РНК, белка, и количество их постоянно;
3) клетки наиболее жизнеспособны;
4) обладают высокой биохимической активностью.
Стационарная фаза наступает тогда, когда число жизнеспособных клеток достигает максимума и не увеличивается, так как скорость размножения бактерий равна скорости их отмирания. В связи с тем, что скорость роста определяется концентрацией субстрата, то еще до его полного использования начинает снижаться и скорость роста, поэтому переход от логарифмической фазы к стационарной происходит постепенно.
Химический состав клеток зависит от фактора, лимитирующего рост. По сравнению с логарифмической фазой роста культур, клетки в стационарной фазе меньше по размеру, содержат меньше РНК, более устойчивы к различного рода воздействиям. В этот период в клетках или в среде культивирования нередко накапливаются продукты вторичного метаболизма.
Продолжительность этой фазы может быть от нескольких часов до нескольких дней в зависимости от вида микроорганизма.
В стационарной фазе роста поведение клеток в бактериальной популяции может регулировать явление, которое получило название апоптоз. Суть его сводится к тому, что при исчерпании питательного субстрата голодающая популяция бактерий разделяется на две субпопуляции, одна из которых погибает и подвергается автолизу, клетки же другой популяции, используя продукты автолиза как субстрат, продолжают размножаться.
В фазе отмирания происходит логарифмическое снижение числа живых клеток. Скорость отмирания бактерий существенно варьирует в зависимости от условий среды и физиологических особенностей организма. Например, энтеробактерии отмирают медленно в отличие от некоторых видов бактерий рода Bacillus, скорость гибели которых происходит быстро. Причины отмирания клеток могут быть разными: накопление в составе питательной среды органических кислот, накоантибиотиков, бактериоцинов, автолиз (автолиз – самопереваривание клеток) и др.
Рассмотрим процесс образования метаболитов на разных этапах роста клетки.
В логарифмической фазе образуются продукты, жизненно важные для роста микроорганизмов: аминокислоты, нуклеотиды, белки, нуклеиновые кислоты, углеводы и т.д. Их называют первичными метаболитами. Первичные метаболиты синтезируются природными микроорганизмами в количествах, необходимых лишь для удовлетворения их потребностей. Поэтому задача промышленных микробиологов состоит в создании мутантных форм микроорганизмов-сверхпродуцентов.
В фазе замедления роста и в стационарной фазе некоторые микроорганизмы синтезируют вещества, не образующиеся в логарифмической фазе и не играющие явной роли в метаболизме. Эти вещества называют вторичными метаболитами. Их синтезируют не все микроорганизмы, а в основном актиномицеты, грибы и спорообразующие бактерии. Промышленное получение вторичных метаболитов представляет огромный интерес, поскольку эти метаболиты – биологически активные вещества: например, антибиотики, гормоны, бактериоцины и т.д. Вторичные метаболиты могут существенно определять экологию микроорганизмов.
Приведенные сведения о первичных и вторичных метаболитах указывают на важность получения знаний об особенностях отдельных фаз при периодическом культивировании. Такие знания позволяют эффективно развивать промышленную микробиологию.






