ќЅўјя ’ј–ј “≈–»—“» ј
ќбща€ характеристика
элементов главной подгруппы VI группы (подгруппы кислорода)
“аблица. Ёлектронное строение и физические свойства.
| ѕор€д- ковый є | Ёлемент | ќтноситель- на€ атомна€ масса | Ёлектронна€ конфигураци€ | јтомный радиус, нм | ѕ» э¬ | Ё.ќ | —тепени окислени€ | t∞пл ∞— | t∞кип ∞— | r г/см3 |
| ислород (O) | 15,9994 | [He] 2s22p4 | 0,066 | 14,5 | 3,5 | -2, -1, +1, +2 | -218,4 | -182,9 | 1,2 (-183∞C) | |
| —ера (S) | 32,06 | [Ne] 3s23p4 | 0,105 | 10,5 | 2,6 | -2, +2, +3, +4, +5, +6 | 112,8 | 444,67 | 2,07 | |
| —елен (Se) | 78,96 | [Ar] 3d104s24p4 | 0,116 | 9,8 | 2,01 | -2, +4, +6 | 4,8 | |||
| “еллур (Te) | 127,60 | [Kr] 4d105s25p4 | 0,143 | 8,6 | 1,9 | -3, +3, +4, +5 | 6,68 | |||
| ѕолоний (Po) | 208,98 | [Xe] 4f145d106s26p4 | 0,176 | 7,8 | 1,76 | +2, +4 | 9,32 |
| ћ≈Ќё | ¬ѕ≈–≈ƒ |
ѕќƒ√–”ѕѕј »—Ћќ–ќƒј
»—Ћќ–ќƒ
ислород O2
( .¬. Ўееле 1772 г., ƒж. ѕристли 1774 г.)
—амый распространенный элемент на «емле; в воздухе - 21% по объему; в земной коре - 49% по массе; в гидросфере - 89% по массе; в составе живых организмов-- до 65% по массе.
—троение атома
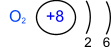
| P11 = 8; n01 = 8; ē = 8 |
| 1s22s22p4 | 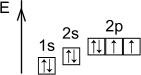
|
‘изические свойства
√аз - без цвета, вкуса и запаха; в 100V H2O раствор€етс€ 3V O2 (н.у.); t∞кип= -183∞—; t∞пл = -219∞C; d по воздуху = 1,1.
—пособы получени€
1. ѕромышленный способ (перегонка жидкого воздуха).
2. Ћабораторный способ (разложение некоторых кислородосодержащих веществ)
2KMnO4 Цt∞Ѓ K2MnO4 + MnO2 + O2≠
2KClO3 Цt∞;MnO2Ѓ 2KCl + 3O2≠
2H2O2 ЦMnO2Ѓ 2H2O + O2≠
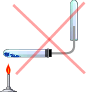
—пособы собирани€
| 
| 
|
| ¬ытеснением воды | ¬ытеснением воздуха |
’имические свойства
¬заимодействие веществ с кислородом называетс€ окислением.
— кислородом реагируют все элементы, кроме Au, Pt, He, Ne и Ar, во всех реакци€х (кроме взаимодействи€ со фтором) кислород - окислитель.
— неметаллами
C + O2 Ѓ CO2
S + O2 Ѓ SO2
2H2 + O2 Ѓ 2H2O
— металлами
2Mg + O2 Ѓ 2MgO
2Cu + O2 Цt∞Ѓ 2CuO
—о сложными веществами
4FeS2 + 11O2 Ѓ 2Fe2O3 + 8SO2
2H2S + 3O2 Ѓ 2SO2 + 2H2O
CH4 + 2O2 Ѓ CO2 + 2H2O
√орение в кислороде

|
ќзон O3
ќзон -аллотропна€ модификаци€ кислорода.
‘изические свойства
√аз, запах свежей хвои, бесцветный, растворим в воде; t∞кип= -112∞—; t∞пл= -193∞C.
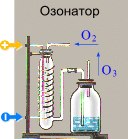
ѕолучение
3O2 Ѓ 2O3
1. ¬о врем€ грозы (в природе), (в лаборатории) в озонаторе
|
2. ƒействием серной кислоты на пероксид бари€
3BaO2 + 3H2SO4 Ѓ 3BaSO4 + 3H2O + O3≠
’имические свойства
1. Ќеустойчив:
O3 Ѓ O2 + O
|
|
|
2. —ильный окислитель:
2KI + O3 + H2O Ѓ 2KOH + I2 + O2
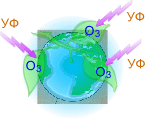
ќбесцвечивает крас€щие вещества, отражает ”‘ - лучи, уничтожает микроорганизмы.
|
—≈–ј » ≈≈ —ќ≈ƒ»Ќ≈Ќ»я
—ера
—ероводород
ќксиды серы
—ерна€ кислота
ѕќƒ√–”ѕѕј »—Ћќ–ќƒј
—≈–ј
S
‘изические свойства
“вердое кристаллическое вещество желтого цвета, нерастворима в воде, водой не смачиваетс€ (плавает на поверхности), t∞кип = 445∞—
јллотропи€
1) ромбическа€ (a - сера) - S8
t∞пл. = 113∞C; r = 2,07 г/см3
Ќаиболее устойчива€ модификаци€.
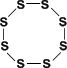
2) моноклинна€ (b - сера) - темно-желтые иглы
t∞пл. = 119∞C; r = 1,96 г/см3
”стойчива€ при температуре более 96∞—; при обычных услови€х превращаетс€ в ромбическую.
3) пластическа€ - коричнева€ резиноподобна€ (аморфна€) масса
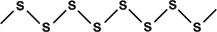
Ќеустойчива, при затвердевании превращаетс€ в ромбическую.
—троение атома
–азмещение электронов по уровн€м и подуровн€м
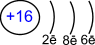
| 1s22p22p63s23p4 | |
| –азмещение электронов по орбитал€м (последний слой) | —тепень окислени€ | ¬алентность |
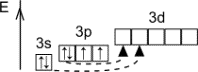
| +2, - 2 | II |
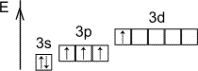
| +4 | IV |
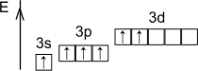
| + 6 | VI |
ѕолучение
1. ѕромышленный метод - выплавление из руды с помощью вод€ного пара.
2. Ќеполное окисление сероводорода (при недостатке кислорода).
2H2S + O2 Ѓ 2S + 2H2O
3. –еакци€ ¬акенродера
2H2S + SO2 Ѓ 3S + 2H2O
’имические свойства
ќкислительные свойства серы
(S0 + 2ē Ѓ S-2)
1) —ера реагирует со щелочными металлами без нагревани€:
2Na + S Ѓ Na2S
c остальными металлами (кроме Au, Pt) - при повышенной t∞:
2Al + 3S Цt∞Ѓ Al2S3
Zn + S Цt∞Ѓ ZnS
2) — некоторыми неметаллами сера образует бинарные соединени€:
H2 + S Ѓ H2S
2P + 3S Ѓ P2S3
C + 2S Ѓ CS2
¬осстановительные свойства сера про€вл€ет в реакци€х с сильными окислител€ми:
(S - 2ē Ѓ S+2; S - 4ē Ѓ S+4; S - 6ē Ѓ S+6)
3) c кислородом:
S + O2 Цt∞Ѓ S+4O2
2S + 3O2 Цt∞;ptЃ 2S+6O3
4) c галогенами (кроме йода):
S + Cl2 Ѓ S+2Cl2
5) c кислотами - окислител€ми:
S + 2H2SO4(конц) Ѓ 3S+4O2 + 2H2O
S + 6HNO3(конц) Ѓ H2S+6O4 + 6NO2 + 2H2O
–еакции диспропорционировани€:
6)
3S0 + 6KOH Ѓ K2S+4O3 + 2K2S-2 + 3H2O
7) сера раствор€етс€ в концентрированном растворе сульфита натри€:
S0 + Na2S+4O3 Ѓ Na2S2O3 тиосульфат натри€
ѕрименение
¬улканизаци€ каучука, получение эбонита, производство спичек, пороха, в борьбе с вредител€ми сельского хоз€йства, дл€ медицинских целей (серные мази дл€ лечени€ кожных заболеваний), дл€ получени€ серной кислоты и т.д.
| Ќј«јƒ | ћ≈Ќё | ћ≈Ќё: ѕќƒ–ј«ƒ≈Ћ | ¬ѕ≈–≈ƒ |
ѕќƒ√–”ѕѕј »—Ћќ–ќƒј
—≈–ќ¬ќƒќ–ќƒ
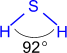
‘изические свойства
√аз, бесцветный, с запахом тухлых €иц, €довит, растворим в воде (в 1V H2O раствор€етс€ 3V H2S при н.у.); t∞пл. = -86∞C; t∞кип. = -60∞—.
ѕолучение
1)
H2 + S t∞Ѓ H2S
2)
FeS + 2HCl Ѓ FeCl2 + H2S≠
’имические свойства
1) –аствор H2S в воде Ц слаба€ двухосновна€ кислота:
|
|
|
H2S ЂH+ + HS- Ђ2H+ + S2-
K1 = ([H+] Х [HS-]) / [H2S] = 1 Х 10-7
K2 = ([H+] Х [S2-]) / [HS-] = 1,3 Х 10-14
—ероводородна€ кислота образует два р€да солей - средние (сульфиды) и кислые (гидросульфиды).
2) ¬заимодействует с основани€ми:
H2S + 2NaOH Ѓ Na2S + 2H2O
3) H2S про€вл€ет очень сильные восстановительные свойства:
H2S-2 + Br2 Ѓ S0 + 2HBr
H2S-2 + 2FeCl3 Ѓ 2FeCl2 + S0 + 2HCl
H2S-2 + 4Cl2 + 4H2O Ѓ H2S+6O4 + 8HCl
3H2S-2 + 8HNO3(конц) Ѓ 3H2S+6O4 + 8NO + 4H2O
H2S-2 + H2S+6O4(конц) Ѓ S0 + S+4O2 + 2H2O
(при нагревании реакци€ идет по - иному:
H2S-2 + 3H2S+6O4(конц) Цt∞Ѓ 4S+4O2 + 4H2O)
4) —ероводород окисл€етс€:
при недостатке O2
2H2S-2 + O2 Ѓ 2S0 + 2H2O
при избытке O2
2H2S-2 + 3O2 Ѓ 2S+4O2 + 2H2O
5) —еребро при контакте с сероводородом чернеет:
4Ag + 2H2S + O2 Ѓ 2Ag2S + 2H2O
6) ачественна€ реакци€ на сероводород и растворимые сульфиды - образование темно-коричневого (почти черного) осадка PbS:
H2S + Pb(NO3)2 Ѓ PbS¯ + 2HNO3
Na2S + Pb(NO3)2 Ѓ PbS¯ + 2NaNO3
Pb2+ + S2- Ѓ PbS¯
ќдной из основных причин потемнени€ художественных картин старых мастеров было использование свинцовых белил, которые за несколько веков, взаимодейству€ со следами сероводорода в воздухе (образуютс€ в небольших количествах при гниении белков; в атмосфере промышленных регионов и др.) превращаютс€ в PbS.
7) –еставраци€:
PbS + 4H2O2 Ѓ PbSO4(белый) + 4H2O
—ульфиды
ѕолучение
1) ћногие сульфиды получают нагреванием металла с серой:
Hg + S Ѓ HgS
2) –астворимые сульфиды получают действием сероводорода на щелочи:
H2S + 2KOH Ѓ K2S + 2H2O
3) Ќерастворимые сульфиды получают обменными реакци€ми:
CdCl2 + Na2S Ѓ 2NaCl + CdS¯
Pb(NO3)2 + Na2S Ѓ 2NaNO3 + PbS¯
ZnSO4 + Na2S Ѓ Na2SO4 + ZnS¯
MnSO4 + Na2S Ѓ Na2SO4 + MnS¯
2SbCl3 + 3Na2S Ѓ 6NaCl + Sb2S3¯
SnCl2 + Na2S Ѓ 2NaCl + SnS¯
’имические свойства
1) –астворимые сульфиды сильно гидролизованы, вследствие чего их водные растворы имеют щелочную реакцию:
K2S + H2O ЂKHS + KOH
S2- + H2O ЂHS- + OH-
2) —ульфиды металлов, сто€щих в р€ду напр€жений левее железа (включительно), растворимы в сильных кислотах:
ZnS + H2SO4 Ѓ ZnSO4 + H2S≠
HgS + H2SO4 Ц\Ѓ
Ќерастворимые сульфиды можно перевести в растворимое состо€ние действием концентрированной HNO3:
FeS2 + 8HNO3 Ѓ Fe(NO3)3 + 2H2SO4 + 5NO + 2H2O
3) ¬одорастворимые сульфиды раствор€ют серу с образованием полисульфидов:
Na2S + nS Ѓ Na2Sn+1 (1 £ n £ 5)
ѕолисульфиды при окислении превращаютс€ в тиосульфаты, например:
2Na2S2 + 3O2 Ѓ 2Na2S2O3
Ќа различной растворимости сульфидов и различной окраске многих из них основан качественный анализ катионов.
| Ќј«јƒ | ћ≈Ќё | ћ≈Ќё: ѕќƒ–ј«ƒ≈Ћ | ¬ѕ≈–≈ƒ |
ѕќƒ√–”ѕѕј »—Ћќ–ќƒј
ќ —»ƒџ —≈–џ
ќксид серы IV
SO2 (сернистый ангидрид; сернистый газ)
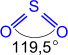
‘изические свойства
Ѕесцветный газ с резким запахом; хорошо растворим в воде (в 1V H2O раствор€етс€ 40V SO2 при н.у.); t∞пл. = -75,5∞C; t∞кип. = -10∞—.
ќбесцвечивает многие красители, убивает микроорганизмы.
ѕолучение
1) ѕри сжигании серы в кислороде:
S + O2 Ѓ SO2
2) ќкислением сульфидов:
4FeS2 + 11O2 Ѓ 2Fe2O3 + 8SO2≠
3) ќбработкой солей сернистой кислоты минеральными кислотами:
Na2SO3 + 2HCl Ѓ 2NaCl + SO2≠ + H2O
4) ѕри окислении металлов концентрированной серной кислотой:
Cu + 2H2SO4(конц) Ѓ CuSO4 + SO2≠ + 2H2O
’имические свойства
1) —ернистый ангидрид - кислотный оксид. ѕри растворении в воде образуетс€ слаба€ и неустойчива€ серниста€ кислота H2SO3 (существует только в водном растворе)
|
|
|
SO2 + H2O ЂH2SO3 K1Ѓ H+ + HSO3- K2Ѓ 2H+ + SO32-
K1 = ([H+] Х [HSO3-]) / [H2SO3] = 1,6 Х 10-2
K2 = ([H+] Х [SO32-]) / [HSO3-] = 1,3 Х 10-7
H2SO3 образует два р€да солей - средние (сульфиты) и кислые (бисульфиты, гидросульфиты).
Ba(OH)2 + SO2 Ѓ BaSO3¯(сульфит бари€) + H2O
Ba(OH)2 + 2SO2 Ѓ Ba(HSO3)2(гидросульфит бари€)
2) –еакции окислени€ (S+4 Ц 2ē Ѓ S+6)
SO2 + Br2 + 2H2O Ѓ H2SO4 + 2HBr
5SO2 + 2KMnO4 + 2H2O Ѓ K2SO4 + 2MnSO4 + 2H2SO4
¬одные растворы сульфитов щелочных металлов окисл€ютс€ на воздухе:
2Na2SO3 + O2 Ѓ 2Na2SO4; 2SO32- + O2 Ѓ 2SO42-
3) –еакции восстановлени€ (S+4 + 4ē Ѓ S0)
SO2 + — Цt∞Ѓ S + —O2
SO2 + 2H2S Ѓ 3S + 2H2O
ќксид серы VI
SO3 (серный ангидрид)
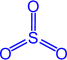
‘изические свойства
Ѕесцветна€ летуча€ жидкость, t∞пл. = 17∞C; t∞кип. = 66∞—; на воздухе "дымит", сильно поглощает влагу (хран€т в запа€нных сосудах).
SO3 + H2O Ѓ H2SO4
“вердый SO3 существует в трех модификаци€х. SO3 хорошо раствор€етс€ в 100%-ной серной кислоте, этот раствор называетс€ олеумом.
ѕолучение
1)
2SO2 + O2 кат;450∞CЃ 2SO3
2)
Fe2(SO4)3 Цt∞Ѓ Fe2O3 + 3SO3≠
’имические свойства
1) —ерный ангидрид - кислотный оксид. ѕри растворении в воде дает сильную двухосновную серную кислоту:
SO3 + H2O Ѓ H2SO4 ЂH+ + HSO4- Ђ2H+ + SO42-
H2SO4 образует два р€да солей - средние (сульфаты) и кислые (гидросульфаты):
2NaOH + SO3 Ѓ Na2SO4 + H2O
NaOH + SO3 Ѓ NaHSO4
2) SO3 - сильный окислитель.
| Ќј«јƒ | ћ≈Ќё | ћ≈Ќё: ѕќƒ–ј«ƒ≈Ћ | ¬ѕ≈–≈ƒ |
ѕќƒ√–”ѕѕј »—Ћќ–ќƒј
—≈–Ќјя »—Ћќ“ј
H2SO4
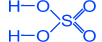
‘изические свойства
“€жела€ масл€ниста€ жидкость ("купоросное масло"); r= 1,84 г/см3; нелетуча€, хорошо растворима в воде Ц с сильным нагревом; t∞пл. = 10,3∞C, t∞кип. = 296∞—, очень гигроскопична, обладает водоотнимающими свойствами (обугливание бумаги, дерева, сахара).

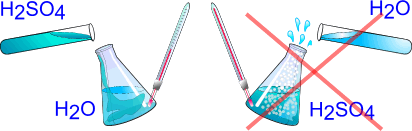
ѕомните!
ислоту вливать малыми порци€ми в воду, а не наоборот!
ѕроизводство серной кислоты
1-€ стади€. ѕечь дл€ обжига колчедана.
4FeS2 + 11O2 Ѓ 2Fe2O3 + 8SO2 + Q
ѕроцесс гетерогенный:
1) измельчение железного колчедана (пирита)
2) метод "кип€щего сло€"
3) 800∞—; отвод лишнего тепла
4) увеличение концентрации кислорода в воздухе
2-€ стади€. ѕосле очистки, осушки и теплообмена сернистый газ поступает в контактный аппарат, где окисл€етс€ в серный ангидрид (450∞— Ц 500∞—; катализатор V2O5):
2SO2 + O2 Ђ2SO3
3-€ стади€. ѕоглотительна€ башн€:
nSO3 + H2SO4(конц) Ѓ (H2SO4 Х nSO3)(олеум)
¬оду использовать нельз€ из-за образовани€ тумана. ѕримен€ют керамические насадки и принцип противотока.
’имические свойства
H2SO4 - сильна€ двухосновна€ кислота
H2SO4 ЂH+ + HSO4- Ђ2H+ + SO42-
ѕерва€ ступень (дл€ средних концентраций) приводит к 100%-ой диссоциации:
K2 = ([H+] Х [SO42-]) / [HSO4-] = 1,2 Х 10-2
1) ¬заимодействие с металлами:
a) разбавленна€ серна€ кислота раствор€ет только металлы, сто€щие в р€ду напр€жений левее водорода:
Zn0 + H2+1SO4(разб) Ѓ Zn+2SO4 + H2O≠
b) концентрированна€ H2+6SO4 Ц сильный окислитель; при взаимодействии с металлами (кроме Au, Pt) может восстанавливатьс€ до S+4O2, S0 или H2S-2 (без нагревани€ не реагируют также Fe, Al, Cr - пассивируютс€):
|
|
|
2Ag0 + 2H2+6SO4 Ѓ Ag2+1SO4 + S+4O2≠ + 2H2O
8Na0 + 5H2+6SO4 Ѓ 4Na2+1SO4 + H2S-2≠ + 4H2O
2) концентрированна€ H2S+6O4 реагирует при нагревании с некоторыми неметаллами за счет своих сильных окислительных свойств, превраща€сь в соединени€ серы более низкой степени окислени€, (например, S+4O2):
—0 + 2H2S+6O4(конц) Ѓ C+4O2≠ + 2S+4O2≠ + 2H2O
S0 + 2H2S+6O4(конц) Ѓ 3S+4O2≠ + 2H2O
2P0 + 5H2S+6O4(конц) Ѓ 5S+4O2≠ + 2H3P+5O4 + 2H2O
3) с основными оксидами:
CuO + H2SO4 Ѓ CuSO4 + H2O
CuO + 2H+ Ѓ Cu2+ + H2O
4) с гидроксидами:
H2SO4 + 2NaOH Ѓ Na2SO4 + 2H2O
H+ + OH- Ѓ H2O
H2SO4 + Cu(OH)2 Ѓ CuSO4 + 2H2O
2H+ + Cu(OH)2 Ѓ Cu2+ + 2H2O
5) обменные реакции с сол€ми:
BaCl2 + H2SO4 Ѓ BaSO4¯ + 2HCl
Ba2+ + SO42- Ѓ BaSO4¯
ќбразование белого осадка BaSO4 (нерастворимого в кислотах) используетс€ дл€ идентификации серной кислоты и растворимых сульфатов.
| MgCO3 + H2SO4 Ѓ MgSO4 + | H2O + CO2≠ |
| H2CO3 |
MgCO3 + 2H+ Ѓ Mg2+ + H2O + CO2≠
ѕолезные свойства селена
 —елен (также как и витамин —, витамин ј ивитамин ≈) €вл€етс€ одним из важнейших компонентов антиоксидантной защиты организма от свободных радикалов. ќ свободных радикалах и их вредоносном воздействии на организм знают уже практически все. ѕравда, не все осознают насколько губительно и опасно дл€ организма накопление в организме свободных радикалов, а также какие заболевани€ возникают при систематическом воздействии свободных радикалов на компоненты клеточных мембран и генетический материал клеток. ¬се заболевани€ не перечесть: от преждевременного старени€ кожных покровов до онкологических заболеваний. »менно поэтому нельз€ недооценивать важность нашей антиоксидантной защитной системы.
—елен (также как и витамин —, витамин ј ивитамин ≈) €вл€етс€ одним из важнейших компонентов антиоксидантной защиты организма от свободных радикалов. ќ свободных радикалах и их вредоносном воздействии на организм знают уже практически все. ѕравда, не все осознают насколько губительно и опасно дл€ организма накопление в организме свободных радикалов, а также какие заболевани€ возникают при систематическом воздействии свободных радикалов на компоненты клеточных мембран и генетический материал клеток. ¬се заболевани€ не перечесть: от преждевременного старени€ кожных покровов до онкологических заболеваний. »менно поэтому нельз€ недооценивать важность нашей антиоксидантной защитной системы.
¬ чем же значимость именно селена?
—елен Ц важнейший элемент антиоксидантной защиты организма. ¬итамины, флавоноиды, коэнзимы не могут заменить селен. ќн входит в состав глютатионпероксидазы Ц фермента, обезвреживающего самые опасные и агрессивные свободные радикалы, именно те, с которыми другие антиоксиданты справитьс€ не в состо€нии. ≈сли селена недостаточно, то это наиважнейшее звено антиоксидантной защиты просто не работает.
Ќедостаток селена не только снижает иммунитет и работоспособность, но и приводит к развитию сердечно-сосудистых и онкологических заболеваний, накоплению т€желых металлов и преждевременному старению, сахарному диабету и болезн€м суставов, мужскому бесплодию и родовой слабости у женщин.
ƒатские ученые показали, что селен преп€тствует развитию болезней сердца и артерий, а его дефицит увеличивает риск коронарной болезни сердца на 70%.
—елен предохран€ет от отравлений свинцом, кадмием, ртутью, табачным дымом и выхлопными газами. ќн предотвращает разрушение и некроз печени, способству€ выведению из организма т€желых металлов. јллергические заболевани€ и риск развити€ бронхиальной астмы тесно св€заны с обменом селена.
¬ ‘инл€ндии после введени€ селена в пищевой рацион населени€ количество сердечно-сосудистых патологий уменьшилось в 2,5 раза, число онкозаболеваний сократилось в 1,8 раза, болезней эндокринной системы Ц на 77%.
ѕо данным »нститута питани€ –јћЌ и результатам клинических исследований 80% росси€н испытывают недостаток селена. ¬ 1994 году ћинистерство здравоохранени€ –‘ прин€ло решение об устранении дефицита селена у жителей –оссии.
—войства селена
Ј —еленвходит в состав более 200 гормонов и ферментов организма, регулиру€ работу всех органов и систем.
Ј ѕри участии селена образуетс€ 80% энергии (ј“‘) у человека.
Ј ѕрием растительной формы (селен-метионина), не только замедл€ет процесс старени€, но и отодвигает его, т.к. увеличиваетс€ активность стволовых клеток.
Ј «апускаетс€ процесс антиоксидантной защиты
Ј ѕовышаетс€ двигательна€ активность; по€вл€етс€ бодрость, прекращаютс€ головные боли, головокружени€, улучшаетс€ сон, настроение, нормализуетс€ аппетит.
Ј ”частвует в синтезе кофермента Q-10, обеспечивает молодость сердца, сосудов, суставов, позвоночника; улучшает состо€ние кожи, волос, ногтей. Ќормализует активность гормонов щитовидной железы.
Ј —одержитс€ в наибольшем количестве в ткан€х печени, печек, мозга, сперме (входит в состав мужского полового гормона тестостерона) и т.д.
Ј ќказывает лечебный эффект при включении в комплексное лечение, при кардиопати€х различной этиологии, при гепатитах, панкреатитах, заболевани€х кожи, уха, горла, носа и т.д. ќбщеизвестна его роль в профилактике и лечении злокачественных новообразований.
Ј явл€етс€ основным компонентом фермента пероксидазы глютатиона (глутатиона), который защищает организм от вредных веществ, образующихс€ при распаде токсинов. —елен антагонист ртути и мышь€ка, способен защитить организм от кадми€, свинца, талли€.
|
|
|
Ј ѕоказан при планировании семьи Ц обоим супругам; женщинам в период беременности и кормлени€ грудью, восстановлени€ после родов.
лассификаци€ селена
1. —елен органический натуральный. ¬ виде селен-метионина содержитс€ в растени€х.
2. —елен органический искусственный. —елен соединен с искусственно созданным белком (пример Ђ—елен-активї). ѕринимают короткими курсами. ѕротивопоказано беременным и корм€щим женщинам, дет€м до 14 лет
3. —елен дрожжевой. ƒрожжи помещают в раствор неорганического селена. ѕолученна€ Ѕјƒ содержит до 20-30% органического селена, преобразованного дрожжами, и 70-80% остаетс€ в неорганической форме. ѕринимают короткими курсами. »з-за наличи€ дрожжевой флоры возможно развитие грибкового дисбактериоза.
4. —елен минеральный (неорганический): ѕрием только под контролем врача по результатам обследовани€ на селен (пример ЂЌеоселенї). »збыточное поступление в организм приводит к образованию и накоплению токсичной формы Ц гидроселениданиона.
”сво€емость селена организмом
ѕриродна€ форма Ц селенметионин, селенцистеинЦ наиболее предпочтительна дл€ организма в св€зи с высокой усво€емостью 95-98%. ∆ивотна€ же форма селена усваиваетс€ на 30%, неорганическа€ форма селена Ц на 10%.
—уточна€ норма селена
1. 80-200 мкг Ц суточна€ норма селен-метионина, селен-цистеина дл€ взрослого человека.
2. ¬ периоды повышенных нагрузок, а также при различных заболевани€х Ц суточна€ норма подлежит корректировке в сторону повышени€ до 500-1000 мкг.
акие продукты содержат селен?
Ј —елен содержитс€ в морской и каменной сол€х, в почках (свиных, гов€жьих и тел€чьих), в печени и сердце, в €йцах птицы, к тому же в желтке еще есть и витамин ≈. Ѕогаты селеном продукты морей Ч рыба, особенно сельдь, не слишком доступные всем крабы, омары, лангусты, креветки и более доступные кальмары. —елена нет в обработанных продуктах Ч консервах и концентратах, а во всех вареных, рафинированных продуктах его наполовину меньше, чем в свежих.
Ј »з продуктов растительного происхождени€ богаты селеном пшеничные отруби, проросшие зерна пшеницы, зерна кукурузы, помидоры, пивные дрожжи, грибы и чеснок, а также черный хлеб и другие продукты из муки грубого, помола.
Ј ¬ молоке корм€щей матери в 2 раза больше селена и в 5Ч6 раз больше витамина ≈, чем в коровьем молоке. «амечено, что младенцы-мальчики умирают чаще девочек. »звестный гематолог-онколог ё. јлексадрович объ€сн€ет это тем, что именно мальчикам требуетс€ гораздо больше селена, чем девочкам, поэтому если вместо материнского молока они получают коровье, в их организме недостает этого микроэлемента.
ѕоследстви€ хронического дефицита селена:
Ј –ост мужского и женского бесплоди€, падение рождаемости
Ј –ост патологий беременности и родов, врожденной патологии новорожденных
Ј –ост частоты психических и физических отклонений здоровь€ в детском и подростковом возрасте
Ј –езкое увеличение заболеваемости Ђболезн€ми цивилизацииї, нарастание частоты т€желого и хронического течени€ заболеваний, смертности от них, снижение качества и продолжительности жизни, по€вление новых вирусных болезней и рост агрессивности известных
Ј теллур
»стори€
¬первые был найден в 1782 году в золотоносных рудах “рансильвании горным инспектором ‘ранцом »озефом ћюллером (впоследствии барон фон –ейхенштейн), на территории јвстро-¬енгрии. ¬ 1798 году ћартин √енрих лапрот выделил теллур и определил важнейшие его свойства.
ѕроисхождение названи€
ќт латинского tellus, родительный падеж telluris, «емл€.
Ќахождение в природе
—одержание в земной коре 1Ј10−6 % по массе. »звестно около 100 минералов теллура. Ќаиболее часты теллуриды меди, свинца, цинка, серебра и золота. »зоморфна€ примесь теллура наблюдаетс€ во многих сульфидах, однако изоморфизм Te Ч S выражен хуже, чем в р€ду Se Ч S, и в сульфиды входит ограниченна€ примесь теллура. —реди минералов теллура особое значение имеют алтаит PbTe, сильванит AgAuTe4, калаверит AuTe2, гессит Ag2Te, креннерит (Au, Ag)Te, петцит Ag3AuTe2, мутманнит (Ag, Au)Te, монбрейит Au2Te3, нагиагит [Pb5Au(Te, Sb)]4S5, тетрадимит Bi2Te2S. ¬стречаютс€ кислородные соединени€ теллура, например “еќ2 Ч теллурова€ охра.
¬стречаетс€ самородный теллур и вместе с селеном и серой (€понска€ теллуриста€ сера содержит 0,17 % “е и 0,06 % Se).
“ипы месторождений
Ѕольша€ часть упом€нутых минералов развита в низкотемпературных золото-серебр€ных месторождени€х, где они обычно выдел€ютс€ после основной массы сульфидов совместно с самородным золотом, сульфосол€ми серебра, свинца, а также с минералами висмута. Ќесмотр€ на развитие большого числа теллуровых минералов, главна€ масса теллура, извлекаемого промышленностью, входит в состав сульфидов других металлов. ¬ частности, теллур в несколько меньшей степени, чем селен, входит в состав халькопирита медно-никелевых месторождений магматического происхождени€, а также халькопирита, развитого в медноколчеданных гидротермальных месторождени€х. “еллур находитс€ также в составе пирита, халькопирита, молибденита и галенита месторождений порфировых медных руд, полиметаллических месторождений алтайского типа, галенита свинцово-цинковых месторождений, св€занных со скарнами, сульфидно-кобальтовых, сурьм€но-ртутных и некоторых других. —одержание теллура в молибдените колеблетс€ в пределах 8 Ч 53 г/т, в халькопирите 9 Ч 31 г/т, в пирите до 70 г/т.
ѕолучение
ќсновной источник Ч шламы электролитического рафинировани€ меди и свинца. Ўламы подвергают обжигу, теллур остаетс€ в огарке, который промывают сол€ной кислотой. »з полученного сол€нокислого раствора теллур выдел€ют, пропуска€ через него сернистый газ SO2.
ƒл€ разделени€ селена и теллура добавл€ют серную кислоту. ѕри этом выпадает диоксид теллура “еќ2, а H2SeO3 остаетс€ в растворе.
»з оксида “еќ2 теллур восстанавливают углем.
ƒл€ очистки теллура от серы и селена используют его способность под действием восстановител€ (Al) в щелочной среде переходить в растворимый дителлурид динатри€ Na2Te2:
6Te + 2Al + 8NaOH = 3Na2Te2 + 2Na[Al(OH)4].
ƒл€ осаждени€ теллура через раствор пропускают воздух или кислород:
2Na2Te2 + 2H2O + O2 = 4Te + 4NaOH.
ƒл€ получени€ теллура особой чистоты его хлорируют
Te + 2Cl2 = TeCl4.
ќбразующийс€ тетрахлорид очищают дистилл€цией или ректификацией. «атем тетрахлорид гидролизуют водой:
TeCl4 + 2H2O = TeO2 + 4HCl,
а образовавшийс€ “еќ2 восстанавливают водородом:
TeO2 + 4H2 = Te + 2H2O.
÷ены
“еллур Ч редкий элемент, и значительный спрос при малом объЄме добычи определ€ет высокую его цену (около 200Ч300 долл. за кг в зависимости от чистоты), но, несмотр€ на это, диапазон областей его применени€ посто€нно расшир€етс€.
‘изико-химические свойства
“еллур Ч хрупкое серебристо-белое вещество с металлическим блеском. ¬ тонких сло€х на просвет красно-коричневый, в парах Ч золотисто-жЄлтый.
’имически теллур менее активен, чем сера. ќн раствор€етс€ в щелочах, поддаетс€ действию азотной и серной кислот, но в разбавленной сол€ной кислоте раствор€етс€ слабо. — водой металлический теллур начинает реагировать при 100 ∞C, а в виде порошка он окисл€етс€ на воздухе даже при комнатной температуре, образу€ оксид TeO2.
ѕри нагреве на воздухе теллур сгорает, образу€ TeO2. Ёто прочное соединение обладает меньшей летучестью, чем сам теллур. ѕоэтому дл€ очистки теллура от оксидов их восстанавливают проточным водородом при 500Ч600 ∞C.
¬ расплавленном состо€нии теллур довольно инертен, поэтому в качестве контейнерных материалов при его плавке примен€ют графит и кварц.
ѕолоний






