Приклад 1.
Проаналізуємо послідовність перетворення у сплаві, з вмістом 0,3 % Карбону під час його охолодження і розглянемо криву охолодження (рис. 2, а).
Спочатку на діаграмі Fe–Fe3C (рис. 2, б) проводимо вертикальну лінію І, що відповідає заданому складу сплаву, позначаємо точки перетинання її з лініями діаграми послідовно цифрами (точки 0...6). За правилом фаз Ґіббса для кожної точки визначаємо кількість ступеней вільності та перевіряємо правильність побудови кривої охолодження.
Від точки 0 до точки 1 відбувається просте фізичне охолодження рідкого розчину. Наявна одна фаза ( ). Число ступеней вільності в цьому інтервалі дорівнює:
). Число ступеней вільності в цьому інтервалі дорівнює:
 (6)
(6)
На кривій охолодження відзначаємо нахилену ділянку 0 – 1, яка означає, що охолодження проходить з певною швидкістю.

Рис. 2. Приклад графічного розв’язку завдання
За температури, що відповідає точці 1 починають виділятися кристали твердого розчину  –фериту. З пониженням температури об’єм кристалічної фази збільшується, а кількість рідкого розчину зменшується. Концентрація рідини змінюється по лінії АB, а вміст твердої фази — по лінії АН. У точці 2 кристалізація завершується й структура сплаву складає лише однорідний твердий розчин
–фериту. З пониженням температури об’єм кристалічної фази збільшується, а кількість рідкого розчину зменшується. Концентрація рідини змінюється по лінії АB, а вміст твердої фази — по лінії АН. У точці 2 кристалізація завершується й структура сплаву складає лише однорідний твердий розчин  –фериту.
–фериту.
Від точки 1 до точки 2, як уже відомо, продовжується із рідкого розчину виділятися  – ферит, маємо дві фази:
– ферит, маємо дві фази:
 (7)
(7)
Поява кристалів твердої фази ( –фериту) супроводжується виділенням прихованої теплоти кристалізації, а тому на кривій охолодження з’являється перегин в точці 1 і відрізок між точками 1–2 змінює нахил (швидкість охолодження зменшується).
–фериту) супроводжується виділенням прихованої теплоти кристалізації, а тому на кривій охолодження з’являється перегин в точці 1 і відрізок між точками 1–2 змінює нахил (швидкість охолодження зменшується).
У точці 2 (температура 1493 ºС) відбувається перитектичне перетворення, коли в рівновазі перебувають одночасно три фази: рідкий розчин, ферит і аустеніт:
 (8)
(8)
Маємо нонваріантну рівновагу:
 , (9)
, (9)
а це означає, що трифазний стан існує за сталої температури. На кривій охолодження маємо горизонтальну лінію 2 – 2′.
Від точки 2 до точки 3 відбувається кристалізація залишків рідкої фази в аустеніт унаслідок виділення значної кількості прихованої теплоти кристалізації, фаз при цьому дві (рідкий розчин і аустеніт):
 (10)
(10)
У точці 3 повністю завершується кристалізація, утворюється однорідний твердий розчин — аустеніт. Охолодження проходить з певною швидкістю, а тому на кривій охолодження маємо нахилену ділянку 2′ – 3.
Від точки 3 до точки 4 відбувається просте фізичне охолодження аустеніту без перетворень, наявна одна фаза — аустеніт:
 (11)
(11)
Охолодження аустеніту проходить з певною швидкістю і на кривій охолодження в точці 3 утворюється перегин, що вказує на збільшення швидкості охолодження, оскільки припиняється виділення теплоти перетворення.
Від точки 4 до точки 5 частина аустеніту перекристалізовується у ферит (Fe  → Fe
→ Fe  ), фаз при цьому дві (аустеніт і ферит):
), фаз при цьому дві (аустеніт і ферит):
 (12)
(12)
Концентрація аустеніту змінюється по лінії GS, а фериту — по лінії GP. Охолодження двофазного сплаву триває, але з меншою швидкістю, тому в точці 4 буде перегин.
У точці 5 відбувається евтектоїдне перетворення, коли у рівновазі перебувають три фази: аустеніт, ферит і цементит вторинний:
 . (13)
. (13)
Знову маємо нонваріантну рівновагу:
 (14)
(14)
Перетворення проходить за сталої температури. На кривій охолодження маємо горизонтальну лінію 5 – 5′.
Від точки 5 до точки 6 є виділення цементиту третинного з фериту, але цементиту дуже мало і це практично не відбивається на нахилі кривої. Структура сплаву на цій ділянці — ферит і перліт, а фаз буде дві (ферит і цементит вторинний):
 (15)
(15)
Охолодження проходить з певною швидкістю і на кривій маємо нахилену ділянку 5′–6. Рівноважна структура сплаву після охолодження до кімнатної температури — перліт і ферит надлишковий (рис. 1).
 Приклад 2.
Приклад 2.
За діаграмою фазової рівноваги залізовуглецевих сплавів із застосуванням правила відрізків (важеля) проведемо кількісний аналіз сплаву, що містить 1,2 % Карбону. Аналізуємо вертикальну лінію ІІ (рис. 2, б), що відповідає концентрації заданого сплаву, точніше точки перетину — точки 0...5. За правилом фаз Ґіббса перевіряємо правильність побудови кривої охолодження (рис. 2.9.3, в), аналізуємо перетворення, що відбуваються у сплаві під час охолодження.
До температури точки 1 сплав перебуває в рідкому стані. За цієї температури починається його кристалізація з утворенням кристалів аустеніту, яка відбувається в інтервалі температур від точки 1 до точки 2. Аустеніт, що закристалізувався, охолоджується до температури точки 3 без перетворень. За цієї температури з аустеніту починає виділятися надлишковий Карбон з утворенням цементиту вторинного. Виділення вторинного цементиту продовжується до температури точки 4 (727 ˚С). У результаті цього перетворення вміст Карбону в аустеніті зменшується і при температурі 727 ˚С сягає евтектоїдної концентрації — 0,76 % С. Такий аустеніт при постійній температурі 727 ˚С перетворюється в перліт за евтектоїдною реакцією. Сплав отримує структуру перліту і цементиту вторинного, яка зберігається при подальшому охолодженні до кімнатної температури.
Застосовуючи правило відрізків, проведемо кількісний фазовий аналіз заданого сплаву (С = 1,2 %) за температури 1400 °С. Для цього через фігуративну точку t (рис. 2, б) проводимо горизонтальну лінію до перетину з двома найближчими суцільними лініями діаграми, а саме — лініями BC і JE. У точці а вона перетне лінію JE,що є границею з однофазною областю аустеніту, а у точці b —перетне лінію ВС, що є границею з рідиною. Отже, заданий сплав за температури 1400 °С складається з двох фаз — аустеніту й рідкого розчину.
Для визначення концентрації компонентів (Fe і C)у сплаві та у кожній із двох фаз (аустеніті й рідкому розчині) спроектуємо точки t, a і b на вісь концентрацій (абсцису), отримавши точки t ′ —концентрацію Карбону у сплаві (С = 1,2 %), a ′ —в аустеніті (С =0,71 %), b ′ —у рідкому розчині (С =1,98%).
Для визначення кількісного співвідношення фаз користуємося відрізком ab Величини відрізків цієї лінії між заданою точкою t і точками a і b — обернено пропорційні до кількостей цих фаз (у нашому випадку аустеніту й рідкого розчину) і записуються співвідношенням:
 . (16)
. (16)
 Якщо прийняти довжину всього відрізка (
Якщо прийняти довжину всього відрізка ( ) за 100 %, то кількісний вміст аустеніту й рідкого розчину можна визначити із залежностей:
) за 100 %, то кількісний вміст аустеніту й рідкого розчину можна визначити із залежностей:
 ;
;  , (17)
, (17)
де  – кількість сплаву;
– кількість сплаву;
 – кількість аустеніту;
– кількість аустеніту;
 – кількість рідкого розчину.
– кількість рідкого розчину.
У нашому випадку довжини відрізків  ,
,  ,
,  матимуть значення:
матимуть значення:
 ;
;
 ; (18)
; (18)
 .
.
Отже, для заданого сплаву, що містить 1,2 % С, за температури 1400 ºС кількість відповідних фаз (аустеніту та рідкого розчину) становитиме:
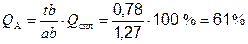 , (19)
, (19)
 . (20)
. (20)
Практична частина
- Накреслити діаграму стану залізо–вуглець (карбід заліза), вказати фази і структурні складові в усіх областях діаграми.
- Охарактеризувати компоненти, фази і перетворення.
- Побудувати схему кривої охолодження (нагрівання) для сплаву із вмістом X % вуглецю, підтвердивши правильність її побудови правилом фаз Гіббса.
- Використовуючи правило відрізків, визначити фазовий склад сплаву із вмістом X % вуглецю при температурі t ºС, концентрацію компонента в кожній фазі даного сплаву та кількісне співвідношення відповідних фаз.






