План
1. Общие сведения.
2. Абсорбция.
2.1 Материальный баланс.
2.2 Рабочая линия процесса абсорбции.
2.3 Движущая сила процесса.
3. Адсорбция.
3.1 Материальный баланс.
3.2 Движущая сила процесса.
3.3 Типы адсорбентов
4. Аппараты для проведения процесса абсорбции адсорбции.
Общие сведения.
Абсорбция - процесс избирательного поглощения компонентов газовой (паровой) смеси жидким поглотителем.
Абсорбируемые компоненты газовой (паровой) смеси называют – абсорбтивом
Жидкий поглотитель – абсорбентом.
Неабсорбированная часть газовой (паровой) смеси называется – инертом.
Если поглощение абсорбтива осуществляется путем его растворения в абсорбенте, то такой процесс называется – физической абсорбцией.
Когда растворение абсорбтива сопровождается химической реакцией между ним и абсорбентом, то этот процесс называется – хемосорбцией.
Обратный процесс в сорбционных процессах называется – десорбцией.
Адсорбция — это поглощение поверхностью твердого тела того или другого компонента из газа или жидкости. Поглощающее вещество, называемое адсорбентом, должно иметь весьма большую поверхность. В качестве адсорбентов используются специально приготавливаемые угли, гель кремневой кислоты, глинозем и другие вещества. Поглощение газа поверхностью тела не сопровождается его конденсацией. Однако в капиллярах сорбента может происходить конденсация поглощаемого газа. Это явление называется капиллярной конденсацией.
Абсорбция.
Абсорбцию применяют:
- для насыщения воды, безалкогольных напитков, пива и некоторых сортов вин углекислым газом;
- для улавливания паров этилового спирта из газов, выделяемых при брожении в спиртовом и винодельческом производствах;
- для уменьшения влажности воздуха в хранилищах складских помещениях, лаб.оборудовании с использованием абсорбентов – конденсированных кислот.
Материальный баланс.
В производстве абсорбция осуществляется в противоточных аппаратах непрерывного действия, в которых газ и жидкость (сорбент) приводятся в тесный контакт. Схема такого аппарата (абсорбера) представлена на рис. 1. Инертный непоглощаемый газ (V в кмоль/ч) при входе в аппарат содержит некоторое количество поглощаемого компонента. Обозначим его концентрацию в кмоль/кмоль инертного газа через yн.

Рис. 1. Схема абсорбера.
При прохождении газовой смеси через абсорбер количество инертного газа не изменяется, а концентрация поглощаемого компонента уменьшается до ук кмоль/кмоль.
Жидкий сорбент поступает в абсорбер в количестве W кмоль/ч. Содержание поглощаемого компонента в жидкости: при ее поступлении в абсорбер Хн кмоль/кмоль чистого сорбента; при выходе из аппарата - Хк.
На основании закона сохранения вещества может быть составлено уравнение материального баланса абсорбционного процесса для поглощаемого компонента:
 (1)
(1)
При составлении баланса мы пренебрегаем возможными потерями при проведении процесса. Из уравнения 1 имеем:
 (2)
(2)
где G — количество компонента, переданного из одной фазы в другую, в кмоль/ч.
Из уравнения 2 вытекает, что
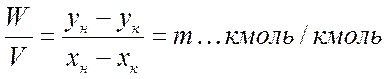 (3)
(3)
где m - удельный расход сорбента.
Рабочая линия процесса абсорбции
Уравнение 2 является уравнением прямой линии, построенной в координатах х - у. На рис. 2 эта линия обозначена А - В. Угловой коэффициент этой линии равен m, T. e. tg ά = m.
Линия А-В называется рабочей линией. При помощи этой линии устанавливается связь между составом жидкости и составом газа для любого сечения аппарата. Так, если в каком-то сечении аппарата содержание поглощаемого компонента в газе ус, то содержание этого компонента в жидкости будет равно хс см. рис. 2.
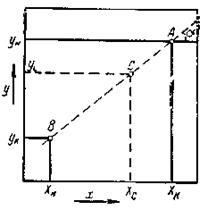
Рис.2 Рабочая линия абсорбера
Движущая сила процесса.
Рабочая линия, изображенная на рис. 2, позволяет установить условия, при которых процесс абсорбции станет возможным. Рассмотрим условия равновесия газа и сорбента. Применим для этого правило фаз. В рассматриваемом случае мы имеем две фазы (газ и жидкость) и три компонента (поглощаемый компонент, инертный газ и жидкость). Определяющими параметрами будут давление, температура и концентрации:
S = K - f+2.
В нашем случае, когда поглощается один компонент газовой смеси,
S = 3 - 2+2 = 3,
где S - число степеней свободы;
К-число компонентов системы;
f - число фаз системы.
Этими тремя степенями свободы будут состав одной из фаз, давление и температура. Содержание поглощаемого компонента в другой фазе не может быть выбрано произвольно. Оно определяется выбранными тремя параметрами.
Для идеальных растворов, в которых силы взаимодействия между молекулами компонентов системы одинаковы, условия равновесия определяются законами Генри и Рауля. Закон Генри можно формулировать так:
х = рψ, (4)
где к - количество растворенного газа, отнесенное к поглощающей жидкости, в
моль-долях.
Уравнение 4 называется законом Генри, который может быть сформулирован так: растворимость газа прямо пропорциональна парциальному давлению газа над жидкостью.
Известно также, что в газовой смеси парциальное давление компонента может быть выражено уравнением:
Р = УР, (5)
где у - моль-доля рассматриваемого компонента в газовой
смеси;
Р - общее давление в смеси.
Приравнивая р из уравнений 4 и 5, получим
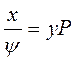 и
и 
или 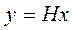
где 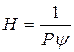 (6)
(6)
Уравнение 6 является уравнением фазового равновесия. Для идеальных растворов, для которых закон Генри точен, величина Н является постоянной и линия равновесия является прямой.
Так как при сильном разбавлении все растворы приближаются к идеальным, то в области низких концентраций линия равновесия является прямой.
Величина Н называется константой фазового равновесия.
В общем случае зависимость между у и х представляется кривой, которая называется кривой равновесия. Кривая равновесия обычно строится на основании экспериментальных данных. Мы можем заметить, что кривая эта (или прямая в частном случае) строится в тех же координатах, что и рабочая линия процесса абсорбции.
Очевидно, что для протекания процесса абсорбции линия равновесия должна проходить ниже рабочей линии рис. 3 На рис. линия OD представляет собой кривую равновесия, соответствующую уравнению у = Нх.

Рис. З. Рабочая линия и линия равновесия фаз.
Рассмотрим произвольное сечение аппарата, в котором жидкая фаза содержит ХА% поглощаемого компонента. Равновесное содержание этого компонента равно уА% Согласно рабочей линии в рассматриваемом сечении, в газовой фазе того же компонента содержится УА%. Очевидно, в данной точке действующей силой процесса будет величина (уА— У*а), изображаемая отрезком NP. Как видно из рис. 3, движущая сила будет меняться по высоте аппарата.






