Переход свободного холестерола из клеток на ЛПВП обусловлен разницей его концентраций на поверхности клеточных мембран и липопротеиновых частиц. Следовательно, он продолжается до тех пор, пока не выровняется концентрация холестерола между донором (поверхность мембран) и акцептором (ЛПВП). Поддержание градиента концентрации обеспечивается постоянным превращением свободного холестерола, поступающего на ЛПВП, в эфиры холестерола. Эта реакция, как уже указывалось, катализируется ферментом лецитин-холестерол-ацилтрансферазой (ЛХАТ[8]).
Происхождение свободного и эстерифицированного ХС в плазме крови
| Липопротеин | Свободный холестерол | Эфиры холестерола |
| ХМ | Синтез в слизистой кишечника | Свободный холестерол |
| ЛПОНП | Гепатоциты | АХАТ гепатоцитов |
| ЛПНП | Гепатоциты | АХАТ гепатоцитов - 60% ЛХАТ плазмы - 40% |
| ЛПВП | Периферические клеточные мембраны - 70% ЛПОНП, ЛПНП - 30% | ЛХАТ плазмы - 100% |
гидрофобными соединениями (в отличие от свободного холестерола, у которого имеется гидроксильная группа, сообщающая ему гидрофильность). В силу своей гидрофобности эфиры холестерола теряют способность к диффузии и не могут вернуться обратно в клетку. Они формируют гидрофобное ядро внутри частиц, благодаря которому ЛПВП приобретают сферическую форму. Здесь, в кровотоке из таких ЛПВП осуществляется транспорт вновь образованных неполярных ЭХ из ЛПВП на ХМ, ЛПОНП, ЛППП, который ускоряется за счет белков-переносчиков (см. выше). Затем происходит опосредованное рецепторами поступление ЛПВП, как и других богатых ЭХ липопротеинов, в гепатоциты с последующим их катаболизмом. В частности, высвобождающиеся эфиры холестерола служат исходным субстратом для образования желчных кислот. Аккумуляция холестерола в сосудистой стенке происходит вследствие дисбаланса между поступлением его в интиму сосудов и его выходом. В результате такого дисбаланса холестерол там накапливается. В центрах накопления холестерола формируются структуры - атеромы. Наиболее известны два фактора, которые вызывают дисбаланс в обмене холестерола. Во-первых, это изменения частиц ЛПНП (гликозилирование, перекисное окисление липидов, гидролиз фосфолипидов, окисление апо В). Поэтому они захватываются специальными клетками - "мусорщиками" (главным образом, макрофагами). Захват липопротеиновых частиц с помощью "мусорных" рецепторов протекает бесконтрольно. В отличие от апо В/Е - опосредованного эндоцитоза это не вызывает регуляторных эффектов, направленных на снижение поступления в клетку ХС, описанных выше. В результате макрофаги переполняются липидами, теряют функцию поглощения отходов и превращаются в пенистые клетки. Последние задерживаются в стенке кровеносных сосудов и начинают секретировать факторы роста, ускоряющие клеточное деление. Возникает атеросклеротическая пролиферация клеток.
Организационно- методические указания лаборантскому составу:
Подготовить мультимедийную презентацию лекции в Power Point и flash проекциях
Лекция подготовлена доц. каф. Свергун В.Т.
Дата
Министерство здравоохранения Республики Беларусь
Учреждение образования
«Гомельский государственный медицинский университет»
Кафедра___биохимии______________________________________________
Обсуждено на заседании кафедры _(МК или ЦУНМС)___________________
Протокол № __________200___года
ЛЕКЦИЯ
по ________биохимии_______________________________________
(наименование дисциплины)
для студентов 2_______курса___лечебного___факультета
Тема: Липиды 3. Липолиз. Тканевой обмен липидов ______________________________________________
Обсуждено на заседании кафедры (МК или ЦУНМС)____________________
Протокол № _______
ЛИТЕРАТУРА
1.Биохимия человека:, Р.Марри, Д.Греннер, П.Мейес, В.Родуэлл.- М.книга,2004.- т.1.
,с..
2.Основы биохимии:А.Уайт, Ф.Хендлер,Э.Смит, Р.Хилл, И.Леман.-М. книга,
1981,т. 1-.2,.с.
3.Наглядная биохимия: Кольман., Рем К.-Г-М.книга 2004г.
4.Липиды, липопротеиды и атеросклероз: А.Н.Климов, Н.Г.Никульчева,,книга,
Питер,1995г.
МАТЕРИАЛЬНОЕ ОБЕСПЕЧЕНИЕ
1.Мультимедийная презентация
РАСЧЕТ УЧЕБНОГО ВРЕМЕНИ
| №п/п | Перечень учебных вопросов | Количество выделяемого Времени в минутах |
| 1. | Липолиз, механизм мобилизации жира | |
| 2. | ||
| 3. |
Всего 90 минут
Вопрос 1. Механизм мобилизации жира (роль гормонов, цАМФ и ионов Са+).
Содержащиеся в организме человека массой 70 кг триацилглицеролы (ТАГ) могут дать 100.000 ккал энергии: белки – 60.000 ккал; гликоген – 6.000 ккал; глюкоза - 400 ккал. ТГ составляют 90% среди всех липидов, содержащихся в организме. Наиболее часто встречающимися жирными кислотами в их составе являются олеиновая (18:1), пальмитиновая (16:0) и линолевая (18:2) кислоты. На их долю приходится 75% всех жирных кислот. В норме более 95% ТГ находится в жировой ткани. Оставшиеся 5% локализованы преимущественно в печени и мышцах. При голодании, тяжелом СД, некоторых других состояниях, при которых жир мобилизуется из жировой ткани(ЛИПОЛИЗ) для энергетических целей, количество ТГ в печени увеличивается.
Жировая ткань функционально специализируется на хранении (запасании) и мобилизации ТАГ. При этом за 2-3 недели в адипоците происходит полное их обновление. Схематически процессы синтеза - гидролиза ТАГ изображены ниже.
Предшественниками для синтеза ТАГ являются глицерол-3-фосфат и активированные жирные кислоты. В печени глицерол-3-фосфат может образовываться или в результате фосфорилирования глицерина, или из глюкозы как промежуточный продукт гликолиза. В жировой ткани отсутствует фермент глицеролкиназа; поэтому единственным источником образования глицерол-3-фосфата является гликолиз.Жировая ткань функционально специализируется на хранении (запасании) и мобилизации ТАГ.
Предшественниками для синтеза ТАГ являются глицерол-3-фосфат и активированные жирные кислоты. В печени глицерол-3-фосфат может образовываться или в результате фосфорилирования глицерина, или из глюкозы как промежуточный продукт гликолиза. В жировой ткани отсутствует фермент глицеролкиназа; поэтому единственным источником образования глицерол-3-фосфата является гликолиз.
Жировая ткань функционально специализируется на хранении (запасании) и мобилизации ТАГ. При этом за 2-3 недели в адипоците происходит полное их обновление. Схематически процессы синтеза - гидролиза ТАГ изображены ниже.
Фосфорилирование активирует гормон-чувствительную липазу, тем самым ускоряется гидролиз ТАГ. Адреналин, норадреналин, глюкагон и АКТГ так же активируют этот фермент, в то время как инсулин вызывает его дефосфорилирование, снижая активность
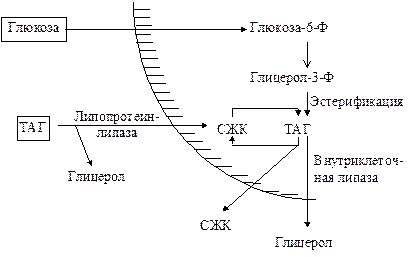
Депонирование жира в жировой ткани сопряжено с питанием и гормональным статусом, которые направлены на стимуляцию поглощения глюкозы. Активация жирных кислот происходит путем их превращения в ацил~КоА под влиянием фермента - ацил~КоАсинтетазы.
Гидролиз триацилглицеролов опосредован липазными ферментами. Активность липазы в клетках жировой ткани находится под строгим регуляторным контролем (отсюда название - гормон-чувствительная липаза). Фермент проявляет субстратную специфичность к ТАГ, 1,2-диацилглицеролам, 2-моноацилглицеролам и эфирам холестерола. Активность гормон-чувствительной липазы регулируется путем фосфорилирования-дефосфорилирования, которые опосредует фермент цАМФ-зависимая протеинкиназа. В результате полного гидролиза молекулы ТАГ образуется 3 молекулы жирных кислот и 1 молекула глицерола. Глицерол из жировой ткани попадает в печень и используется там как предшественник в синтезе глюкозы путем глюконеогенеза. Жирные кислоты выходят из адипоцитов в плазму крови. Они используются любыми тканями, клетки которых содержат митохондрии, способные окислять жирные кислоты с выделением энергии. Однако преимущественно эти жирные кислоты утилизируются в клетках сердечной, скелетных мышц и печени. Другим важным источником ТГ являются ЛП плазмы крови.
Метаболизм ТАГ в жировой ткани скоординирован с анаболической и катаболической фазами метаболизма на уровне целого организма. Вслед за перевариванием пищи в плазме крови увеличивается концентрация глюкозы, инсулина, липопротеинов, богатых ТАГ. Наряду с этим стимулируется образование ТАГ в жировой ткани. В развитие этой анаболической фазы вовлечены переносчики глюкозы и гликолиз; стимулируется активность ЛПЛ для гидролиза ТАГ в составе липопротеинов и снижается активность жиромобилизующей липазы в жировой ткани. Натощак или при повышенной потребности в энергии во время физической работы, повышении уровня катехоламинов, гормона роста, АКТГ и глюкагона в плазме крови, снижении секреции инсулина эти процессы меняются на противоположные - увеличивается липолиз, высвобождаются жирные кислоты, используемые в качестве источника энергии, и глицерол - для глюконеогенеза
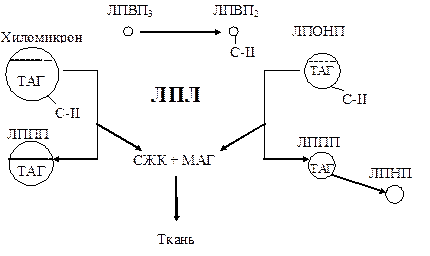
Олеиновая кислота (18:1 w 9) или цис - 9 - октадеценовая кислота.
Линолевая кислота (18:2 w 6) или цис -9-цис-12 -октадекадиеновая кислота.
Линоленовая кислота (18:3 w 3) или цис-9, цис-12, цис-15-октадека-триеновая кислота.
Арахидоновая кислота (20:4 w 6) или (эйкозатетраен-5,8,11,14-овая кислота), цис-5, цис-8, цис-11, цис-14- эйкозатетраеновая кислота.
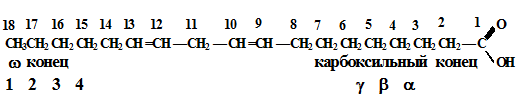
Характерно, что все двойные связи в составе жирных кислот организма имеют цис-конфигурацию Двумя преобладающими мононенасыщенными жирными кислотами животных липидов являются олеиновая и пальмитолеиновая. Олеиновая кислота наиболее широко распространена в природе и преобладает в количественном отношении. Среди полиненасыщенных жирных кислот в тканях млекопитающих наиболее часто встречается линолевая кислота, содержащая две двойные связи, линоленовая - с тремя двойными связями и арахидоновая - с четырьмя двойными связями. Ненасыщенность жирных кислот существенно влияет на их свойства. С увеличением числа двойных связей снижается температура плавления жирных кислот, возрастает их растворимость в неполярных растворителях. Все ненасыщенные жирные кислоты, встречающиеся в природе, при комнатной температуре являются жидкостями. Олеиновая кислота (18:1 w 9) или цис - 9 - октадеценовая кислота.
Линолевая кислота (18:2 w 6) или цис -9-цис-12 -октадекадиеновая кислота.
Линоленовая кислота (18:3 w 3) или цис-9, цис-12, цис-15-октадека-триеновая кислота.
Арахидоновая кислота (20:4 w 6) или (эйкозатетраен-5,8,11,14-овая кислота), цис-5, цис-8, цис-11, цис-14- эйкозатетраеновая кислота.
Транспорт свободных жирных кислот (СЖК) в плазме крови
Как уже упоминалось, основными потребителями СЖК являются клетки сердечной и скелетной мышц, печени. Для этих тканей характерно поглощение 30%-40% СЖК, содержащихся в артериальной крови. Основными СЖК плазмы крови являются пальмитиновая и олеиновая.
Комплекс СЖК - альбумин. Вследствие сильной гидрофобности >99% жирных кислот плазмы циркулируют в нековалетно связанном с альбумином состоянии. Важнейшей функцией альбумина, наиболее распространенного белка во внеклеточной жидкости, является связывание небольших, плохо растворимых в воде молекул. На молекуле альбумина имеется 3 центра связывания, к которым присоединяется 10 и более молекул жирных кислот. В плазме имеется небольшая концентрация жирных кислот, которые не связаны с альбумином, но уравновешены с комплексом альбумин-жирные кислоты. Они могут диффундировать через эндотелий капилляров и поглощаться тканями. Присутствие альбумина обеспечивает существование мощного резервуара жирных кислот в непосредственной близости к тканям всего организма.
Вклад СЖК плазмы крови в энергетический обмен. Период полужизни СЖК плазмы короток (около 1,5 мин), а оборот СЖК плазмы значительный и составляет около 200г/сутки. Если бы все они подверглись окислению, то выделилось бы 1800 ккал энергии. На самом деле, значительная часть этих жирных кислот используется для эстерификации ТАГ.
Оценка вклада СЖК плазмы крови в энергетический обмен
человека
| Параметр | Значение |
| Масса | 70 кг |
| Объем плазмы | 3 л |
| СЖК плазмы (средн. концентрация) | 0,5 ммоль |
| Молекулярная масса СЖК (средн.) | |
| Период полужизни СЖК плазмы | 1,5 мин |
| Оборот СЖК плазмы | 10 ммоль/л 720 ммоль/сутки 201,6 г/сутки |
| Калорический коэффициент оборота (9 ккал/г) | 1818 ккал/сутки |
| Калорическая потребность (умеренная активность) | 2350 ккал/сут |
| Максимальный вклад оборота СЖК плазмы в калорическую потребность | 77% |






